Газета «Новости медицины и фармации» №15-16 (775-777), 2021
Вернуться к номеру
Делирий в неврологической практике
Авторы: Дубенко О.Е., Никонов В.В.
Харьковская медицинская академия последипломного образования, г. Харьков, Украина
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Термин «делирий» введен в медицинскую литературу, по одним данным, в I веке до н.э. и происходит от латинского глагола delilare, что означает дословно «выходить из себя». По другим данным, термин «делирий» введен древнеримским ученым по имени Корнелий Цельс в I веке н.э. и происходит от латинских терминов delirium — «безумие, бред»; deliro — «безумствую, брежу». Однако с самого начала термин «делирий» использовался как синоним сумасшествия, безумия, спутанности сознания [1].
В современном понимании делирий утратил прежнее значение как исключительно психопатологическое состояние и расценивается, скорее, как острая недостаточность мозга вследствие диффузного нарушения метаболизма. Клиническое значение делирия состоит в том, что он связан с повышенными показателями смертности, с более длительным пребыванием в больнице и помещением в дом престарелых, с плохим функциональным восстановлением. Делирий — частое неврологическое проявление у пожилых пациентов, госпитализированных по общему заболеванию. Исследования показали связь между делирием и неблагоприятными исходами, такими как длительное пребывание в больнице, повышенная внутрибольничная смертность, более высокие показатели повторной госпитализации, а также с когнитивным снижением и худшим функциональным исходом и дополнительным экономическим бременем [2]. Распространенность делирия среди пациентов, госпитализированных в медицинские учреждения, колеблется от 10 до 31 %, достигая > 50 % среди ослабленных пожилых пациентов [3].
Делирий как концепция восходит к эпохе Гиппократа и пережил неоднократные попытки определения и переопределения за последние 2000 лет. Этот термин часто употребляют для описания преходящего психического синдрома, сопровождающего соматические заболевания, в частности эпизоды лихорадки. В психиатрической литературе делирий называют острым органическим мозговым синдромом, в неврологической — токсической энцефалопатией, в общемедицинском смысле данный термин используется для описания белой горячки. При этом точно известно, что это единственное психическое состояние, вызванное нарушением метаболизма мозга. Это относительно распространенное заболевание, особенно у пожилых людей с физическим заболеванием, с высокой заболеваемостью и смертностью, часто недооцененное и недолеченное, имеющее острую и витиеватую психиатрическую симптоматику и разнообразную феноменологию [4].
В некоторых источниках делирий относят к продуктивным нарушениям сознания и определяют как острое помрачение сознания с грубой дезориентировкой в окружающей действительности и нарушением когнитивных функций (память, речь, ориентировка в месте и времени), нарушением восприятия (иллюзии, галлюцинации), нарушением цикла сна, быстрой сменой эмоций, повышением психомоторной активности и активности автономной системы [5]. В МКБ-10 диагностические критерии делирия представлены следующим образом: для постановки точного диагноза симптомы, легкие или тяжелые, должны присутствовать в каждой из следующих областей [6]:
1. Нарушение сознания и внимания (от помутнения до комы; снижение способности направлять, фокусировать, поддерживать и переключать внимание).
2. Глобальное нарушение познавательных функций (искажения восприятия, иллюзии и галлюцинации — чаще всего визуальные; нарушение абстрактного мышления и понимания с преходящими иллюзиями или без них; нарушение немедленного воспроизведения и недавних воспоминаний, но с относительно неповрежденной отдаленной памятью; дезориентация во времени, а в более тяжелых случаях — в месте и собственной личности).
3. Психомоторные расстройства (гипо- или гиперактивность и непредсказуемые переходы от одного к другому; увеличение времени реакции; усиление или уменьшение плавности речи; усиление реакции испуга).
4. Нарушение цикла «сон — бодрствование» (бессонница или, в более тяжелых случаях, полная потеря сна или изменение цикла «сон — бодрствование»; дневная сонливость; ночное ухудшение симптомов; тревожные сны или кошмары, которые могут продолжаться в виде галлюцинаций после пробуждения).
5. Эмоциональные расстройства, например депрессия, тревога или страх, раздражительность, эйфория, апатия или блуждание, замешательство.
Согласно 5-й версии классификации и диагностики ментальных расстройств DSM-5 и МКБ-11, делирий относится к группе нейрокогнитивных расстройств [7] и характеризуется наличием истинных, преимущественно зрительных, галлюцинаций и иллюзий и, как следствие, вторичным бредом, наличием эмоциональных (аффективных) нарушений, сенестопатиями, затрудненной ориентировкой в окружающем мире, дезориентацией во времени. При этом сохраняются осознание собственной личности и опасностей. Эмоциональное состояние больного зависит от характера галлюцинаций. Больной может быть опасен для себя и окружающих. После выхода из делирия наблюдается частичная конградная амнезия (амнезируются реальные события и болезненные воспоминания). В DSM-5 предложены диагностические критерии делирия (табл. 1).
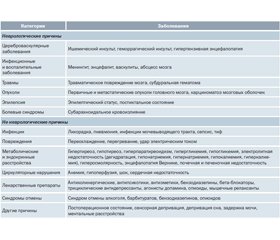
Делирий — это острое, преходящее, обычно обратимое флуктуирующее нарушение уровня сознания, внимания, познавательной деятельности, причиной которого может быть практически любое заболевание или лекарственное средство (табл. 2).
Клинические проявления делирия могут быть достаточно разнообразны, но многие авторы подчеркивают три главных симптомокомплекса: нарушения сознания, нарушения памяти, нарушение цикла «сон — бодрствование». Для нарушения сознания характерны флуктуации, часто с ухудшением вечером, когда уменьшается внешняя стимуляция. Бдительность и внимание к окружающей обстановке могут быть снижены или ложно преувеличены, характерно повышенное тревожное состояние, повышенное внимание ко всем внешним раздражителям без разбора. Иногда нарушения сознания могут быть незначительными, например затруднение оценки течения времени. Нарушение внимания — еще одна ключевая клиническая особенность делирия: при беседе наблюдается нарушение концентрации внимания и повышенная отвлекаемость. Цикл «сон — бодрствование» почти всегда нарушен, с выраженными периодами сонливости днем и бессонницей ночью. Мышление также нарушено. Речь может быть замедленной или, наоборот, ускоренной, со снижением способности выносить суждения и понимать абстрактные понятия, мысли становятся несвязными и неорганизованными. Может показаться, что пациент отрезан от внешнего мира и все больше занят внутренними мыслями и переживаниями. Нарушение памяти — еще одна характерная черта делирия. В первую очередь нарушается кратковременная, немедленная или рабочая память, что подтверждается тестами на внимание, такими как повторение цифр в течение нескольких секунд; страдает и более длинная антероградная память (например, умение запоминать некоторые слова и обращаться к ним через 2–5 минут). Неспособность отслеживать время во время делирия может иногда приводить к появлению ложных воспоминаний, конфабуляций. Возможны нарушения психомоторного поведения в виде малой спонтанной активности при легком нарушении, хотя галлюцинации или иллюзии могут вызывать быструю двигательную активность. Могут наблюдаться сложные стереотипные движения — ощупывание или ковыряние и даже имитация профессиональных действий.
Клиническое разнообразие проявлений дало основание некоторым авторам выделять 2 формы делирия: гиперактивный и гипоактивный.
Концепция подтипов делирия была первоначально введена Липовски, который предложил использовать термины «гиперактивный» и «гипоактивный» для описания двигательного поведения пациентов (беспокойство и агрессия в сравнении с низкой активностью и апатией). Позднее была добавлена третья, «смешанная» категория, в которую были включены пациенты с симптомами обоих подтипов [8, 9]. Последующие наблюдения подтвердили клиническую полезность подтипов делирия, и по этой теме были опубликованы два системных обзора [10, 11]. Гипоактивный делирий обычно привлекает меньше клинического внимания, чем гиперактивный. Как и любой делирий, он может возникать у самых разных пациентов и в различных условиях, и, следовательно, с ним сталкиваются многие группы врачей. Его бывает труднее распознать, и он связан с худшими исходами, чем гиперактивный делирий. При гипоактивном делирии преобладают симптомы сонливости и бездействия, тогда как гиперактивный делирий характеризуется беспокойством и ажитацией. В некоторых случаях наблюдается сочетание этих подтипов. Все формы делирия представляют собой синдром, характеризующийся резкими изменениями по сравнению с исходным уровнем способности пациента сохранять внимание и осведомленность, что сопровождается другими нарушениями познавательной деятельности, которые развиваются в течение короткого периода времени (от часов до дней) и имеют тенденцию колебаться по степени тяжести в течение дня. Делирий может быть физиологическим последствием медицинского состояния, синдрома отмены психоактивных веществ или состояния интоксикации, воздействия токсинов или их комбинации [12]. Существует предположение, что гипоактивный вариант делирия может быть связан с тяжестью основного заболевания и состоянием пациента. Возможно, гиперактивный подтип может развиваться у физически здоровых людей, а гипоактивный делирий может быть индикатором тяжести соматического состояния пациентов. Это также согласуется с предположением о том, что пожилой возраст может быть предрасполагающим фактором для развития гипоактивного делирия и косвенным индикатором тяжести у пожилых, которые чаще страдают от нескольких заболеваний, чем более молодые пациенты [13].
Патофизиология
Расстройство высших корковых функций при делирии является свидетельством распространенной дисфункции в различных областях мозга — подкорковых структурах, стволе головного мозга, таламусе, недоминантной теменной доле, фузиформной и префронтальной коре, а также первичной моторной коре. Поражения правого полушария являются предрасполагающим фактором, это обусловлено тем, что лобная и теменная кора правого полушария обеспечивают функцию внимания. Инфаркты мозга в бассейне правой средней мозговой артерии чаще сопровождаются возбуждением и делирием.
Несмотря на клиническое значение, патофизиология делирия остается малоизученной. Имеются данные о том, что в его патогенезе играет роль холинергическая недостаточность. Во-первых, факторы риска делирия включают метаболические и структурные аномалии головного мозга, связанные с уменьшением активности ацетилхолина. Во-вторых, высокий уровень антихолинергической активности в сыворотке крови ассоциируется с тяжестью делирия [14]. На сегодняшний день центральный холинергический дефицит — ведущий предполагаемый механизм делирия, другие гипотезы включают избыток дофамина и воспаление.
Роль холинергической регуляции в формировании нейрокогнитивных расстройств обусловлена распространенностью холинергических синапсов в структурах нервной системы с образованием массивных нейрональных сетей, высокой представленностью холинергических нейронов в структурах головного мозга, играющих ключевую роль в формировании когнитивных функций, декларативной памяти, обучения и внимания. Холинергические пути имеют широкие взаимосвязи, посылая проекции в базальные отделы переднего мозга, понтомезенцефальные нейроны, стриатум и в конечном итоге — в кору мозга. Этот медиатор обеспечивает также сложные двигательные функции — инициацию движений, двигательные стереотипы. Существует восемь групп холинергических клеток, от которых начинаются проводящие пути в различные отделы центральной нервной системы, — базальное ядро Мейнерта, медиальное ядро перегородки, гиппокамп, поясную извилину, гипоталамус, миндалевидные тела, обонятельную луковицу. В эксперименте электрическая стимуляция базального ядра Мейнерта, расположенного в области внутренней капсулы ниже медиального сегмента бледного шара, приводит к высвобождению ацетилхолина. Другая группа холинергических нейронов сконцентрирована в области покрышки среднего мозга — это педункулопонтинное ядро. Его активность максимальна в период бодрствования и уменьшается в период медленноволнового сна. Холинергические рецепторы в коре и гиппокампальной области относятся к типу мускариновых М1. Мускариновые ацетилхолиновые рецепторы широко представлены в мозге и играют значительную роль в патогенезе делирия. Мускариновые рецепторы обеспечивают активирующее, растормаживающее действие на слой пирамидных клеток коры, никотиновые рецепторы оказывают тормозное влияние на кору. Никотиновые ацетилхолиновые рецепторы модулируют когнитивные функции, память, внимание, бодрствование. Основная психофизиологическая роль ацетилхолина связана с обеспечением запоминания новой информации, а его дефицит нарушает процесс перехода кратковременной памяти в долговременную. Также ацетилхолин играет ключевую роль в обеспечении устойчивого внимания за счет активирующего влияния на префронтальную кору. Дисфункция базальной холинергической системы приводит к повышенной отвлекаемости, сниженной концентрации внимания. Известно также, что медиатором, обеспечивающим запоминание вербальных и зрительных образов, также является ацетилхолин. Исследования с использованием структурной и функциональной нейровизуализации подтверждают наличие изменений в холинергических путях у пациентов с делирием. При болезни Альцгеймера атрофия базальных ядер переднего мозга приводит к недостаточности холинергической системы. Как и при болезни Альцгеймера, дефицит холинергических функций может быть ответственным за когнитивные нарушения при делирии [15]. Исследования подтверждают схожесть механизмов развития делирия и болезни Альцгеймера, которые включают нарушение синтеза ацетилхолина, повреждение холинергических синаптических механизмов, нейротрансмиттерный дисбаланс. Делирий и болезнь Альцгеймера могут быть двумя точками в континууме когнитивных расстройств, и существует четкая связь между этими состояниями. Холинергический дефицит имеет место при обоих состояниях и обусловлен нейрональной гибелью, снижением синтеза ацетилхолина и нейроиммунным ответом. При обоих состояниях введение ингибиторов ацетилхолинэстеразы способствует улучшению когнитивных функций [16].
Анестезирующие вещества, ингибирующие постсинаптические никотиновые рецепторы, могут вызывать когнитивные расстройства после хирургических вмешательств. Антихолинергические вещества и их метаболиты индуцируют делирий путем антагонистического воздействия на постсинаптические мускариновые рецепторы. Антихолинергические токсины и медикаменты ингибируют ацетилхолиновые интернейроны путем блокады постсинаптических М1 мускариновых рецепторов, вызывая галлюцинации и когнитивный дефицит. Делирий-индуцирующие медикаменты могут оказывать антагонистическое воздействие на пресинаптические и постсинаптические ацетилхолиновые рецепторы. Препараты, влияющие на пресинаптические отделы, препятствуют высвобождению ацетилхолина в синапс. Опиаты и каннабиноиды связывают регуляторные G-протеинсвязанные рецепторы, что ингибирует открытие кальциевых каналов, блокируя пресинаптическую деполяризацию и нарушая холинергическую трансмиссию. Этанол вызывает апоптоз холинергических нейронов, повреждение пресинаптических терминалей, холинергический дефицит и снижение порога для развития делирия.
Холинергическая система балансируется моноаминергической активностью, дисфункция которой также может быть связана с развитием делирия. Допамин, эпинефрин и серотонин играют важную роль в регуляции цикла «сон — бодрствование», опосредуя физиологический ответ на стимулы. Этот ответ также модулируется холинергическими путями. Таким образом, при делирии происходит взаимодействие между холинергическими путями и моноаминами. Норэпинефрин играет важную роль в модуляции внимания, настроения, тревоги. Повышение норадренергической активности ассоциируется с развитием гиперактивного делирия. Норэпинефрин контролирует допаминергические нейроны в мезокортексе. Таким образом, дисбаланс холинергической/норадренергической оси также может лежать в основе патофизиологии делирия [17].
Делирий и инсульт
Пациенты с острым инсультом особенно предрасположены к развитию этого клинического осложнения. Зачастую делирий у этих пациентов недостаточно диагностируется и лечится, в то время как его развитие оказывает влияние на продолжительность пребывания в больнице, уровень смертности, функциональный исход и снижение когнитивных функций. Хотя делирий обычно является транзиторным состоянием, он усугубляет тяжесть состояния после острого инсульта. Ряд исследований выявил более высокую частоту делирия у пациентов с инсультом (13–48 %) по сравнению с 10–25 % у пациентов, госпитализированных в отделения общей внутренней медицины, при этом госпитализированные пациенты с делирием имеют повышенный уровень смертности и более длительную госпитализацию. Пожилой возраст, инфекция мочевыводящих или респираторных органов и предшествующие когнитивные нарушения являются обычными предрасполагающими условиями [18]. Таким образом, делирий наблюдается примерно у одной трети пациентов, перенесших острый инсульт, и связан с более высокой смертностью, более длительной госпитализацией и зависимостью после выписки. Раннее распознавание и профилактика делирия у пациентов с инсультом могут улучшить клинические исходы и облегчить планирование выписки [19]. Наличие делирия сразу после госпитализации по поводу острого инсульта представляет диагностические трудности. В систематическом обзоре и метаанализе обнаружено, что делирий поражает от 10 до 30 % пациентов в острой фазе инсульта. Пациенты с постинсультным делирием имели менее благоприятные клинические исходы. В частности, вероятность смерти в больнице и в течение 12 месяцев после выписки у них была в 4,7 раза выше. Более того, пациенты с делирием после инсульта, как правило, имеют худшие функциональные результаты и с большей вероятностью будут переведены в учреждения длительного лечения, так как требуют дальнейшего медицинского обследования [20]. Наиболее частыми предрасполагающими факторами были пожилой возраст, пол, этиология инсульта и его локализация, а также наличие предшествующих когнитивных нарушений/деменции. На сегодняшний день наиболее изученными провоцирующими факторами являются пневмония, инфекции мочевыводящих путей и синдром игнорирования (связанный с правополушарной локализацией инсульта), исходами постинсультного делирия — функциональная зависимость, длительность пребывания в стационаре, постинсультные когнитивные нарушения или деменция, краткосрочная и долгосрочная смертность [21].
Инструменты, которые используются для скрининга или диагностики делирия в общих терапевтических или хирургических отделениях интенсивной терапии, могут быть адаптированы для группы пациентов с первичным неврологическим повреждением. В общей интенсивной терапии клиницист (то есть медсестра или врач) должен рассматривать такие клинические данные, как колебания психического статуса и невнимательность, как потенциальные предвестники его развития. Делирий при критических состояниях ассоциирован с выживаемостью, продолжительностью пребывания в стационаре, стоимостью и долгосрочным прогнозом для когнитивных функций, и, хотя причинно-следственная связь остается недоказанной, раннее распознавание делирия остается важным. Очевидно, что оценка делирия у пациентов с нейрокритическими заболеваниями сложнее, чем у общих терапевтических и общих хирургических пациентов. Некоторые из них не поддаются тестированию на делирий из-за снижения уровня сознания (например, комы) вследствие первичного неврологического повреждения или из-за глубокого седативного воздействия. У пациентов с инсультом, например, могут быть коммуникативные нарушения из-за афазии, что делает оценку делирия особенно сложной. Однако при некоторых видах афазии пациенты могут выполнять команды и давать ответы на вопросы кивками головы или движениями рук, таким образом, они могут выполнять тесты на внимательность. Психиатрические расстройства, такие как депрессия или кататония, являются факторами, которые могут имитировать некоторые симптомы гипоактивного делирия в их наиболее тяжелых формах. В целом остается неясным, какие пропорции гипоактивного или гиперактивного делирия существуют среди больных с нейрокритическими состояниями [22]. Наиболее частыми факторами риска, связанными с развитием делирия после инсульта, были: возраст старше 64 лет; внутрижелудочковое кровоизлияние; интубация; наличие когнитивной дисфункции, афазии или неглекта (синдром игнорирования) и острое повреждение почек [23].
Данные исследований показывают, что фармакологические вмешательства, такие как прием антипсихотических препаратов, часто используются для лечения симптомов делирия в клинической практике. Рекомендации руководства NICE 2010 г. включают устранение любых потенциальных медицинских или лекарственных триггеров, которые могут способствовать развитию делирия. Если симптомы делирия сохраняются и причиняют беспокойство или опасны, может быть назначен антипсихотический препарат (нейролептик) на короткое время (< 1 недели) в самой низкой эффективной дозе. Антипсихотические препараты, также известные как транквилизаторы, в основном используются для лечения психозов (например, галлюцинаций). Существует два типа нейролептиков: нейролептики первого поколения, или типичные антипсихотики (например, галоперидол), и антипсихотики второго поколения, или атипичные антипсихотики (например, кветиапин). Обе группы нейролептиков блокируют дофаминовые рецепторы мозга, но атипичные нейролептики также действуют на серотониновые рецепторы. Также отмечается, что атипичные нейролептики эффективны для лечения как положительных (например, галлюцинаций), так и отрицательных (например, эмоциональной отстраненности) симптомов психоза. Обнаружено, что антипсихотические препараты не уменьшают тяжесть делирия, не устраняют симптомы и не снижают смертность. Экстрапирамидные симптомы при приеме нейролептиков встречались не чаще, чем при лечении неантипсихотическими лекарственными препаратами, и не отличались при приеме типичных и атипичных антипсихотиков [24–26]. В недавнем руководстве по ведению пациентов с болью, делирием и нарушением сна в палатах интенсивной терапии систематизированы современные данные по ведению пациентов с делирием и сформулированы рекомендации, однако все они основаны на доказательствах низкого уровня. В руководстве подчеркивается, что основная нефармакологическая стратегия должна быть направлена на устранение модифицируемых факторов делирия, улучшение познавательных функций, оптимизацию сна, подвижности, слуховых и зрительных стимулов у пациентов в критических состояниях. Подчеркивается, что необходимо избегать рутинного назначения галоперидола, атипичных антипсихотиков, а также статинов для лечения делирия. Однако у пациентов с выраженными симптомами тревоги, страха, ажитации и галлюцинациями для их купирования краткосрочное использование галоперидола или атипичных нейролептиков может быть оправданно [27]. Следует отметить, что во всех руководствах рекомендуется избегать длительного назначения нейролептиков, так как это может усугублять некоторые симптомы делирия.
Таким образом, делирий является особой формой изменения сознания, которая значительно осложняет течение ряда острых, в том числе неврологических заболеваний, но транзиторным и потенциально курабельным состоянием. Вначале это состояние обратимо, но, если его вовремя не обнаружить и не устранить метаболическую причину, оно может прогрессировать вплоть до необратимых нарушений функций мозга и смерти.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов и собственной финансовой заинтересованности при подготовке данной статьи.
Список литературы
Список литературы находится в редакции

/10_m.jpg)