Газета «Новости медицины и фармации» №11 (765), 2021
Вернуться к номеру
Аналіз причин ускладненого перебігу COVID-19 у пацієнтів із цукровим діабетом
Авторы: Галушко О.А., Лоскутов О.А., Тріщинська М.А., Кучинська І.А., Болюк М.В.
Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
Вступ
Із грудня 2019 року нова коронавірусна хвороба 2019 (COVID-19) впевнено й агресивно крокує по планеті. 11 березня 2020 року Всесвітня організація охорони здоров’я оголосила коронавірусну хворобу COVID-19 пандемією [1]. Серед основних факторів ризику розвитку і тяжкого перебігу COVID-19 називають похилий вік, артеріальну гіпертензію, цукровий діабет (ЦД), хронічні обструктивні захворювання легень, серцево-судинні та цереброваскулярні захворювання. Проте останнім часом на підставі отриманих епідеміологічних даних ЦД не вважається фактором ризику зараження SARS-CoV-2, але він пов’язаний із більш тяжким перебігом даного захворювання [2]. У чому ж причина ускладненого перебігу COVID-19 у хворих на цукровий діабет? Необхідність дати відповідь на дане питання зумовила проведення цього дослідження.
Мета: встановити причини ускладненого перебігу COVID-19 у хворих на цукровий діабет.
Матеріали та методи
Для вирішення поставленого завдання був проведений пошук публікацій за допомогою пошукових систем PubMed та Google Scholar за ключовими словами: COVID-19, цукровий діабет, гіперглікемія, гіпоглікемія, ускладнення. У результаті проведеного пошуку за вказаними термінами знайдені 1459 публікацій, оприлюднених із початку епідемії в грудні 2019 року по 30 травня 2020 року.
Результати та їх обговорення
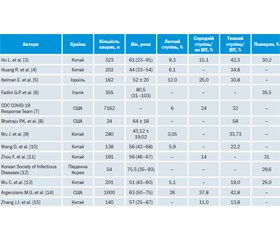
Огляд літературних джерел доцільно розпочати з відповіді на питання, чи дійсно наявність у людини цукрового діабету погіршує перебіг COVID-19. Аналіз поширеності ЦД у хворих на COVID-19 залежно від тяжкості стану пацієнтів наведений у табл. 1.
Аналіз наведених даних дозволяє простежити чітку тенденцію: чим тяжчим був стан хворих, тим частіше в даній когорті зустрічався ЦД. Показові дані наведені в китайському дослідженні С. Wu et al. (2020): у хворих із легким перебігом інфекції ЦД реєструвався в 5,1 % випадків, у хворих, госпіталізованих до відділень інтенсивної терапії (ВІТ), — у 19 % пацієнтів, і серед померлих хворих — у 25,0 % [13]. Подібну картину відображено в американському дослідженні, що провела CDC COVID-19 Response Team. Поширеність ЦД у даному дослідженні становила в легких хворих 6 %, у тяжких, але не госпіталізованих у ВІТ — 24 %, у пацієнтів ВІТ — 32 % [7].
Таким чином, наведені результати підтверджують тезу про те, що наявний ЦД може ускладнювати перебіг COVID-19, погіршувати стан хворих та підвищувати летальність.
Проведений аналіз літературних джерел дозволяє виділити три групи факторів, які, на нашу думку, погіршують перебіг інфекційного захворювання у хворих на ЦД:
1. Особливості власне ЦД, взаємний вплив ЦД на COVID-19 і навпаки.
2. Вплив окремих груп препаратів, що застосовують при лікуванні обох захворювань.
3. Недоліки в організації лікування і догляду за пацієнтами.
Розглянемо всі причини послідовно.
Особливості власне цукрового діабету і взаємний вплив діабету і COVID-19
Сьогодні існує лише обмежена кількість експериментальних досліджень, які безпосередньо стосуються ролі гіперглікемії та ЦД у патогенезі та прогнозі вірусних респіраторних захворювань [16]. Так, у дослідженні M.E. Morra et al. (2018) було показано, що підвищений рівень глюкози в крові може безпосередньо збільшувати концентрацію глюкози в секретах слизової оболонки дихальних шляхів [17]. In vitro внаслідок впливу підвищених концентрацій глюкози на епітеліальні клітини легень значно зростає кількість випадків проникнення вірусу та його реплікація, що дозволяє припустити, що гіперглікемія може посилити реплікацію вірусу in vivo. Підвищений рівень глюкози може також приводити до пригнічення противірусної імунної відповіді. Дані результати узгоджуються з дослідженнями пацієнтів, інфікованих високопатогенним пташиним грипом, коли гіперглікемія асоціювалася з летальним наслідком. Гіперглікемія також може впливати на легеневу функцію так, що індукована вірусом грипу дихальна дисфункція посилюється в пацієнтів із ЦД. У тваринних моделях хвороби діабет асоціюється з численними структурними змінами легень, зокрема з посиленою проникністю судинної оболонки та колапсом альвеолярного епітелію [18].
Інша причина, що ускладнює перебіг коронавірусної хвороби, — особливості вегетативної іннервації у хворих на ЦД. Тяжкість COVID-19 при діабеті може бути прихована більш м’якими проявами вірусної інфекції, оскільки пацієнти з ЦД менше відчувають лихоманку, озноб, скутість грудної клітки та задишку [19]. Даний феномен нагадує «мовчазні» симптоми, які спостерігаються при ЦД. Так, порушення вегетативної іннервації серця, що описане як синдром кардіальної гіпестезії, призводить до ураження аферентних вісцеральних волокон, які визначають сприйняття болю при ураженні міокарда. Унаслідок цього у хворих на ЦД часто реєструють «безбольовий» інфаркт міокарда [20]. Те саме може спостерігатися і в пацієнтів із діабетом, коли при діагностованому COVID-19 симптоми недооцінюються пацієнтом, а адекватне лікування не проводиться вчасно і в повному обсязі. Як результат — допомога відтерміновується, розвиваються ускладнення, результати лікування погіршуються.
Наступний механізм, що ускладнює перебіг коронавірусної хвороби, — порушення функції підшлункової залози на фоні інфекції. Вважається, що коронавірус SARS-CoV-2 призводить до тимчасових порушень функції клітин острівців підшлункової залози [21]. Установлено, що коронавіруси прикріпляються до клітин-хазяїнів за допомогою дипептидилпептидази-4 (DPP-4), що фізіологічно бере участь у модуляції дії інсуліну і як фермент відіграє головну роль у метаболізмі глюкози і відповідає за деградацію інкретинів, таких як глюкагоноподібний пептид 1 (GLP-1) [22, 23]. Гіперглікемія, відзначена в пацієнтів із COVID-19, може бути викликана за допомогою таких (або аналогічних) механізмів [24]. Питання доцільності призначення цукрознижувальних препаратів інгібіторів DPP-4 в умовах пандемії COVID-19 активно обговорювалося в науковій літературі, й на сьогодні немає даних стосовно необхідності відміняти лікування даними препаратами.
Ще один феномен, який спостерігається при розвитку вірусної інфекції у хворих із ЦД, — взаємообтяжувальний вплив захворювань. Так, сама по собі гіперглікемія може негативно впливати на функції легень та імунну відповідь [25], а ЦД є фактором ризику, що впливає на прогресування та прогноз COVID-19. У дослідженні W. Guo et al. (2020) було встановлено, що хворі на COVID-19, які не мали інших супутніх захворювань, крім діабету, мали високий ризик розвитку тяжкої пневмонії, вивільнення пов’язаних із травмами тканин ферментів, надмірних неконтрольованих реакцій на запалення та гіперкоагуляційного стану, пов’язаного з порушенням регуляції обміну глюкози [26]. Крім того, рівень сироваткових біомаркерів запалення, таких як IL-6, С-реактивний білок, сироватковий феритин, протромбіновий індекс, D-димер, був значно вищим (р < 0,01) у хворих на діабет порівняно з хворими без ЦД, що свідчить про розвиток більш широкого комплексу запальних реакцій у пацієнтів із діабетом, а це, зі свого боку, із часом призводить до швидкого погіршення перебігу COVID-19 [26].
Зі свого боку, COVID-19 може погіршити перебіг ЦД у хворих. Як підкреслюють Е. Maddaloni, R. Buzzetti (2020), взаємодія між COVID-19 та діабетом може бути двонаправленою, оскільки SARS-CoV-2 потенційно може погіршити перебіг наявного діабету або навіть схильність до діабету в осіб, які не страждають від ЦД [19].
Так, у тяжкохворих пацієнтів, у тому числі і у хворих на COVID-19, часто реєструються гіперглікемія та інсулінорезистентність. Вони є результатом вивільнення контрінсулярних гормонів, таких як глюкагон, кортизол та адреналін, а також підвищення рівня прозапальних цитокінів, таких як IL-6 та TNF-α, що призводить до «цитокінового шторму» [27]. Їх дія на чутливі до інсуліну тканини призводить до зниження поглинання глюкози в м’язах, посиленого ліполізу та збільшення синтезу глюкози в печінці [28].
COVID-19 також може проявлятись диспептичними симптомами, такими як блювання та діарея, що призводять до зневоднення [29]. Дослідження J. Li et al. (2020) показало, що інфекція SARS-CoV-2 була пов’язана з кетоацидозом у 12 % хворих на діабет [30].
Загальновизнано, що певні вірусні захворювання можуть викликати автоімунний діабет типу 1 у генетично схильних пацієнтів або навіть спричинити бурхливий розвиток діабету від масового колапсу β-клітин [33]. COVID-19 використовує рецептор ангіотензинперетворюючого ферменту типу 2 (АПФ-2) як «шлюз» для вторгнення в клітини-мішені людини [31]. Даний фермент експресується різними тканинами та типами клітин, включаючи і легені, а також з ендокринною частиною підшлункової залози [31]. У дослідженні J.K. Yang et al. (2010) було висловлене припущення, що зараження SARS-CoV, що також використовує рецептор АПФ-2 як рецептор входу, може пошкодити острівці Лангерганса, викликаючи гіперглікемію пд час інфекції [21]. У дослідженні D.J. Drucker (2020) повідомлено про травму підшлункової залози, що характеризувалася підвищенням рівня плазмової амілази та ліпази в 17 % пацієнтів із COVID-19, серед яких 67 % мали помірно підвищений рівень глюкози в плазмі [32].
Вплив окремих груп препаратів, що застосовують при лікуванні цукрового діабету та COVID-19
Інгібітори АПФ
Препарати інгібіторів АПФ на сьогодні є найбільш дискусійною групою лікарських засобів, що часто використовують у пацієнтів з артеріальною гіпертензією та ЦД, у тому числі при розвитку в них коронавірусної хвороби. Хоча добре відомий АПФ-1 сприяє конверсії ангіотензину I (AT I) до АТ II, його гомологічний аналог AПФ-2 є ферментом, пов’язаним із мембраною (карбоксипептидазою), який зазвичай сприяє інактивації AT II і тому фізіологічно протидіє активації ренін-ангіотензин-альдостеронової системи (РААС) [31–33].
АПФ-2 виконує багато фізіологічних ролей, зокрема негативна регуляція РААС та полегшення транспорту амінокислот. Нещодавно AПФ-2 був ідентифікований як рецептор SARS-CoV-2, що забезпечує критичний зв’язок між імунітетом, запаленням та серцево-судинними захворюваннями [34]. АПФ-2 також діє як рецептор, який дозволяє потрапляти коронавірусам (SARS-CoV-2 та SARS-CoV) у клітини людини [35]. SARS-CoV-2, щойно зв’язаний з АПФ-2, активується трансмембранною сериновою протеазою типу 2 (TMPRSS2) для сприяння інвазії та реплікації вірусу всередині клітин-мішеней людини включно з пневмоцитами типу ІІ [35]. З іншого боку, АПФ-2 відіграє вирішальну роль у підтримці гомеостазу глюкози та функції B-клітин [32, 36].
Інгібітори АПФ зазвичай пригнічують AПФ-1, але не AПФ-2 [37]. Проте дослідження показали, що дані ліки посилюють регуляцію рецептора АПФ-2, який вірус SARS-CoV-2 використовує для входу в клітини хазяїна [38]. Зі свого боку, вторгнення SARS-CoV-2 у клітини альвеолярного епітелію людини часто призводить до гострого респіраторного дистрес-синдрому (ГРДС) — клінічного стану з високою смертністю, з яким пов’язують поганий прогноз пацієнтів із COVID-19 [39]. Крім того, ЦД збільшує експресію АПФ-2, як показано в декількох експериментальних моделях [40, 41], й отримане в результаті збільшення вірусного навантаження також може пояснити більш тяжкий перебіг COVID-19 у хворих на діабет [42]. Усе це може ускладнювати перебіг COVID-19 і погіршувати стан хворих, які приймають інгібітори АПФ. У деяких публікаціях пропонується замінити інгібітори АПФ та блокатори рецепторів ангіотензину ІІ у хворих на артеріальну гіпертензію та ЦД на інші групи препаратів, наприклад на блокатори кальцієвих каналів [43].
Проте є й інші твердження. Зокрема, група американських і голландських дослідників під керівництвом A.H.J. Danser et al. (2020) стверджують, що інгібітори АПФ не пригнічують АПФ-2, оскільки АПФ-1 та АПФ-2 є різними ферментами, а отже, інгібітори АПФ не можуть сприяти входженню вірусу в клітину [35]. Крім того, немає точних доказових даних, які підтверджують, що інгібітори АПФ або блокатори рецепторів ангіотензину II типу 1 полегшують проникнення коронавірусу SARS-CoV-2, збільшуючи експресію АПФ-2 [35]. Із цією позицією згодні й деякі інші дослідники. Більше того, невідомо, чи не несуть такого ж ризику альтернативні антигіпертензивні засоби. Ураховуючи недостатність доказової бази, Європейська медична асоціація (EMA) радить не припиняти прийом препаратів групи інгібіторів АПФ в умовах пандемії COVID-19 [44].
Ібупрофен та інші нестероїдні протизапальні засоби
Нестероїдні протизапальні засоби (НПЗП) часто використовують для лікування гіпертермії при вірусних інфекціях. Проте в дослідженні M. Day (2020) було продемонстровано чотири випадки, коли в молодих пацієнтів із COVID-19, які не мали жодних основних проблем зі здоров’ям, розвивалися серйозні симптоми після використання НПЗП на ранній стадії захворювання [45]. Дещо раніше в дослідженні G. Voiriot et al. (2019) були описані випадки складного перебігу з підвищеною частотою емпієми, кавітацією легенів та тривалим перебуванням у ВІТ пацієнтів, у яких НПЗП застосовувались на фоні пневмонії [46]. Однак сьогодні Всесвітня організація охорони здоров’я відзначає поточну відсутність доказів щодо розвитку тяжких побічних явищ та потреби використання додаткової медичної допомоги (госпіталізація, заходи інтенсивної терапії, киснева підтримка) у пацієнтів із COVID-19 внаслідок використання НПЗП [47].
НПЗП, у тому числі ібупрофен, слід з обережністю застосовувати пацієнтам із супутніми захворюваннями шлунково-кишкового тракту та серцево-судинної системи. Протипоказано використання НПЗП у разі ниркової недостатності [48]. В огляді NICE (Великобританія, 2020) зазначено, що наявні дані свідчать про те, що, хоча протизапальна дія НПЗП зменшує гострі симптоми (наприклад, гарячку), дані препарати можуть або не впливати, або погіршувати довгострокові результати лікування, можливо, через маскування симптомів прогресування гострої інфекції дихальних шляхів. Необхідні додаткові докази з рандомізованих клінічних досліджень для підтвердження впливу НПЗП на перебіг COVID-19 [49].
Використання НПЗП для лікування гарячки в пацієнтів із COVID-19 продовжує обговорюватися. Поки не знайдеться більше доказів, кампанія з виживання при сепсисі (2020) пропонує для тяжкохворих дорослих із COVID-19 для лікування гарячки використовувати ацетамінофен (парацетамол) [50]. Крім того, слід зауважити, що використання НПЗП у хворих із діабетичною нефропатією протипоказане через можливість розвитку гострої ниркової недостатності. Тому вважаємо доцільним у хворих на ЦД та COVID-19 для лікування больового синдрому чи гіпертермії відмовитися від ібупрофену та інших НПЗП і використовувати парацетамол.
Глюкокортикостероїди
У тяжкохворих пацієнтів протоколи лікування часто включають широке використання глюкокортикостероїдів (ГКС), що значно погіршує пов’язану з інфекцією гіперглікемію. У звіті італійського Вищого інституту здоров’я (ISS — Istituto Superiore di Sanità) зазначено, що ГКС застосовувались у 34 % пацієнтів ВІТ [51]. У той же час терапія з використанням ГКС підвищує рівень глюкози у 80 % пацієнтів із діабетом та в багатьох пацієнтів без діабету, що може збільшити ризик смертності від коронавірусної інфекції [52]. Слід пам’ятати, що ГКС не показані всім тяжкохворим на COVID-19. Кампанія з виживання при сепсисі (Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID19)) рекомендує використовувати ГКС лише для пацієнтів, яким проводиться штучна вентиляція легень, та й то тільки у хворих із тяжким ГРДС, а також у хворих із рефрактерним шоком і не використовувати у хворих без ГРДС та при інших рутинних випадках [50]. Якщо хворому необхідно призначити кортикостероїди, то рівень глюкози слід ретельно контролювати для підтримання еуглікемії, що сприяє оптимальним дихальній та імунологічній функціям [50].
Гідроксихлорохін
Гідроксихлорохін та хлорохін використовуються для профілактики та лікування малярії і деяких автоімунних станів, таких як ревматоїдний артрит та системний червоний вовчак. Розглядаються дослідниками як один із потенційних союзників для боротьби проти COVID-19 [48]. Проте лікарські засоби гідроксихлорохін та хлорохін можуть мати серйозні побічні ефекти. Так, при застосуванні гідроксихлорохіну повідомлялося про випадки кардіоміопатії, що призводила до розвитку серцевої недостатності, у деяких випадках із летальним наслідком [53]. Відзначається також, що при застосуванні гідроксихлорохіну часто спостерігається подовження інтервалу QT, що може призводити до небезпечних аритмій [54]. Цікаво, що в згаданому дослідженні в десяти пацієнтів введення гідроксихлорохіну було припинено достроково через побічні явища: непереборну нудоту, гіпоглікемію та один випадок шлуночкової аритмії (torsades de pointes) [54]. Крім того, у хворих на ЦД на фоні лікування гідроксихлорохіном може виникати тяжка гіпоглікемія [55].
Варто пам’ятати, що молекула гідроксихлорохіну має гіпоглікемічну дію і використовується в Індії як альтернативний засіб, що знижує рівень глюкози [56]. Механізми, що лежать в основі даного гіпоглікемічного ефекту, недостатньо вивчені; серія складних молекулярних ефектів може покращити як чутливість до інсуліну, так і секрецію інсуліну [29]. Дозування препаратів, що знижують глюкозу, слід відповідно коригувати.
Проте є й окремі позитивні відгуки. Зокрема, A.K. Singh et al. (2020) вважають, що, ураховуючи мінімальний ризик при застосуванні, багаторічний досвід використання при інших захворюваннях, економічну ефективність та доступність, гідроксихлорохін та хлорохін можуть бути розглянуті для клінічного використання як експериментальні препарати, навіть у хворих із супутнім ЦД [56]. Ураховуючи дані літератури, вважаємо, що гідроксихлорохін може застосовуватися у хворих на ЦД та COVID-19 лише у виняткових випадках у рамках клінічних досліджень і, звичайно, тільки в стаціонарі, в умовах ретельного моніторингу, і не можуть використовуватися хворими для самолікування.
Азитроміцин
Азитроміцин — антибіотик широкого спектра дії з групи макролідів, що має активність проти бактерій та інших мікроорганізмів. Щодо застосування азитроміцину разом із гідроксихлорохіном при COVID-19 сьогодні існує недостатньо доказів або докази суперечливі [48]. У дослідженні P. Gautret et al. (2020) отримано позитивний результат у 6 пацієнтів з ураженням нижніх дихальних шляхів при COVID-19, пролікованих гідроксихлорохіном разом з азитроміцином [57]. У дослідженні E.S. Rosenberg et al. (2020) серед 1438 госпіталізованих пацієнтів із діагнозом COVID-19 у Нью-Йорку лікування азитроміцином було проведено у 211 хворих, серед яких було 58 (27,5 %) осіб із ЦД. При цьому зазначене лікування не призвело до змін у рівні летальності [58]. Якщо азитроміцин передбачається використовувати для лікування COVID-19, слід переглянути призначення та відмінити непотрібні ліки, які можуть подовжити інтервал QT; пацієнтам із відомим спадковим синдромом тривалого QT або наявною в анамнезі поліморфною шлуночковою тахікардією типу «пірует» (torsade de pointes), індукованою лікарськими засобами, рішення щодо використання даних препаратів слід приймати лише після консультації з кардіологом [48].
Метформін
Метформін був затверджений FDA в 1995 році як пероральний гіпоглікемічний засіб, що став одним із найбільш часто призначених антидіабетичних препаратів у всьому світі [59]. Останнім часом було висловлено припущення, що метформін може пригнічувати активність вірусів через підвищення чутливості до інсуліну [60]. У США з 2002 по 2012 рік було проведено ретроспективне когортне дослідження для літніх пацієнтів віком понад 65 років та з ЦД в анамнезі, які були госпіталізовані з пневмонією. Цікаво, що попереднє введення метформіну в даних пацієнтів було пов’язане зі значно меншою смертністю [61]. На думку окремих авторів, доцільно доповнити показання для використання в інструкції метформіну: як засіб допоміжної терапії для зменшення ризику смертності від COVID-19 у пацієнтів літнього віку, з ожирінням та діабетом через зменшення ваги та зниження ризику пневмонії [62]. Крім того, є повідомлення про ефективність метформіну при супутніх захворюваннях печінки та функціональних змінах печінки на фоні інфекції SARS-CoV-2 [63]. Проте більшість дослідників з обережністю ставляться до можливості застосування метформіну при коронавірусній хворобі. Так, L. Orioli et al. (2020) вважають, що пацієнтам із тяжкими формами COVID-19 слід відмінити метформін через ризик виникнення лактатацидозу [29].
Таким чином, при тяжких формах COVID-19 слід відмінити метформін та інгібітори SGLT-2, враховуючи їх власний ризик лактатацидозу та кетоацидозу відповідно. А в разі глибокої декомпенсації ЦД і при порушеннях свідомості обов’язковим є перехід на інсулін як оптимальний спосіб корекції порушень вуглеводного обміну.
Недоліки в організації лікування і догляду за хворими
Уже на амбулаторному етапі виявляються перші недоліки в лікуванні хворих на COVID-19 при супутньому ЦД. Відомо, що більшість пацієнтів із діабетом скасовують звичайні візити до ендокринолога. У багатьох хворих розвивається надмірний стрес, пов’язаний із соціальною ізоляцією та недостатністю фізичних навантажень, що сприяє погіршенню глікемічного контролю та ще більше підвищує ризик розвитку COVID-19 у даної вразливої категорії пацієнтів [16]. Неправильна організація амбулаторного прийому, недостатнє і незбалансоване харчування, відсутність забезпеченості лікарськими засобами і діагностичним приладдям, недостатня комунікація з ендокринологом і сімейним лікарем, нехтування правилами особистої гігієни і соціальної дистанції — ось далеко не всі проблеми в організації лікування і догляду за хворими в умовах пандемії COVID-19.
На стаціонарному етапі лікування виникає не менше проблем в організації ведення хворих на ЦД та COVID-19. Так, експериментальні дані підтверджують важливу тезу про те, що контроль глікемії може сприятливо впливати на клінічні результати в пацієнтів із супутнім діабетом та вірусними респіраторними захворюваннями, такими як COVID-19 [16]. У той же час, як показав досвід в епіцентрах спалаху інфекції, більшість фахівців із невідкладних станів не є професійними ендокринологами, і в них можуть бути відсутні стурбованість рівнем глюкози в крові пацієнта та недостатній клінічний досвід терапії діабету, що може призвести до різких коливань глікемії і розвитку гострих порушень вуглеводного обміну у хворих на діабет [64]. Тому дуже важливо підвищити обізнаність серед лікарів, які безпосередньо займаються лікуванням хворих на COVID-19, про важливість контролю глікемії в даних пацієнтів і налагодити своєчасний стандартизований менеджмент глікемії у хворих на діабет із COVID-19.
У дослідженні J. Zhou і J. Tan (2020) звертають увагу на те, що під час перебування в стаціонарі з карантином неможливо здійснювати фізичні вправи через обмежений простір у приміщенні та знижену респіраторну функцію хворого. Крім того, дієта для хворих на COVID-19 або персоналізована дієта часто недоступні [65], у той час як у дослідженні X. Li et al. (2020) показано, що недостатнє і неправильне харчування часто спостерігається в пацієнтів із тяжким перебігом захворювання [66].
У зв’язку із зазначеними факторами оптимальне лікування хворих на COVID-19 при супутньому ЦД повинно включати багатодисциплінарний командний підхід із залученням фахівців із невідкладної медицини, ендокринології, інфекційних захворювань, респіраторної підтримки, дієтології та реабілітації.
Проведений аналіз дозволяє стверджувати: головним фактором, що має вирішальне значення у веденні хворих на COVID-19 із супутнім ЦД, є нормалізація рівня глікемії і вуглеводного балансу, яку потрібно досягати усіма можливими засобами.
Висновки
1. Наявний ЦД може ускладнювати перебіг COVID-19, погіршувати стан хворих та підвищувати летальність.
2. Аналіз літературних джерел дозволяє виділити три групи причин, які погіршують перебіг інфекційного захворювання у хворих на ЦД:
1) особливості власне ЦД і взаємовплив діабету і COVID-19;
2) вплив окремих груп препаратів, що застосовують при лікуванні обох захворювань;
3) недоліки в організації лікування і догляду за хворими.
3. Головним фактором, що має вирішальне значення у веденні хворих на COVID-19 при супутньому ЦД, є нормалізація рівня глікемії і вуглеводного балансу, яку потрібно досягати усіма можливими засобами.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Список литературы
Список літератури знаходиться в редакції

/12_u.jpg)