Газета «Новости медицины и фармации» №6 (724), 2020
Вернуться к номеру
COVID-19 и сопутствующие заболевания
Авторы: Мельник А.А., к.б.н.
Специализированный медицинский центр «Оптима-фарм», г. Киев, Украина
Рубрики: Аллергология
Разделы: Справочник специалиста
Версия для печати
Появление нового коронавируса, известного как SARS-CoV-2, создало беспрецедентную проблему для мирового медицинского сообщества. Высокая инфекционность, способность передаваться даже во время бессимтомной фазы и относительно низкая вирулентность привели к быстрому распространению вируса во всех географических регионах мира, что вызвало пандемию. Первый случай этого заболевания, известный как коронавирусная болезнь 2019 года, или COVID-19, был зафиксирован 8 декабря 2019 г. в провинции Хубэй в Китае [1]. С тех пор в течение короткого времени, всего лишь за 5 месяцев, инфекция распространилась по всему миру. К середине мая 2020 г. уже зафиксировано 4,5 миллиона подтвержденных случаев заражения и более 300 тысяч летальных исходов.
Распространение коронавирусной инфекции представляет особую опасность в отношении лиц, имеющих сопутствующие заболевания, особенно в случаях тяжелого течения, когда отмечается высокий риск неблагоприятных исходов. Политропность вируса SARS-CoV-2 определяет полиморфность клинических проявлений инфекции. Рецепторы ангиотензинпре-вращающего фермента-2 (АПФ-2), к которым прикрепляется вирус, представлены на клетках дыхательного тракта, сердца, почек, центральной нервной системы, пищевода, мочевого пузыря. Поэтому поражаться могут любые органы и системы человека. В группе риска находятся категории пациентов, имеющие следующие заболевания:
— сердечно-сосудистые заболевания (ишемическая болезнь сердца, аритмия и др.);
— сахарный диабет (повышенный уровень глюкозы в крови);
— гипертония (повышенное давление);
— хронические респираторные заболевания (хронический бронхит, хроническая обструктивная болезнь легких);
— рак;
— цереброваскулярные заболевания;
— иммунодефицит;
— аутоиммунные и ревматические заболевания;
— цереброваскулярные заболевания;
— болезнь почек;
— болезнь печени;
— метаболический синдром;
— ожирение;
— тромбофилия, антифосфолипидный синдром.
I. Поражение сердечно-сосудистой системы и COVID-19
Если сердечно-сосудистое заболевание (ССЗ) у пациента является основным среди других сопутствующих заболеваний, то при инфицировании вирусом SARS-CoV-2 оно представляет самый высокий уровень смертности.
Общими механизмами, ответственными за сердечно-сосудистые осложнения при COVID-19, являются следующие [2, 3].
1. Прямое повреждение миокарда
Вирус SARS-Co-V2 попадает в организм человека и связывается с АПФ-2 на мембране клеток, который высоко экспрессируется в сердце и легких. АПФ-2 играет важную роль в нейрогуморальной регуляции сердечно-сосудистой системы в норме и при патологии. Связывание SARS-CoV-2 с АПФ-2 приводит к изменению сигнальных путей АПФ-2, что способствует повреждению миокарда.
2. Системное воспаление
Характеризуется острым системным воспалительным ответом и цитокиновым штормом. Это может вызвать повреждение некоторых органов и полиорганную недосточность. В некоторых исследованиях были показаны высокие уровни провоспалительных цитокинов у пациентов с тяжелой/критической COVID-19 [4, 5].
3. Сдвиг в соотношении метаболического спроса/предложения кислорода миокарду
Увеличение кардиометаболического спроса, связанного с системной инфекцией в сочетании с гипоксией, вызванной острым респираторным заболеванием, может нарушить соотношение спроса и предложения кислорода при остром повреждении миокарда.
4. Разрыв бляшки и коронарный тромбоз
Системное воспаление увеличивает напряжение сдвига из-за повышения коронарного потока крови при разрыве бляшки, что приводит к острому повреждению миокарда. Протромботическое состояние, созданное системным воспалением, еще больше увеличивает риск (например, тромбоз
стента).
5. Побочные эффекты различных методов лечения
Некоторые противовирусные препараты, кортикостероиды и другие лекарственные средства, применяемые для лечения COVID-19, могут оказывать вредное воздействие на сердечно-сосудистую систему.
6. Электролитный дисбаланс
Электролитный дисбаланс может возникнуть при любом критическом состоянии, особенно у пациентов с заболеванием сердца. Из-за воздействия SARS-CoV-2 на ренин-ангиотензин-альдестероновую систему (РААС) может развиться гипокалиемия [6].
7. Микроваскулярное повреждение
Вследствие прямого повреждающего действия SARS-CoV-2 на эндотелий сосудов возможно микроваскулярное повреждение, повышенная сосудистая проницаемость.
Сердечно-сосудистые осложнения при COVID-19 представлены в табл. 1.
Контроль уровня биомаркеров
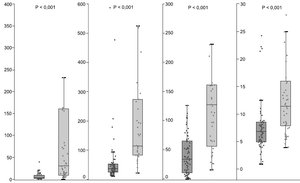
Для стратификации риска и определения тактики ведения пациентов могут быть использованы маркеры тяжести COVID-19, такие как тропонин, миоглобин, D-димер, высокочувствительный С-реактивный белок, интерлейкин-6, фибриноген, глюкоза [10] (рис. 1).
Рекомендации по определению тропонина
Для выявления пациентов групп риска необходимо проводить регулярный контроль уровня тропонина:
— ежедневно в отделении реанимации и интенсивной терапии;
— через день у стационарных пациентов.
Изолированного повышения тропонина недостаточно для диагностики инфаркта миокарда. Частота острого инфаркта миокарда при COVID-19 низкая.
Таким образом, сочетание COVID-19 с сердечно-сосудистыми заболеваниями создает дополнительные сложности в диагностике, определении приоритетной тактики, изменении порядков маршрутизации пациентов с неотложными состояниями, выборе терапии.
II. Сахарный диабет и COVID-19
Сахарный диабет (СД) является фактором риска смертности от инфекции COVID-19. В многочисленных исследованиях было показано, что смертность среди лиц с диабетом примерно в три раза выше по сравнению с общей смертностью от COVID-19 [11–18].
Потенциальные механизмы, которые могут увеличить восприимчивость к COVID-19 у пациентов с СД, включают: высокую аффинность клеточного связывания и эффективное проникновение вируса, снижение вирусного клиренса, снижение функции Т-клеток, повышенную восприимчивость к гипервоспалению и цитокиновому шторму, наличие сердечно-сосудистых заболеваний (рис. 2).
Повышенная экспрессия АПФ-2 в альвеолярных клетках, миокарде, почках и поджелудочной железе приводит к усилению связывания SARS-CoV-2 с клеткой [19]. В рандомизированном исследовании Rao et al. [20] изучались заболевания, которые могли быть связаны с экспрессией АПФ-2 в легких. Интересным оказалось то, что СД имеет причинную связь с этим процессом. Циркулирующие уровни фурина, клеточной протеазы, участвующей в обеспечении проникновения вируса в клетку путем расщепления домена S1 и S2 белка S, повышены у пациентов с СД [21]. Эти исследования подтверждают гипотезу о том, что пациенты с СД более восприимчивы к инфекции SARS-CoV-2. Недавнее исследование показало, что клиренс SARS-CoV-2 у пациентов с СД был отсрочен [22].
Введение инсулина приводит к снижению экспрессии АПФ-2 [23], в то время как гипогликемические агенты, такие как глюкагоноподобный пептид 1, агонисты (лираглутид), тиазолидиндионы, гипотензивные средства (ингибиторы АПФ) и статины, активируют АПФ-2.
У пациентов с СД нарушен иммунный ответ на инфекцию как в отношении профиля цитокинов, так и в изменении иммунного ответа, включая активацию Т-клеток и макрофагов. При диабетической патологии SARS-CoV-2 представляет серьезную угрозу из-за затяжного течения пневмонии, высокой вероятности дыхательной недостаточности. При этом пациентам важно контролировать уровень глюкозы в крови и корректировать гликемеческий индекс. Необходимо отметить, что наибольшее количество смертей от COVID-19 в Украине зафиксировано у тех, кто имел сахарный диабет.
III. Артериальная гипертензия и COVID-19
Одной из часто сопутствующих патологий, которая приводит к летальному исходу у больных COVID-19, является гипертония, которая считается одной из основных причин смертности в мире.
Ренин-ангиотезин-альдостероновая система может быть связана с патогенезом вируса SARS-CoV-2. РААС представляет собой элегантный каскад вазоактивных пептидов, играющих ключевую роль в физиологии человека. Ренин, или ангиотензиногеназа, — это протеолитический фермент, секретируемый в юкстагломерулярном аппарате почек из предшественника-проренина. При нарушении артериального давления происходит снижение почечного кровотока, что способствует выделению ренина, который воздействует на ангиотензиноген. Ренин запускает преобразование ангиотензиногена в неактивный ангиотензин I (АТ I). Далее ангиотензинпревращающий фермент (АПФ-1) преобразовывает АТ I в активный сосудосуживающий ангиотензин II (АТ II), который оказывает свое воздействие через связь с двумя подтипами рецепторов — АТ1 и АТ2 [24]. При связывании ангиотензина II c рецепторами АТ1 происходит высвобождение альдостерона из надпочечников, секреция вазопрессина из гипоталамуса и вазоконстрикция. Вазопрессин и альдо-стерон приводят к увеличению реабсорбции натрия и свободной воды в почках, что повышает артериальное давление. Ангиотензин II метаболизируется в Ang-(1–7) с помощью ангиотензинпревращающего фермента-2 (АПФ-2). Для проникновения в клетку-хозяина вирус SARS-CoV-2 должен связаться с рецептором АПФ-2, так же как и антигиотензин II, что приводит к конкурентному ингибированию рецептора АПФ-2. Кроме того, связывание ангиотензина II c рецепторами АТ1 приводит к интернализации, подавлению и расщеплению АПФ-2. Все эти метаболические пути могут помешать SARS-CoV-2 проникнуть в клетку [25] (рис. 3).
Артериальная гипертензия может способствовать развитию сердечной недостаточности, инфаркта миокарда, мерцательной аритмии, инсульта и усугубить течение пневмонии в виде осложнений при инфицировании SARS-CoV-2.
В связи с тем, что АПФ-2 является функциональным рецептором для SARS-CoV-2, было высказано предположение, что это может объяснять высокий риск летального исхода при COVID-19 у пациентов с артериальной гипертензией, получающих препараты из группы ингибиторов АПФ или блокаторов рецепторов к ангиотензину. Эти опасения носили гипотетический характер и не получили практического подтверждения. Более того, имеются косвенные данные о возможном протективном действии этих препаратов при инфекции COVID-19. Экспертами Европейского общества кардиологов опубликовано заявление о том, что данных о неблагоприятных эффектах этих препаратов на течение COVID-19 нет и что их прием настоятельно рекомендуется продолжать [26].
IV. Онкологические заболевания и COVID-19
Больные раком более восприимчивы к COVID-19 из-за системного иммуносупрессивного состояния, которое вызвано химиотерапией, таргетной и иммунотерапией, используемой для лечения злокачественного заболевания [27, 28]. Потенциальными факторами риска являются лица старшего возраста и имеющие сопутствующие заболевания. Это позволит определить пациентов с плохим прогнозом на ранней стадии. Кроме того, необходимо учитывать неблагоприятные исходы COVID-19 при лечении онкологических пациентов после хирургии, системной химио- или лучевой терапии. В табл. 2 представлены рекомендации по принятию решения о лечении рака при заболевании COVID-19 [29].
Окончательное принятие решения должно быть основано на экспертном онкологическом заключении с учетом состояния отдельных пациентов и локальной системы здравоохранения.
V. Хронические респираторные заболевания и COVID-19
Поскольку вирус SARS-CoV-2 поражает легкие, пациенты с хроническими заболеваниями легких, такими как хроническая обструктивная болезнь легких (ХОБЛ), астма и легочный фиброз, более восприимчивы к инфекции COVID-19.
Можно выделить три стадии заболевания COVID-19, которые соответствуют различным клиническим стадиям:
1) бессимптомное состояние (первые 1–2 дня инфекции);
2) вирус распространяется и мигрирует вниз по дыхательным путям, актвируется врожденный иммунный ответ (следующие несколько дней);
3) гипоксия, инфильтраты «матового стекла» и прогрессирование до острого респираторного дистресс-синдрома (ОРДС).
К сожалению, у 20 % пациентов, инфицированных вирусом SARS-Co-V2, заболевание будет прогрессировать до 3-й стадии. Показатели смертности при этом составляют около 2 %, что заметно изменяется с возрастом. Вирус преимущественно инфицирует альвеолярные клетки типа II по сравнению с клетками типа I [30, 31]. Это происходит в периферических и субплевральных отделах легких [32, 33]. Размножение SARS-CoV-2 происходит в клетках типа II с продуцированием большого количества вирусных частиц, в результате чего клетки подвергаются апоптозу и погибают [34]. Конечным результатом является самореплицирующийся вирусный токсин в виде высвобожденных вирусных частиц, которые заражают соседние клетки типа II. Легкие теряют большое количество клеток типа II, и запускается вторичный путь эпителиальной регенерации. Патологическим результатом COVID-19 является диффузное альвеолярное повреждение через богатые фибрином гиалиновые мембраны и некоторых многоядерных гигантских клеток [35]. Ненормальное заживление раны может привести к серьезным рубцам и фиброзу. Для восстановления потребуется врожденный и приобретенный иммунный ответ и регенерация эпителия. Лица старшего возраста особенно подвержены риску из-за ослабленного иммунного ответа и снижения способности восстановливать поврежденный эпителий. Они также имеют сниженный мукоцилиарный клиренс, что может позволить вирусу быстрее распространяться в газообменных отделах легкого [36].
Фенотипы пневмонии при COVID-19
На основании наблюдений за больными COVID-19, находящимися в отделении интенсивной терапии, обнаружены некоторые различия в проявлении заболевания, которые зависят от взаимодействия трех факторов [37]:
1) тяжесть инфекции, ответ организма, физиологический резерв и коморбидность;
2) ответная дыхательная реакция на гипоксемию;
3) время, прошедшее между началом заболевания и наблюдением в стационаре.
Взаимодействие этих факторов приводит к развитию спектра заболеваний, связанных по времени двух фенотипов: тип L и тип Н.
1. COVID-19 и пневмония, тип L:
— низкая эластичность, количество газа в легких практически нормальное;
— низкое соотношение вентиляции и перфузии;
— низкий вес легких;
— низкая рекрутируемость легких.
Можно избежать искусственной вентиляции легких с соотвествующей терапией кислородом. Пациент может реагировать на легочные вазодилататоры (например, оксид азота).
2. COVID-19 и пневмония, тип Н:
— высокая эластичность;
— высокий шунт справа налево;
— большой вес легких;
— высокая рекрутируемость легких.
Типичен для поздней стадии болезни и классического ОРДС, включая пациентов с длительной неинвазивной вентиляцией (повреждение легких от баротравмы) и сопутствующими заболеваниями. Применяется обычная терапия при ОРДС, включая открытый доступ к легким.
Для идентификации пациентов с пневмонией типов L и H применяют компьютерную томографию. Понимание патофизиологии данного процесса имеет решающее значение для надлежащего лечения.
VI. COVID-19 и печень
Впервые сообщение о нарушении функционирования ферментов печени у пациентов с COVID-19 отмечено в работе Chen et al. [38]. Из 99 зарегистрированных случаев с COVID-19 43 % пациентов имели повышенные уровни аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и лактатдегидрогеназы. У большинства из них было небольшое повышение аминотрансфераз, и только в одном случае были зарегистрированы высокие уровни: АЛТ — 7590 Ед/л и АСТ — 1445 Ед/л. Не было отмечено ни одного случая с внутрипеченочным холестазом или печеночной недосточностью. В последнее время появляется все больше данных о связи нарушения биохимии печени с тяжестью COVID-19. Отмечено, что уровни трансаминаз и билирубина в тяжелой и критической стадии были значительно выше, чем в легкой и тяжелой стадии заболевания [39–41].
Пока не ясно, может ли повреждение печени напрямую быть вызвано самим коронавирусом. В физиологических условиях печень является важным органом, который встречает и фильтрует большое количество инородного материала, а затем поддерживает иммунную толерантность через ось «кишечник — печень». Однако иммунная толерантность нарушается при психологическом стрессовом состоянии у пациентов с тяжелой формой COVID-19. Гиперактивированные иммунные ответы и системное воспаление при цитокиновом шторме поражают многие органы, включая кишечник и печень. У пациентов с тяжелой формой значительно повышены уровни Th17 и CD8 T-клеток, интерлейкин-2, интерлейкин-6, фактор некроза опухоли альфа, гранулоцит-стимулирующий фактор, интерферон-индуцируемый протеин-10, моноцитарный хемотаксический протеин-1, макрофагальный воспалительный протеин-1-альфа [42, 43]. Стресс-индуцированное повреждение печени может быть связано с гипоксией-реоксигенацией, чрезмерной активацией клеток Купфера и окислительным стрессом, кишечной эндотоксемией, активацией симпатической нервной и адренокортикальной систем у пациентов с COVID-19. Сепсис не является редкостью при тяжелой и критической форме COVID-19, особенно у пациентов с дисбалансом микрофлоры кишечника и циррозом печени [44]. Патофизиология, связанная с сепсисом при повреждении печени, включает гипоксическое повреждение печени из-за ишемии и шока, холестаза из-за изменения обмена желчи, гепатоцеллюлярной травмы из-за лекарственной токсичности или воспаления [45]. Ишемическое/гипоксическое повреждение печени связано с метаболическим ацидозом, перегрузкой кальцием и изменением проницаемости мембран митохондрий, что проявляется повышением аминотрансфераз в сыворотке [46]. Умеренный микрососудистый стеатоз указывает на возможные иные причины повреждения печени.
В клинической практике большое количество пациентов используют жаропонижающие препараты, содержащие парацетамол, который приводит к повреждению печени. Кроме того, пациенты с COVID-19 применяют одновременно несколько противовирусных препаратов, например осельтамивир, арбидол и лопинавир/ритонавир [47, 48]. Таким образом, если повышение ферментов возникло после использования лекарственного препарата, это должно быть подтверждено или исключено, учитывая при этом большое распространение хронических заболеваний печени, неалкогольное ожирение печени и др., которые также могут быть одной из альтернативных причин повреждения печени у пациентов с COVID-19. Поэтому в данном контексте вирус SARS-CoV-2 может рассматриваться как так называемый «второй удар».
VII. COVID-19 и почки
Хотя диффузное альвеолярное повреждение и острая дыхательная недостаточность являются основными особенностями COVID-19, тем не менее другие органы также подвергаются воздействию вируса SARS-CoV-2. После инфицирования легких вирус может попасть в кровь и накапливаться в почках, что приведет к повреждению резидентных клеток почки. В большом проспективном когортном исследовании впервые была показана связь между поражением почек и плохим исходом у пациентов с COVID-19 [49]. Более 40 % пациентов имели нарушения функции почек, а у 13 % отмечены повышенные уровни креатинина и азота мочевины крови. Эти показатели могут быть связаны с плохим прогнозом при COVID-19. Пациенты с повышенным уровнем креатинина в сыворотке более склонны к развитию острого повреждения почек (ОПП).
Поражение почек у пациентов с COVID-19 имеет многофакторный характер. Известно, что SARS-CoV-2 использует АПФ-2 в качестве рецептора для проникновения в клетку. Последние данные РНК-секвенирования показали, что экспрессия АПФ-2 в почках была почти в 100 раз выше, чем в легких [50]. Следовательно, во-первых, заболевание почек может быть вызвано попаданием коронавируса в почки через АПФ-2 (зависимый путь) и оказывать прямое цитопатическое действие на ткани почек. Во-вторых, влияние вирус-индуцированного специфического иммунологического эффекта (специфические Т-клетки или антитело) может привести к повреждению почек. В третьих, вирус-индуцированные цитокины или посредники могут косвенно оказывать влияние на почечную ткань при гипоксии, шоке и рабдомиолизе. Врачи-клиницисты должны обладать информацией о заболевании почек у госпитализированных пациентов с COVID-19, так как ранняя диагностика и эффективное вмешательство могут помочь снизить смертность пациентов с COVID-19.
Пациенты на гемодиализе
Хотя имеющиеся эпидемиологические данные подтвердили, что ОПП является одним из основных факторов риска COVID-19, необходимо также оценить влияние таких почечных состояний, как терминальная стадия почечной недостаточности и трансплантация почки. Анализ образцов периферической крови пациентов с SARS-CoV-2, находящихся на гемодиализе, показал уменьшение количества Т- и NK-клеток, а также снижение уровней воспалительных цитокинов [51]. Это исследование показывает, что пациенты с COVID-19 на гемодиализе могут иметь легкую форму заболевания, которая не перейдет в пневмонию из-за снижения функции иммунной системы. Тем не менее предполагается, что для этих пациентов необходимо применение дополнительных профилактических мер [52].
VIII. Нарушение системы гемостаза и COVID-19
Инфекция, вызванная вирусными, бактериальными или грибковыми патогенами, вызывает комплексное системное воспаление. При заболевании COVID-19 происходит повреждение сосудистого эндотелия, активация тромбоцитов и лейкоцитов, что, в свою очередь, ведет к нарушению регуляции образования тромбина как системно, так и локально (например, в легких у больных тяжелой пневмонией). Это приводит к отложению фибрина с последующим повреждением тканей и развитием микроангиопатической патологии.
Активация системы защиты запускает активацию коагуляции, генерацию тромбина и перепроизводство провоспалительных цитокинов [53–55]. Хотя основная функция тромбина заключается в образовании сгустка путем активации тромбоцитов и превращения фибриногена в фибрин, тем не менее тромбин оказывает множественные эффекты на клетки, которые в дальнейшем могут усилить воспаление через протеиназа-активированные рецепторы (PAR), главным образом PAR-1 [56]. Генерация тромбина контролируется отрицательной обратной связью и физиологическими антикоагулянтами, такими как антитромбин III, ингибитор пути тканевого фактора и протеина С. При воспалении все эти три контрольных механизма могут быть повреждены. Результатом этого является снижение концентрации антикоагулянтов из-за сокращения их продуцирования и увеличения потребления. Такой дефект прокоагулянтно-антикоагулянтного баланса приводит к развитию микротромбоза, диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганной недостаточности как свидельству тяжелой формы COVID-19 с повышением концентрации D-димера [57]. Наличие повышенного уровня D-димера у пациентов с COVID-19 свидетельствует о присутствии венозного тромбоэмболизма, нарушении вентиляции-перфузии, распространении легочной эмболии и является одним из предикторов смертности [58]. Известно, что пациенты с сопутствующими заболеваниями и лица старшего возраста имеют повышенные уровни D-димера, поэтому риск смертности у них значительно выше. Так, у умерших пациентов содержание D-димера составляло в среднем 2,12 мкг/мл
(0,77–5,27 мкг/мл), в то время как у выживших средний показатель составлял 0,61 мкг/мл (0,35–1,29 мкг/мл). Кроме того, у пациентов определяли количество тромбоцитов и протромбиновое время (ПВ). Было отмечено, что ПВ у пациентов с летальным исходом было незначительно увеличено и составляло в среднем 15,5 с (14,4–16,3 с) против 13,6 с (13,0–14,3 с) у выживших при норме 11,5–14,5 с. Известно, что тромбоцитопения является плохим прогностическим признаком и приводит к более высокому проценту смертности [59].
Очень важно проводить постоянный мониторинг показателей системы гемостаза, а именно определение уровней D-димера, ПВ, количества тромбоцитов и фибриногена, в отделениях реанимации и интенсивной терапии для выявления ухудшения состояния пациентов (табл. 3).
Исходя из опубликованных данных о септической коагулопатии, проведение мониторинга значений D-димера, ПВ, количества тромбоцитов и содержания фибриногена очень важно для определения показаний к назначению лечения и госпитализации у пациентов с COVID-19 [60, 61]. При ухудшении этих параметров должна проводиться более агрессивная реанимационная помощь.
Международное общество по тромбозу и гемостазу (International Society on Thrombosis and Haemostasis (ISTH)) рекомендует определять уровень D-димера, ПВ и количество тромбоцитов у всех пациентов с инфекцией COVID-19. Снижение количества тромбоцитов обусловлено образованием тромбоцитарных сгустков (тромбов), которое, в свою очередь, приводит к нарушению микроциркуляции в тканях (происходит повышенное потребление тромбоцитов для образования первичного тромбоцитарного тромба). Увеличение уровня D-димера в плазме (продукт распада фибрина) указывает на фибринолитический процесс и является ключевым показателем тромботического состояния. ПВ (отражает время свертывания крови) при ДВС-синдроме увеличено. Снижение количества тромбоцитов и значительное повышение содержания D-димера является прогностически неблагоприятным фактором.
Заключение
Инфекционный процесс может спровоцировать развитие и обострение болезни. Сопутствующие и хронические заболевания, такие как ССЗ, гипертония, диабет, ХОБЛ, заболевания почек, печени и др., являются факторами риска и предикторами неблагоприятного исхода у пациентов с COVID-19. Тщательная оценка и знание этих факторов могут установить риск стратификации и позволят более целенаправленно и конкретно осуществлять подходы к лечению данной категории пациентов.
1. Wu Z., McGoogan J.M. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China: summary of a report of 72314 cases from the Chinese center for disease Control and prevention. J. Am. Med. Assoc. 2020.
2. Xiong T.Y., Redwood S., Prendergast B., Chen M. Coronaviruses and the cardiovascular system: acute and long-term implications. Eur. Heart J. 2020.
3. Li B., Yang J., Zhao F. et al. Prevalence and impact of cardiovascular metabolic diseases on COVID-19 in China. Clin. Res. Cardiol. 2020.
4. Zhou F., Yu T., Du R. et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020.
5. Huang C., Wang Y., Li X. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. 395. 497. e506.
6. Chen D., Li X., Song Q., Hu C., Su F., Dai J. Hypokalemia and clinical implications in patients with coronavirus disease 2019 (COVID-19). МedRxiv. 2020. https://doi.org/10.1101/2020.02.27.20028530
7. Lippi G., Plebani M. Laboratory abnormalities in patients with COVID-2019 infection. Clin. Chem. Lab. Med. 2020.
8. Wang D., Hu B., Hu C. et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. J. Am. Med.
Assoc. 2020.
9. Wu Q., Zhou L., Sun X. et al. Altered lipid metabolism in recovered SARS patients twelve years after infection. Sci Rep. 2017. 7. 9110.
10. Strabelli T.M.V., Uip D.E. COVID-19 and the Heart. Arq. Bras. Cardiol. 2020. [online]. ahead print.
11. Yang X., Yu Y., Xu J. et al. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational study. Lancet Respir. Med. 2020. doi: 10.1016/S2213-2600(20)30079-5.
12. Guan W.J., Ni Z.Y., Hu Y. et al. Clinical characteristics of coronavirus disease 2019 in China. N. Engl. J. Med. 2020. doi: 10.1056/NEJMoa2002032.
13. Zhang J.J., Dong X., Cao Y.Y. et al. Clinical characteristics of 140 patients infected with SARS-CoV-2 in Wuhan, China. Allergy. 2020. doi: 10.1111/all.
14238.
14. Yang J., Zheng Y., Gou X. et al. Prevalence of comorbidities in the novel Wuhan coronavirus (COVID-19) infection: a systematic review and meta-analysis. Int. J. Infect. Dis. 2020. pii: S1201-9712(20)30136-3. doi: 10.1016/j.ijid.2020.03.017.
15. Ruan Q., Yang K., Wang W. et al. Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China. Intensive Care Med. 2020. doi: 10.1007/s00134-020-05991-x.
16. Wu C., Chen X., Cai Y. et al. Risk factors associated with acute respiratory distress syndrome and death in patients with coronavirus disease 2019 pneumonia in Wuhan, China. JAMA Intern. Med. 2020. doi: 10.1001/jamainternmed.2020.0994.
17. Wu Z., McGoogan J.M. Characteristics of and important lessons from the coronavirus disease 2019
(COVID-19) outbreak in China: Summary of a report of 72 314 cases from the Chinese Center for Disease Control and Prevention. JAMA. 2020. doi: 10.1001/jama.2020.2648.
18. Leung C. Clinical features of deaths in the novel coronavirus epidemic in China. Rev. Med. Virol. 2020. e2103. doi: 10.1002/rmv.2103.
19. Lukassen S., Chua R.L., Trefzer T. et al. SARS-CoV-2 receptor ACE2 and TMPRSS2 are predominantly expressed in a transient secretory cell type in subsegmental bronchial branches. bioRxiv. 2020. 2020.2003.2013.991455.
20. Rao S., Lau A., So H.-C. Exploring diseases/traits and blood proteins causally related to expression of ACE2, the putative receptor of 2019-nCov: A Mendelian Randomi-zation analysis. МedRxiv. 2020. 2020.2003.2004.20031237.
21. Fernandez C., Rysa J., Almgren P., Nilsson J. et al. Plasma levels of the proprotein convertase furin and incidence of diabetes and mortality. J. Intern. Med. 2018. 284. 377-387.
22. Chen X., Hu W., Ling J. et al. Hypertension and Diabetes Delay the Viral Clearance in COVID-19 Patients. МedRxiv. 2020. 2020.2003.2022.20040774.
23. Roca-Ho H., Riera M., Palau V., Pascual J., So–ler M.J. Characterization of ACE and ACE2 287 Expression within Different Organs of the NOD Mouse. Int. J. Mol. Sci. 2017. 18.
24. Dihn D.T., Frauman A.G., Jonston C.I., Fabiani M.E. Angiotensin receptors: distribution, signaling and function. Clinical. Sci. 2001. 100. 481-492.
25. Busse et al. COVID-19 and the RAAS — a potential role for angiotensin II? Critical. Care. 2020. 24. 136. https://doi.org/10.1186/s13054-020-02862-1
26. Giovanni de Simone, Chair ESC Council on Hypertension. Position Statement of the ESC Council on Hypertension on ACE-Inhibitors and Angiotensin Receptor Blockers, 13 Mar 2020.
27. Shankar A., Saini D., Roy S. et al. Cancer Care Delivery Challenges Amidst Coronavirus Disease — 19
(COVID-19) Outbreak: Specific Precautions for Cancer Patients and Cancer Care Providers to Prevent Spread. Asian Pacific journal of cancer prevention. April 2020. doi: 10.31557/APJCP.2020.21.3.569.
28. Liang W., Guan W., Chen R. et al. Cancer patients in SARS-CoV-2 infection: a nationwide analysis in China. Lancet Oncol. 2020. 21. 335-337. PMID: 32066541. doi: 10.1016/S1470-2045(20)30096-6.
29. Kutikov A., Weinberg D.S., Edelman E.M. A War on Two Fronts: Cancer Care in the Time of COVID-19. Annals of Internal Medicine©. American College of Physicians. 2020.
30. Mossel E.C., Wang J., Jeffers S. et al. SARS-CoV replicates in primary human alveolar type II cell cultures but not in type I-like cells. Virology. 2008. 372.
127-135.
31. Weinheimer V.K., Becher A., Tonnies M. et al. Influenza A viruses target type II pneumocytes in the human lung. J. Infect. Dis. 2012. 206. 1685-1694.
32. Wu J., Wu X., Zeng W. et al. Chest CT findings in patients with corona virus disease 2019 and its relationship with clinical features. Invest. Radiol. 2020. In press.
33. Zhang S., Li H., Huang S. et al. High-resolution CT features of 17 cases of corona virus disease 2019 in Sichuan province, China. Eur. Respir. J. 2020. In press.
34. Qian Z., Travanty E.A., Oko L. et al. Innate immune response of human alveolar type II cells infected with severe acute respiratory syndrome-coronavirus. Am. J. Respir. Cell Mol. Biol. 2013. 48. 742-748.
35. Xu Z., Shi L., Wang Y. et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir. Med. 2020. 8. 420-422.
36. Ho J.C., Chan K.N., Hu W.H. et al. The effect of aging on nasal mucociliary clearance, beat frequency, and ultrastructure of respiratory cilia. Am. J. Respir. Crit. Care Med. 2001. 163. 983-988.
37. Gattinoni L., Chiumello D., Pietro Caironi P. et al. COVID‑19 pneumonia: different respiratory treatments for different phenotypes? Intensive Care Med. https://doi.org/10.1007/s00134-020-06033-2
38. Chen N., Zhou M., Dong X., Qu J., Gong F., Han Y. et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. The Lancet. 2020. 395. 507-513. doi: 10. 1016/S0140-6736(20)30211-7.
39. Lu H., Ai J., Shen Y., Li Y., Li T., Zhou X. et al. A descriptive study of the impact of diseases control and prevention on the epidemics dynamics and clinical features of SARS-CoV-2 outbreak in Shanghai, lessons learned for metropolis epidemics prevention. МedRxiv. 2020. V. 1. doi: 10.1101/2020.02.19.20025031.
40. Huang C., Wang Y., Li X., Ren L., Zhao J, Hu Y. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. 395. 497-506. doi: 10.1016/S0140-6736(20)30183-5.
41. Wang D., Hu B., Hu C., Zhu F., Liu X., Zhang J. et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020. doi: 10.1001/jama.2020.1585.
42. Wan S., Yi Q., Fan S., Lv J., Zhang X., Guo L. et al. Characteristics of lymphocyte subsets and cytokines in peripheral blood of 123 hospitalized patients with 2019 novel coronavirus pneumonia (NCP). МedRxiv. 2020. V. 1. doi: 10. 1101/2020.02.10.20021832.
43. Diao B., Wang C., Tan Y., Chen X., Liu Y., Ning L. et al. Reduction and functional exhaustion of t cells in patients with coronavirus diszease 2019 (COVID-19). МedRxiv. 2020. V. 1. doi: 10.1101/2020.02.18.20024364.
44. Joung J.Y., Cho J.H., Kim Y.H., Choi S.H., Son C.G. A literature review for the mechanisms of stress-induced liver injury. Brain. Behav. 2019. 9. e01235. doi: 10.1002/brb3.1235.
45. Strnad P., Tacke F., Koch A., Trautwein C. Liver — guardian, modifier and target of sepsis. Nat. Rev. Gastroenterol. Hepatol. 2017. 14. 55-66. doi: 10. 1038/nrgastro.2016.168.
46. Li J., Li R.J., Lv G.Y., Liu H.Q. The mechanisms and strategies to protect from hepatic ischemia-reperfusion injury. Eur. Rev. Med. Pharmacol. Sci. 2015. 19. 2036-2047.
47. Zhang C., Shi L., Wang F.S. Liver injury in
COVID-19: management and challenges. Lancet Gastroenterol. Hepatol. 2020. pii: S2468-1253(20)30057-1. doi: 10.1016/S2468-1253(20)30057-1.
48. Jiang F., Deng L., Zhang L., Cai Y., Cheung C.W., Xia Z. Review of the Clinical Characteristics of Coronavirus Disease 2019 (COVID-19). J. Gen. Intern. Med. 2020. doi: 10.1007/s11606-020-05762-w.
49. Cheng Y., Luo R., Wang K. et al. Kidney disease is associated with in-hospital death of patients with COVID-19. Kidney International. 2020.
50. Li Z., Wu M., Guo J. et al. Caution on kidney dysfunctions of 2019-nCoV patients 2020. MedRxiv preprint. Available at: https://doi.org/10.1101/2020.02. 08.20021212. Accessed March 14, 2020.
51. Ma Y., Diao B., Lv X., Zhu J., Liang W., Liu L. et al. 2019 novel coronavirus disease in hemodialysis (HD) patients: report from one HD center in Wuhan, China. МedRxiv. 2020 Feb. 2020.02.24.20027201.
52. CDC. Coronavirus Disease 2019 (COVID-19) [Internet]. Centers for Disease Control аnd Prevention. 2020 Feb [cited 2020 Mar 12]. Available from: https: //www.cdc.gov/coronavirus/2019-ncov/infection-control/control-recommendations.html
53. Engelmann B., Massberg S. Thrombosis as an intravascular effector of innate immunity. Nat. Rev. Immunol. 2013. 13. 34-45.
54. Delabranche X., Helms J., Meziani F. Immunohaemostasis: a new view on haemostasis during sepsis. Annals of intensive care. 2017. 7. 117.
55. Jackson S.P., Darbousset R., Schoenwaelder S.M. Thromboinflammation: challenges of therapeutically targeting coagulation and other host defense mechanisms. Blood. 2019. 133. 906-18.
56. Jose R.J., Williams A.E., Chambers R.C. Proteinase-activated receptors in fibroproliferative lung disease. Thorax. 2014. 69. 190-92.
57. Tang N., Li D., Wang X., Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J. Thromb. Haemost. 2020. 18. 844-47.
58. Chen J., Wang X., Zhang S. et al. Findings of acute pulmonary embolism in COVID-19 patients. SSRN Electron. J. 2020. published online April 11. doi: 10.2139/ssrn.3548771.
59. Vanderschueren S., De Weerdt A., Malbrain M. et al. Thrombocytopenia and prognosis in intensive care. Crit. Care Med. 2000. 28(6). 1871-6. doi: 10.1097/00003246-200006000-00031.
60. Levi M., Toh C.H., Thachil J., Watson H.G. Guidelines for the diagnosis and management of disseminated intravascular coagulation. British Committee for Standards in Haematology. Br. J. Haematol. 2009. 145(1). 24-33. doi: 10.1111/j.1365-2141.2009.07600.x.
61. Di Nisio M., Baudo F., Cosmi B. et al.; Italian Society for Thrombosis and Haemostasis. Diagnosis and treatment of disseminated intravascular coagulation: Guidelines of the Italian Society for Haemostasis and Thrombosis (SISET). Thromb. Res. 2012. 129(5). e177-84. doi: 10.1016/j.thromres.2011.08.028.

/50-1.jpg)
/52-1.jpg)
/53-1.jpg)
/54-1.jpg)
/57-1.jpg)