Статтю опубліковано на с. 144-146
Вступ
Адекватне періопераційне знеболювання упродовж багатьох років залишається актуальною проблемою сучасної хірургії. Біль не тільки викликає дискомфорт у пацієнта, але й є одним із рушійних факторів післяопераційної стрес-відповіді.
Традиційним для України методом знеболювання після апендектомії є введення метамізолу натрію в поєднанні з димедролом за вимогою пацієнта. На жаль, така методика не забезпечує ані адекватного знеболювання, ані достатнього профілю безпеки. Золотим стандартом із позиції доказової медицини є мультимодальні методики аналгезії, що включають:
— преемптивне призначення субнаркозних доз кетаміну;
— планове використання неспецифічних нестероїдних протизапальних засобів (НПЗЗ) або інгібіторів циклоокигенази (ЦОГ)-2 як базисної аналгезії;
— додаткове знеболювання наркотичними аналгетиками за потреби.
Біль після апендектомії має полімодальну структуру та включає як центральні, так і периферичні механізми. Серед останніх значну роль відіграють запальні зміни з активацією метаболізму простагландинів. Саме тому аналгетики з вираженим протизапальним ефектом займають провідне місце в терапії цього виду болю.
Вважається, що аналгетичний та протизапальний ефекти НПЗЗ визначаються інгібіцією ЦОГ-2, а розвиток побічних реакцій — супресією ізоферментів ЦОГ-1. Однак останнім часом з’явилися дані про участь у розвитку болю та запалення не тільки ЦОГ-2, але й ЦОГ-1 та про відсутність кореляції між здатністю НПЗЗ пригнічувати синтез простагландинів та їх аналгетичною активністю. Таким чином, можна припустити, що в деяких випадках препарати з високою неселективною активністю щодо циклооксигенази можуть здійснювати більш виражений знеболюючий ефект, ніж селективні інгібітори ЦОГ-2.
Для дослідження було обрано декскетопрофен як сучасний неселективний НПЗЗ із високим рівнем профілю «ефективність — безпека» та рофекоксиб як класичний представник інгібіторів ЦОГ-2. Метою дослідження було порівняти аналгетичний потенціал рофекоксибу та декскетопрофену у хворих, які перенесли апендектомію, та дослідити гіпотезу про значну роль ЦОГ-1 у формуванні післяопераційного больового синдрому.
Наскільки нам відомо, досі не проводилися контрольовані дослідження з оцінки ефективності періопераційної аналгезії рофекоксибом та декскетопрофеном у хворих після апендектомії.
Методи дослідження
У дослідженні брали участь 66 пацієнтів віком 18–58 років. Усі пацієнти госпіталізовані до клініки в ургентному порядку, з давністю захворювання від 4 до 36 годин. Хворі були інформовані про мету та методику дослідження, отримано їх добровільну згоду.
Критерії включення: хворі, яким запланована апендектомія через доступ Волковича — Дьяконова.
Критерії виключення:
1) підвищена чутливість до декскетопрофену або рофекоксибу в анамнезі;
2) прийом НПЗЗ протягом тижня перед госпіталізацією;
3) систематичний прийом діуретиків;
4) вік пацієнтів більше ніж 60 років;
5) наявність ішемічної хвороби серця або серцевої недостатності з ФК > II (NYHS) клінічно або в анамнезі;
6) наявність ознак ішемії міокарда на ЕКГ;
7) апендектомія шляхом серединної лапаротомії або через параректальний доступ.
Пацієнти були рандомізовані методом послідовних номерів. Групи були репрезентативні за віковим та гендерним складом. Нами було вирішено відмовитися від плацебо-контролю через завідомо недостатній рівень знеболювання в цій групі. Усі хворі оперовані в умовах збалансованої ендотрахеальної анестезії: тіопентал натрію + кетамін 0,5 мг/кг одноразово + фентаніл 7,2–8,4 мкг/кг/год із міорелаксацією атракурію бесилатом 0,45–0,55 мг/кг.
Рівень болю оцінювали в спокої за допомогою візуальної аналогової шкали (ВАШ) через 6, 24 та 48 годин після завершення оперативного втручання.
Пацієнти 1-ї групи в складі премедикації, за 40 хв до оперативного втручання, отримували 50 мг декскетопрофену. Післяопераційне знеболювання проводилося шляхом планового введення декскетопрофену 50 мг кожні 8 годин.
Пацієнти 2-ї групи в складі премедикації, за 40 хв до оперативного втручання, отримували 50 мг рофекоксибу внутрішньом’язово. Післяопераційне знеболювання проводилося шляхом планового введення рофекоксибу 25 мг на добу.
При рівні болю вище за 30 балів за ВАШ хворим обох груп додатково вводився метамізол 1000 мг внутрішньовенно одноразово. Якщо рівень болю перевищував 50 за ВАШ або введення метамізолу не зменшувало рівень болю нижче від 30 балів протягом 30 хв, пацієнти отримували 10 мг морфіну.
Через добу після припинення знеболювання проводилась оцінка суб’єктивної задоволеності післяопераційною аналгезією за критеріями «добре», «задовільно», «незадовільно».
Статистичні методи
Дані подані у вигляді середнього арифметичного (95% довірчий інтервал; n = розмір вибірки). Рівень відмінності між групами даних оцінювали із використанням методу порівняння довірчих інтервалів. Гіпотеза про відмінність груп приймалася при відсутності перекриття довірчих інтервалів. При перекритті довірчих інтервалів використовувався U-критерій Манна — Уїтні для непараметричних даних. Гіпотеза про відсутність відмінності груп підтверджувалася при коефіцієнті р > 0,05. Статистичний аналіз виконано за допомогою програми SPSS, версія 17.0 для Windows.
Результати
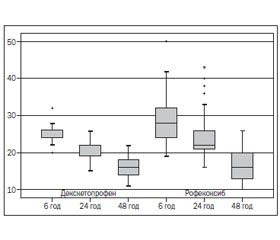
Середній рівень болю через 6 годин після оперативного втручання становив для декскетопрофену 25,2 (24,4; 26,0; n = 33) та для рофекоксибу 29,2 (26,4; 32,0; n = 33). Через 24 години ці показники становили відповідно 20,7 (19,7; 21,6; n = 33) та 24,5 (22,0; 26,9; n = 33) а через 48 годин — 16,4 (15,3; 17,4; n = 33) та 16,3 (14,9; 17,7; n = 33) відповідно. Рівень болю був вірогідно нижчим у групі декскетопрофену через 6 та 24 години та порівнювався з таким у групі рофекоксибу (р = 0,722) до другої доби післяопераційного періоду. Ураховуючи, що НПЗЗ не мають кумулятивного ефекту, вирівнювання інтенсивності болю на другу добу можна пояснити природним зниженням інтенсивності запальних процесів у післяопераційній рані.
Аналіз отриманих результатів показав, що жоден досліджуваний препарат не забезпечив 100% адекватного періопераційного знеболювання і потребував додаткового призначення аналгетиків, у тому числі і наркотичних. У першу добу в пацієнтів, які отримували декскетопрофен, зареєстровано 0,46 (0,26; 0,66; n = 33) випадку додаткового введення метамізолу та 0,09 (0,01; 0,19; n = 33) випадку використання наркотичного аналгетика. У групі рофекоксибу додаткове введення ненаркотичних аналгетиків відмічено в 0,82 (0,58; 1,1; n = 33) випадку, а наркотичних аналгетиків — в 0,15 (0,58; 1,1; n = 33). На другу добу в групі декскетопрофену зареєстровано 0,18 (0,04; 1,1; n = 33) випадку додаткового знеболювання ненаркотичними аналгетиками, у групі рофекоксибу — 0,33 (0,16; 0,50; n = 33). Потреби в наркотичних аналгетиках на другу добу в жодній групі не було. Таким чином, у першу добу спостерігалася статистично вірогідна (p = 0,022) різниця між групами у витраті метамізолу. Статистичної різниці в потребі в наркотичних аналгетиках та метамізолі на другу добу не було.
Суб’єктивна оцінка загальної якості знеболювання відображена в табл. 2.
Висновки
1. Використання НПЗЗ у премедикації перед апендектомією відповідає стратегії preemptive analgesia.
2. Монотерапія як декскетопрофеном, так і рофекоксибом не дозволяє досягти адекватного контролю болю у всієї популяції пацієнтів, які перенесли апендектомію, але може бути рекомендована як базисне знеболювання.
3. Декскетопрофен у режимі введення 50 мг кожні 8 год забезпечував кращу якість та меншу потребу в додатковому знеболюванні в першу добу післяопераційного періоду порівняно з рофекоксибом 25 мг кожні 24 год. На другу добу вірогідної різниці між препаратами не було, що зумовлено природним перебігом раньового процесу, а саме зниженням інтенсивності запальних реакцій у рані.
4. Жодного пацієнта не виключено з дослідження через побічну дію препаратів, що свідчить про достатній профіль безпеки обох препаратів.
5. Наявність переваг у знеболюванні неселективним протизапальним засобом декскетопрофеном над інгібітором ЦОГ-2 в еквіаналгетичних дозах може свідчити про значущу роль ЦОГ-1 у формуванні периферичного компонента післяопераційного болю та потребує подальшого дослідження.
Конфлікт інтересів. Автор повідомляє про відсутність конфлікту інтересів у даній роботі.
/145.jpg)

/146.jpg)