Статья опубликована на с. 20-21 (Укр.)
На сегодняшний день наиболее надежными критериями оценки состояния здоровья пациентов остаются лабораторные, функциональные, инструментальные и другие методы исследования. Предполагается, что все они в комплексе представляют собой мощный и эффективный инструмент ранней диагностики значительной части известных нозологических форм, а также мониторинга течения заболевания и оценки эффективности проводимой терапии [1].
Современная медицина всегда предъявляла высокие требования к методам исследования, что обусловливает их модификацию, усовершенствование и, как следствие, повышение чувствительности. Именно поэтому арсенал врача постоянно пополняется новыми диагностическими методами, имеющими более высокую воспроизводимость и специфичность [1–3].
Вместе с тем врачу постоянно приходится принимать решение о выборе наиболее оптимального количества методов исследования, которые он назначает своему пациенту. Анализ большого количества показателей нередко бывает трудоемким, а при предпатологическом состоянии организма пациента — зачастую неэффективным. Поэтому постоянно существует острая необходимость в разработке принципиально новых подходов к анализу результатов исследований, что позволит врачу принимать наиболее правильное решение относительно постановки диагноза и выбора тактики лечения. Данная необходимость становится весьма острой, учитывая предстоящее в ближайшее время вхождение мультиплексного анализа в число клинико-лабораторных тестов. Когда это произойдет, без
IT-технологий врачу будет практически невозможно получить объективную информацию о состоянии пациента. Поэтому уже сейчас делаются попытки оптимизировать процесс обработки результатов лабораторных, функциональных и других тестов [3].
Наряду с этим в медицине, как и в любой другой науке, существует два фундаментальных аналитических подхода: механистический (дифференциальный) и системный (интегральный). В первую очередь это относится к обработке, систематизации и анализу данных, которые получают в результате обследования пациентов. Как правило, в этих случаях наши врачи руководствуются механистическим принципом — сравнением результатов исследований с референтными значениями или уровнями. Входит результат в пределы нормы — хорошо, не входит — плохо. Все, казалось бы, просто. При этом в подавляющем большинстве случаев врачом используются абсолютные значения результатов обследования больного, характеризующие отдельные признаки и свойства. А ведь врачу приходится иметь дело с целостным организмом, структурно-функциональное состояние которого можно охарактеризовать при помощи тысяч постоянно изменяющихся показателей и их соотношения [4–5].
Однако нельзя не отметить тот факт, что в последние годы с целью оценки состояния здоровья пациента, определения тяжести течения заболевания, выявления прогностических рисков как возникновения заболевания, так и дальнейшего течения уже сформировавшейся патологии все чаще используются интегральные медицинские показатели (ИМП). К ним относятся различные коэффициенты, индексы, шкалы оценки различных структур и функций. По своей сути использование ИМП — лишь первый шаг на пути к комплексной интегральной технологии определения состояния целостного организма. К числу наиболее простых, известных и достаточно часто используемых врачами можно отнести такие показатели, как индекс массы тела, коэффициент атерогенности, иммунорегуляторный индекс, международное нормализованное отношение и некоторые другие [6].
Методики расчета различных ИМП, как правило, существенно различаются. В простейшем случае это может быть отношение одного абсолютного показателя к другому. Например, коэффициент де Ритиса рассчитывается по формуле АСТ/АЛТ. В то же время расчет десятилетнего риска кардиоваскулярной катастрофы с использованием шкалы FHS представляет собой достаточно сложное и трудоемкое вычисление [2].
Ежегодно в мире разрабатывается, апробируется и внедряется в медицинскую практику большое число ИМП, которые находят свое применение в самых различных областях медицины. Это и неудивительно, ведь использование данных относительных показателей дает врачу значительные преимущества. Так, в кардиологии широко используют шкалы SCORE, PROCAM, FHS, коэффициент атерогенности и многие другие ИМП. Из обычного анализа крови, например, можно рассчитать более двадцати гематологических интегральных показателей, таких как лейкоцитарный индекс интоксикации, индекс сдвига лейкоцитов крови, индекс аллергизации, реактивный ответ нейтрофилов и прочие [7–10].
Несмотря на свою относительность, ИМП более информативны, чем абсолютные величины, которые используются для их расчета [4]. В этом легко можно убедиться на простом примере. Даже такой простой интегральный показатель, как индекс массы тела, дает врачу информацию куда более высокого уровня, чем обычные килограммы массы тела и сантиметры роста пациента. Опытный врач по величине индекса массы тела может судить о многих процессах, происходящих в организме пациента. В частности, об интенсивности обмена веществ, его характере и общей направленности.
ИМП можно разделить на две большие группы индексов и коэффициентов, а также на оценочные шкалы. Для получения индексов и коэффициентов, как правило, используются несложные математические расчеты (отношения, простые формулы и др.). Значительно более сложные математические подходы реализуются в оценочных шкалах, что дает информацию не только диагностического характера, но и, что более важно, прогностического плана. К числу наиболее важных оценочных шкал относятся SCORE, PROCAM, ASSIGN, QRISK, FHS и другие. Данные шкалы были получены в результате многолетних эпидемиологических исследований, проведенных в развитых странах [8–10]. Все они имеют большое прогностическое значение в кардиологии, реже — в других областях медицины.
Так, доказана высокая информативность интегральных гематологических показателей при онкологических заболеваниях (ЛИИ, ИСЛК). Известно, что успех лечения онкологических больных во многом определяет ранняя диагностика и использование комплексного подхода в ее проведении. Поэтому использование интегральных гематологических показателей может быть перспективным в комплексных мероприятиях ранней диагностики онкологических заболеваний [13–15].
Дерматологические и гематологические ИМП признаны эффективными в дифференциальной диагностике дерматозов. Показатели данных ИМП увеличиваются от 1,5 до 2 раз в зависимости от стадии заболевания и выраженности эндогенной интоксикации. Так, тенденция к увеличению данных показателей свидетельствует о разгаре заболевания, тогда как постепенное их снижение говорит о предстоящем улучшении состояния пациента. В травматологии ИМП активно используются в прогнозировании течения и исхода переломов и вывихов [16].
Выявлены коррелятивные связи между величиной отдельных ИМП, с одной стороны, и степенью тяжести бронхиальной астмы, хроническим обструктивным бронхитом и патологией, связанной с дисфункцией щитовидной железы у беременных, — с другой. ИМП также нашли свое применение в педиатрии, в частности при оценке поствакцинальных ревматических осложнений и диагностике заболеваний верхних дыхательных путей [16].
ИМП широко применяются гепатологами для оценки степени фиброза печени при различных ее заболеваниях. Так, в частности, для оценки характера и прогноза течения хронического гепатита С используются такие ИМП, как APRI, фиброиндекс, фибротест, индекс Форнса и др. При этом данные ИМП имеют как диагностическое, так и прогностическое значение, что значительно упрощает решение терапевтических, профилактических и реабилитационных задач, которые стоят перед гепатологом. Также отмечена высокая прогностическая и диагностическая значимость шкал MELD, FIB-4 при гепатите [16–18].
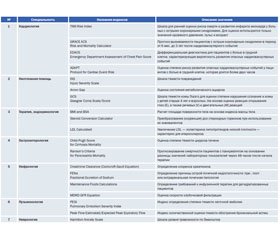
Как видим, на сегодняшний день ИМП широко применяются для оценки состояния организма пациентов при различных заболеваниях. Наиболее популярные и часто используемые врачами во всем мире ИМП представлены в табл. 1.
Таким образом, ИМП являются более информативными, чем те абсолютные значения, на основании которых они рассчитываются. Использование ИМП в клинической практике позволяет врачу правильно поставить диагноз заболевания, определить стратегию лечения, оценить эффективность проводимой терапии, прогнозировать исход заболевания, определить стратегию дальнейшей коррекции лечения для достижения максимального эффекта и многое другое.
Естественно, что далеко не все клиницисты готовы кардинально менять принципы своей работы. В то же время использование всего лишь одного ИМП уже позволит врачу получить значительные преимущества. Например, включение в клинический алгоритм семейного врача таких прогностических шкал, как SCORE и PROCAM, повысит эффективность его работы в плане профилактики сердечно-сосудистых заболеваний [3].
Список литературы
1. Меньшиков В.В. Лекарственная терапия и результаты лабораторных исследований. Лекция // Клин. лаб. диагностика. — 2001. — № 1. — С. 21-36.
2. Назаренко Г.И., Кишкун А.А. Клиническая оценка результатов лабораторных исследований. — 2-е изд. — М.: Медицина, 2006. — 544 с.
3. Сокол А.Ф. Современный врач: особенности, пути оптимизации профессиональных и личностных качеств // Социология медицины. — 2014. — № 1 (24). — С. 7-14.
4. Аврунин А.С., Тихилов Р.М., Егоров К.С. Проблемы дифференциальной (механизменной) и интегральной (системной) оценки организма // Гении ортопедии. — 2004. — № 4. — С. 110-117.
5. Сорокин О.Г., Ушаков И.Б. Актуальность целостной оценки состояния организма. Сборник научных трудов Шестого все–российского симпозиума по проблемам боевого стресса. — М., 2007. — С. 47-54.
6. Крыжановский Г.Н. Дисрегуляционная патология и патологические интеграции в нервной системе // Журнал неврологии и психиатрии. — 2009. — № 1. — С. 4-9.
7. Kannel W.B., D’Agostino R.B., Silbershatz H., Belanger A.J., Wilson P.W., Levy D. Profile for Estimating Risk of Heart Failure // Arch. Intern. Med. — 1999 Jun 14. — 159 (11). — P. 1197-204.
8. Wilson P.W.F., D’Agostino R.B., Levy D., Belanger A.M., Silbershatz H., Kannel W.B. Prediction of Coronary Heart Disease Using Risk Factor Categories // Circulation. — 1998. — 97. — P. 1837-1847.
9. Assmann G., Schulte H., Cullenand P., Seedorf U. Assessing risk of myocardial infarction and stroke:new data from the Prospective Cardiovascular Münster (PROCAM) study // European Journal of Clinical Investigation. — 2007. — 37. — P. 925-932.
10. Hippisley-Cox J., Coupland C., Vinogradova Y., Robson J., Minhas R., Sheikh A., Brindle P. Рredicting cardiovascular risk in England and Wales: prospective derivation and validation of QRISK2 // BMJ. — 2008 Jun 28. — 336 (7659). — P. 1475-82.
11. Парахонский А.П. Гематологические критерии диагностики бронхолегочных заболеваний // Фундаментальные –исследования. — 2005. — № 8. — С. 42-43.
12. Мустафина Ж.Г., Крамаренко Ю.С., Кобцева В.Ю. Интегральные гемато–логические показатели в оценке иммунологической реактивности организма у больных с офтальмопатологией // Клин. лаб. диагностика. — 1999. — № 5. — С. 47-48.
13. Левченко К.Ф. Гематологические индексы и их значение в ранней диагностике и диагностике стадий рака молочной железы // Сибирский онкологический журнал. — 2008. — Приложение № 1. — С. 78-79.
14. Левченко К.Ф., Магарилл Ю.А. Значение гематологических индексов в динамике заболеваний молочной железы // Сибирское медицинское –обозрение. — 2009. — Т. 58, № 4. — С. 58-61.
15. Гирин С.В., Юрченко И.В. Интегральные гематологические показатели в оценке состояния организма // Биологическая терапия. — 2010. — № 4. — С. 18-21.
16. Дябкин Е.В., Дунаевская С.С., Антюфриева Д.А. Изучение интегральных гематологических индексов у больных с механической желтухой доброкачественного генеза // Клиническая лабораторная диагностика. — 2010. — № 8. — С. 23-29.
17. Stauber R.E., Lackner C. Noninvasive diagnosis of hepatic fibrosis in chronic hepatitis C // World J. Gastroenterology. — 2007. — 13 (32). — P. 4287-4294.
18. Shawky A.F., Serag E., Dalia O., Laila R., Mohamed H.K. Noninvasive assessment of hepatic fibrosis in Egyptian patients with chronic hepatitis C virus infection // World J. Gastroenterology. — 2012. — 18 (23). — P. 2988-2994.
Материал предоставлен компанией «УАМБ»

/20_u.jpg)