Газета «Новости медицины и фармации» 15 (509) 2014
Вернуться к номеру
Современные проблемы лечения и профилактики инфекций мочевой системы у детей
Авторы: Багдасарова И.В., Лавренчук О.В. - ГУ «Институт нефрологии НАМН Украины», г. Киев
Разделы: Справочник специалиста
Версия для печати
Распространенность микробно-воспалительных заболеваний мочевыделительной системы (цистит, уретрит, вульвит, пиелонефрит), согласно проведенным эпидемиологическим исследованиям в Украине, составляет 19 на 1000 детского населения, что соответствует эпидемиологическим показателям других стран мира. Согласно статистическим отчетам МЗ Украины, распространенность заболеваний почек и мочевой системы у детей в нашей стране за последние 5 лет практически не изменилась (10,23–10,34), несколько уменьшилась распространенность хронического пиелонефрита (ПН) (6,58–6,05) и увеличилась — острого цистита (2,33–2,62), кроме того, обращает на себя внимание стойкая тенденция к увеличению патологии мочевыделительной системы в промышленных городах. Аналогичная тенденция отмечена и по уровню заболеваемости. По результатам исследования 2133 детей г. Киева в возрасте от 1 года до 15 лет, симптомы инфекции мочевыделительной системы (ИМС) обнаруживались у 1 % детей, а бессимптомная бактериурия — у 1,2 %.
Согласно европейским данным, приведенным Д.Д. Ивановым (2013), на первом году жизни от ИМС чаще страдают мальчики (3,7 против 2 % у девочек), в последующем соотношение меняется.
Изучая современные особенности лечения и профилактики, необходимо остановиться на вопросах терминологии и классификации ИМС у детей.
ИМС — микробно-воспалительный процесс органов мочевыделительной системы без уточнения его локализации (мочевыводящие пути или почечная паренхима) и определения его характера. К ИМС относятся пиелонефрит, цистит, уретрит.
При наличии практически одинаковых признаков ИМС — клинического течения, микробиологического спектра, степени отрицательного воздействия на функциональное состояние почки — возможности обратного развития могут существенно различаться и требуют дифференцированного подхода к лечению.
Согласно классификации, принятой на II съезде нефрологов Украины (2005), выделяют острый и хронический пиелонефрит, острый и хронический цистит и те же нозологические формы дополняются характеристикой «осложненный» и «неосложненный».
В европейских странах и США применяют следующую классификацию ИМС у детей:
1. Вид ИМС: осложненная и неосложненная.
2. Характер ИМС: бессимптомный и симптомный.
3. Локализация ИМС: пиелонефрит, цистит, уретрит.
Достаточно удачной для практической медицины является классификация ИМС, предложенная M.H. Ebell (2006), — дифференциация по клинико–лабораторным показателям (табл. 1).
Безусловно, из всей группы ИМС наибольшую проблему для клиницистов представляет ПН, т.к. именно ПН с рецидивирующим течением и не всегда успешным лечением приводит к формированию хронической почечной недостаточности (ХПН), являющейся серьезной социально-экономической проблемой. Медико-социальная актуальность проблемы заключается в склонности заболевания к прогрессированию, что приводит к инвалидизации больных. По данным регистра EDTA (Европейская ассоциация диализа и трансплантаций), ежегодная заболеваемость ХПН у детей в Европе составляла 7,1 на 1 млн населения в 1980–1984 годах и 9,9 — в последующие 15 лет. Причинами развития ХПН в детском возрасте, в отличие от взрослого населения (по данным NAPRTCS, 2005), считаются обструктивные нефропатии (21,6 %), аплазия или дисплазия почек (17,6 %), фокально-сегментарный гломерулосклероз (8,7 %), рефлюкс-нефропатия (8,3 %), ПН или интерстициальный нефрит (1,3 %), хронический гломерулонефрит (1,2 %).
Профилактика рецидивирования и хронизации ПН является одной из ведущих задач педиатров и нефрологов. Согласно данным В.Г. Майданника, у 86 % больных с рецидивирующим течением ИМС первый эпизод реинфекции отмечался через 6 месяцев после первичного эпизода. Рецидивирующей считается ИМС при наличии 3 и более рецидивов в год.
Обращает на себя внимание изменение клинического течения ПН — прогрессивное увеличение количества латентных и малосимптомных форм и снижение показателей достижения полной ремиссии. Причем эти особенности современного течения ПН относятся не только к вторичным обструктивным, но и к первичным необструктивным вариантам ПН. Как при любом инфекционном процессе, взаимодействие факторов вирулентности возбудителя и состоятельности защитных механизмов макроорганизма в значительной мере определяет течение и исход заболевания. Анализируя исследования современных авторов, можно заключить, что хронизация инфекций мочевыделительной системы обусловлена нарушением равновесия факторов микро- и макроорганизмов в виде возрастания уропатогенности возбудителя и снижения возможностей общего и местного иммунитета макроорганизма, что приводит к неполной элиминации возбудителя из организма и хронической его персистенции в уротракте. Из этого следуют определенные требования к терапии и профилактике ИМС у детей.
Следует отметить, что за последнее десятилетие проведено множество значительных исследований в микробиологии, молекулярной биологии, иммунологии, которые изменили представление о механизмах развития инфекционных процессов. В полной мере это относится и к возбудителю ИМС — кишечной палочке, доминирующей в моче приблизительно у 80 % пациентов. Большим вкладом в понимание механизмов хронизации и рецидивирования ИМС, вызванных кишечной палочкой, стала теория патогенетического каскада.
L. Cegelski с соавторами (2008) разработали механизм патогенетического каскада уропатогенной E.coli. Было доказано, что бактерии вначале прикрепляются к мембранам клеток хозяина с помощью адгезинов на верхушках пилей. Потом проникают в клетку, где начинают размножаться, формируя внутриклеточные биологические сообщества, продуцируя биопленки, которые могут располагаться как внутриклеточно, так и на поверхности клеточных мембран. Биопленки защищают внутриклеточную колонию, в том числе и от воздействия антимикробных препаратов. Когда масса размножившихся бактерий становится критической, микробы разрывают клетку, выходят из нее и атакуют соседние. В возможности существования такого каскада в эпителии мочевого пузыря сомнений практически нет, однако наличие его в других отделах мочевой системы остается спорным. Благодаря теории каскада можно объяснить патогенез рецидивирующего цистита. За счет кругооборота бактерий в мочевом пузыре возникает второй резервуар кишечной палочки (первым считается кишечник). Наличие добавочных резервуаров бактерий в мочевыводящих путях может облегчить проникновение микроорганизмов в верхние отделы мочевого тракта, в том числе и в почку.
В распространении уропатогенных штаммов E.сoli ведущая роль принадлежит факторам инвазии — благодаря им бактерии проникают в клетку — и факторам, угнетающим фагоцитоз: эндотоксины выявлены только у грамотрицательных микроорганизмов. Важное значение для практической нефрологии имеют такие понятия, как факторы патогенности микроорганизмов — адгезия и колонизация, с их помощью бактерии распознают рецепторы на мембранах клеток, прикрепляются к ним и колонизируют разные поверхностные структуры клеточной стенки. Высокая степень адгезионности кишечной палочки способствует проникновению и фиксации ее в мочевыводящих путях с выделением эндотоксина. Далеко не всегда антибактериальная терапия приводит к полной санации мочи и тканей мочевыводящей системы, наличие E.coli в контаминационных значениях свидетельствует о персистенции возбудителя в организме. Это говорит или о неадекватности выбранной терапии, или о наличии резистентности микроба к препарату. Длительная персистенция микроорганизма в мочевыделительной системе приводит к рецидивированию ИМС у детей. Установлено, что штаммы E.coli, вызывающие ПН, имеют больший набор факторов патогенности, чем те, которые вызывают ИМС. Наличие вирулентных свойств генетически детерминировано и различно у уропатогенных штаммов, вызывающих ПН, цистит и асимптомную бактериурию.
Рецидивированию и хронизации ИМС способствует и снижение местной и общей иммунорезистентности организма ребенка. Длительное и частое антибактериальное лечение пациентов с рецидивирующим течением ПН, циститов приводит к нарушению защитных свойств как слизистых уроэпителия, так и клеточного иммунитета организма. Все вышесказанное вынуждает клиницистов искать новые пути лечения и профилактики ИМС у детей.
Лечение ИМС у детей имеет четыре основные цели:
1. Устранение симптомов заболевания и эрадикация возбудителя при остром эпизоде.
2. Профилактика рецидивов ИМС.
3. Профилактика склеротических изменений в почках.
4. Коррекция сопутствующих урологических нарушений (Эрман М.В., 2012).
Для устранения микробно-воспалительного процесса в мочевыделительной системе применяются антибактериальные препараты. В настоящее время имеется 150–200 препаратов и более 600 наименований (Зоркин, 2001), но спектр препаратов, используемых для лечения детей, ограничен как возрастными особенностями, так и ростом резистентности микроорганизмов. Возрастающая резистентность к антибактериальным препаратам стала темой обсуждения ВОЗ в 2011–2012 гг., вследствие чего была принята «Глобальная стратегия по сдерживанию резистентности микроорганизмов к антимикробным препаратам». Основной целью этой стратегии стало переосмысление подходов к антибактериальной терапии, отход от штампов назначения антимикробных препаратов прошлых десятилетий, поиск новых препаратов и альтернативных или дополнительных методов лечения. По мнению Naber, для всех антибиотиков, которые применяются давно, существует очень высокий риск необратимости их высокой резистентности. Поэтому назначение антибиотиков должно обосновываться и контролироваться. Wagenlehner призывает по возможности избегать антибиотиков широкого спектра действия. Выходом является назначение альтернативной терапии, такой как мультимодальная комбинация фитопрепаратов.
На базе отделения детской нефрологии ГУ «Институт нефрологии НАМН Украины» в течение 7 лет проводилось изучение ИМС у 404 детей с целью разработки новых, более эффективных методов топической диагностики, лечения и профилактики.
Все пациенты в активной стадии ПН неоднократно получали антибактериальную терапию коротким курсом или по ступенчатой схеме. Проспективное наблюдение за этой кагортой больных в течение 6 лет зафиксировало трансформацию острого первичного ПН в хронический в 16,9 % случаев, а при вторичном варианте трансформация в хронический состоялась в 38,5 % наблюдений.
Кроме того, у 45,6 % больных с хроническим вторичным ПН, несмотря на отсутствие клинико-лабораторных признаков активного воспаления в почках в 22 % наблюдений, обнаружено вторичное сморщивание почки, а у 12 % констатирована ХПН.
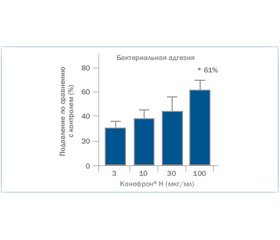
Результаты проведенного исследования заставили искать альтернативные методы лечения и профилактики ПН с рецидивирующим течением. Поскольку все пациенты неоднократно получали антибактериальные препараты коротким курсом или по ступенчатой схеме, мы обратились к препаратам растительного происхождения как альтернативе. Препарат Канефрон® Н («Бионорика СЕ») является комплексным растительным препаратом с противовоспалительным, спазмолитическим и антибактериальным эффектом. Проведенное в 2013 г. исследование (Кюнсте Г. и др., Германия) доказало высокую антибактериальную активность препарата Канефрон® Н в связи с его антиадгезивными свойствами. Антиадгезивные эффекты исследовали с помощью подавления in vitro адгезии E.coli к клеткам мочевого пузыря человека. Также изучали противовоспалительные эффекты и воздействие на гиперрефлекторный мочевой пузырь в эксперименте. Было доказано, что Канефрон® Н активен против адгезии уропатогенных бактерий к уротелию мочевого пузыря in vitro. Канефрон® Н ослаблял воспалительные реакции in vitro и in vivo, после перорального применения Канефрон® Н был способен угнетать гиперактивность мочевого пузыря в модели интерстициального цистита. Кроме того, в работе доц. Е.И. Слободян и Н.Н. Каладзе «Восстановительное лечение детей, больных хроническим пиелонефритом, на этапе санаторно-курортной реабилитации» было показано, что применение препарата Канефрон® Н у детей с хроническим пиелонефритом в фазе ремиссии угнетает латентное воспаление в почечной паренхиме и препятствует склеротическим изменениям, ведущим к необратимой утрате фильтрующей способности почек. Методика реабилитации пациентов с хроническим пиелонефритом с применением препарата Канефрон® Н в условиях бальнео- и физиотерапевтического лечения получила государственный патент МЗ Украины 2013 г.
Полученные результаты свидетельствовали о мультифакторной активности препарата Канефрон® Н, специализированной для лечения инфекций мочевых путей. Мы применяли препарат в течение 3 месяцев после антибактериальной терапии у детей в активной стадии ПН, что способствовало полной элиминации возбудителя из организма и нормализации иммуно-реактивности организма. У пациентов в стадии ремиссии, но имевших рецидивирующее течение ПН в анамнезе, Канефрон® Н назначался профилактически курсами по месяцу в осенне-весенний период с целью превентивной санации мочевыделительной системы, стимуляции иммунитета и улучшения уродинамики.
Одним из критериев эффективности назначения препарата Канефрон® Н больным с хроническим рецидивирующим течением ПН являлась частота рецидивов заболевания в течение года после окончания терапии. У пациентов основной группы наблюдалось 0,06 и 0,08 рецидива/год через 9 месяцев, тогда как в группе детей, не применявших Канефрон® Н, рецидивы документированы у 0,52 больного/год. Кроме того, было отмечено, что у детей, часто болеющих ОРВИ, после проведения курса терапии препаратом Канефрон® Н в течение 9 месяцев не документировались интеркуррентные вирусные инфекции: 0 и 0,09 больного/год против 0,34 в группе детей, не принимавших препарат. Полученные результаты наблюдения позволили рекомендовать введение препарата Канефрон® Н в схему лечения и профилактики ИМС у детей длительностью от 1 до 6 месяцев.
Таким образом, с учетом возрастающей резистентности микроорганизмов к основным группам антибактериальных препаратов, сниженного иммунитета у часто болеющих детей, высокой частоты осложнений и побочных действий от длительного применения антибиотикотерапии, альтернативным способом лечения и профилактики ИМС у детей является все более широкое применение растительных мультифакторных препаратов.
1. Наказ МОЗ України № 627 від 03.11.2008 «Про затвердження протоколу лікування дітей з інфекціями сечової системи і тубулоінтерстиціальним нефритом».
2. The Cochrane Database of systematic Reviews. — 2010, Issue 9.
3. Інфекції сечових шляхів у дітей: оновлення 2012 року / Іванов Д.Д. // Почки. — 2013. — № 1 (3). — С. 55–60.
4. Инфекция мочевой системы у детей. Терапия и резистентность / Эрман М.В. // Материалы IV Юбилейной международной конференции АО Olainfarm. — 2012. — С. 28–34.
5. Критерии диагностики и антибактериальная терапия пиелонефрита у детей / Майданник В.Г., Бурлай В.Г., Кампи Ю.Ю. // Клиническая антибиотикотерапия. — 2003. — № 3 (23). — С. 25–32.

/10_m/10_m.jpg)
/10_m/10_m2.jpg)