Газета «Новости медицины и фармации» Кардиология (475) 2013 (тематический номер)
Вернуться к номеру
Острый коронарный синдром: нарушения иммунных процессов, метаболизм липидов, белков и предикторы воспаления
Авторы: Шушляпин О.И., к.м.н., доцент, Шелест А.Н., Борзова Е.Ю., Рынчак П.И. - Харьковский национальный медицинский университет, кафедра внутренней медицины № 2, клинической иммунологии и аллергологии
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Атеросклероз — одновременно проявление как биохимических нарушений обмена липидов, так и воспалительных процессов, требующих комплексной оценки состояния цитокинов, Среактивного белка (СрБ) и сывороточного амилоида А.
При остром коронарном синдроме, когда нарушается метаболизм липидов и белков, происходит образование аутоантигенов, противокардиальных липидов и белков, что приводит к повреждению кардиомиоцитов и коронарных сосудов.
Механизмы повреждающего действия иммунологических процессов связаны с гиперпродукцией IgG и IgA вследствие нарушения регуляторной функции Тсупрессоров, активации Влимфоцитов и комплемента с образованием иммунных комплексов [1, 5].
Иммунные нарушения при ишемической болезни сердца (ИБС) рассматриваются как фактор, определяющий во многом возникновение и течение заболевания. Это влияние особенно манифестируется при остром коронарном синдроме — нестабильной стенокардии, остром инфаркте миокарда, когда нарушения метаболизма белков и липидов ведут к образованию аутоантигенов, противокардиальных и сосудистых антител, что вызывает повреждение миокарда и эндоваскулярные коронарные сосудистые нарушения [2].
В некоторых случаях стенокардия и инфаркт миокарда встречаются у лиц с нормальным уровнем липидов в плазме крови. Вместе с тем известно, что дестабилизированная атеросклеротическая бляшка является источником провоспалительных цитокинов, которые способны увеличивать инфильтрацию сосудистой стенки воспалительными клетками, усиливать атерогенез, прокоагулянтную активность эндотелия, воздействовать на метаболизм липидов и формировать острый коронарный синдром [6].
Ишемическая болезнь сердца попрежнему находится в центре внимания клиницистов в связи с широкой распространенностью и высокой смертностью. По данным Американской ассоциации сердца, ежегодно острый инфаркт миокарда (ОИМ) развивается примерно у 1,5 миллиона человек, и летальность продолжает оставаться высокой, несмотря на очевидные успехи современной кардиологии. Как известно, нарушение целостности покрытия атеросклеротической бляшки с образованием эрозии, трещины или ее разрыва с последующим формированием на этом месте пристеночного или обтурационного тромба, а также активации нейрогуморальных систем (симпатоадреналовой, ренинангиотензинальдостероновой) лежит в основе нестабильной стенокардии, ОИМ и внезапной смерти. В последние годы широко обсуждается нарушение баланса цитокинов, неспецифических индикаторов воспаления, таких как СрБ и сывороточный амилоид А, а также их участие в развитии внезапной смерти [7].
Цитокины — гликопротеиды, участвующие в созревании и дифференциации клеток крови, активирующие рост и влияющие на функциональную активность лимфоцитов, обеспечивают сложные корпоративные взаимодействия между клетками. Доказана их роль при иммунологических состояниях и в формировании воспалительных процессов. Провоспалительные цитокины (ПЦ) играют важную роль в процессах гиперкоагуляции крови, участвуют в активации процессов рестенозирования коронарных артерий после ангиопластики, в нарушении регуляции сосудистого тонуса, развитии острого коронарного синдрома и формировании синдрома эндотелиальной дисфункции, индукции метаболических процессов в скелетных мышцах и прогрессировании мышечной дистрофии. У больных ОИМ повышение уровня ПЦ является медиатором ответа острой фазы [8].
Оценка вышеуказанных изменений в целом может служить показателем тяжести коронарного синдрома при ИБС и его осложнениях и определить дифференциальнодиагностические критерии прогрессирования заболевания с позиции участия неспецифических индикаторов воспаления, с одной стороны, и нарушений липидного обмена — с другой, а также изучение динамики уровней провоспалительных цитокинов (интерлейкин6, 1бета (ИЛ6 и 1бета)) и СрБ в сыворотке крови больных острым коронарным синдромом (ОИМ, нестабильная стенокардия).
Материал и методы исследования
Обследовано 130 больных с острым коронарным синдромом. Нестабильная стенокардия определена у 70 больных, у 60 пациентов диагностирован ОИМ.
Диагноз ОИМ устанавливали на основе возникшего и продолжавшегося больше 30 минут болевого синдрома в загрудинной области, элевации сегмента ST более 0,2 мм в двух и больше отведениях с повышением креатинфосфокиназы более чем в 2 раза. Больные ОИМ были разделены на 2 группы: в первую группу вошли 60 больных, у которых диагностирован ОИМ с зубцом Q, во вторую группу — 40 больных с ОИМ без зубца Q.
Сывороточные уровни ПЦ определялись иммуноферментным способом (ИЛ6) и полуколичественно — уровень СрБ на 1, 6–7 и 26–27е сутки от начала ОИМ. При этом ПЦ у больных ОИМ были увеличены по сравнению со здоровыми лицами, пик сывороточной концентрации ИЛ6 и 1бета приходился на 6–7е сутки заболевания, что совпадает с окончанием формирования зоны некроза. Повышенный уровень ПЦ наблюдался и у больных ОИМ с зубцом Q, воспалительная реакция, обусловленная провоспалительными цитокинами — ИЛ6 и 1бета, у них более ярко выражена.
Длительность предшествующей ИБС у исследуемых больных составила от одних суток до 10 лет.
У больных 1й группы возникали различные осложнения ОИМ: кардиогенный шок, при котором в 3 случаях наблюдался летальный исход; нарушения ритма и проводимости — в 19 случаях; подострая аневризма — в 2 случаях; рецидивирующая сердечная астма и отек легких — в 5 случаях.
У пациентов с ОИМ в 5 случаях обнаружены различные нарушения ритма и проводимости.
У ряда обследованных больных ОИМ наблюдали сопутствующие заболевания: сахарный диабет II типа — в 6 случаях, язвенная болезнь в форме ремиссии — в 3, хронический необструктивный бронхит в фазе ремиссии — в 4 случаях.
Суточное мониторирование ЭКГ проводили на эхокардиографе Ultrasound Scanner model 628 A по стандартной методике.
Всем обследованным больным с ОИМ проводили повторное исследование содержания в плазме крови провоспалительных цитокинов (ИЛ6, 1бета) методом иммуноферментного анализа с использованием наборов ProCon (Россия) на 1, 6–7 и 26–28е сутки заболевания.
Больные ОИМ обеих групп получали медикаментозное лечение, включающее гепарин, нитраты, аспирин, ингибиторы ангиотензинпревращающего фермента, адреноблокаторы (метопролол, карведилол) и диуретики.
При нестабильной стенокардии определялось не менее двух болевых эпизодов в предыдущие 48 часов или сердечный приступ, который продолжался больше 20 минут. Во время приступа повышался сегмент ST и был увеличенным уровень креатинфосфокиназы в сыворотке крови. Всех больных с нестабильной стенокардией распределили на две группы: больные с нормальными показателями СрБ и с повышенным его уровнем.
Лечение больных с нестабильной стенокардией включало прием аспирина 125 мг, метопролола 100 мг/сут, нитрогранулонга 5,2 мг 2–3 раза в сутки, а также гепарина 20 тыс ЕД/сут в течение 4–5 дней. Нормальным уровнем СрБ считали значения до 6 мг/л.
Биохимическое исследование липидов включало определение в сыворотке крови общего холестерина, триглицеридов, холестерина липопротеинов низкой плотности (ХС ЛПНП) и холестерина липопротеинов высокой плотности (ХС ЛПВП) ферментным методом на автоанализаторе фирмы Boehringer Mannheim (Австрия). Уровень СрБ определяли методом латексагглютинации с использованием реактивов фирмы «Ольвекс Диагностикум» (Россия). Концентрацию фибриногена определяли методом твердофазного иммуноферментного анализа в сэндвичварианте (производство Центрального НИИ вакцин и сывороток им. И.И. Мечникова, Московская область, г. ПетровоДальнее).
Контрольную группу составили 10 здоровых лиц в возрасте от 25 до 48 лет.
Статистическая обработка полученных результатов проводилась на ЭВМ с использованием стандартного пакета прикладных программ. Достоверность различий оценивали по tкритерию Стьюдента.
Результаты и обсуждение
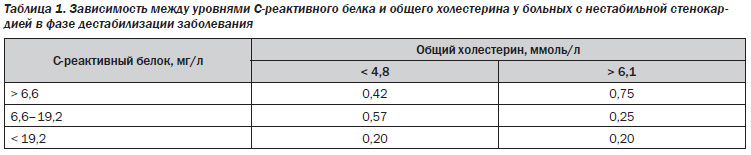
При нестабильной стенокардии в группе больных с повышенным уровнем СрБ за время периода наблюдения его показатели находились в пределах 6,6–19,2 мг/л (Р < 0,05) против первой группы с нормальными показателями СрБ и были повышены у 24 из 26 больных при поступлении и у 26 из 33 спустя 3 месяцев. У 81 % (21 больной) из этих 26 больных уровень СрБ был постоянно повышен на протяжении всего периода наблюдения, что составило 40 % из общего количества больных (53 чел.) (табл. 1).
За время наблюдения у 18 из 26 больных (69 % против 15 % больных первой группы) имело место ухудшение течения ИБС с дестабилизацией нестабильной стенокардии у 14 больных.
При изучении влияния взаимосвязи между уровнями СрБ, холестерина и фибриногена у больных с нестабильной стенокардией было установлено, что ухудшение течения ИБС имело место у 13,4 % больных с содержанием СрБ 6,6 мг/л, у 42 % больных наступило ухудшение при величинах СрБ 6,6–17,2 мг/л и у 67 % — с уровнем 17,2 мг/л и более.
Такая же зависимость наблюдалась и при сопоставлении уровня фибриногена и частоты ухудшения ИБС. При уровне фибриногена до 2,6 г/л частота ухудшения стенокардии имела место у 22 % больных, при уровне фибриногена 2,6–3,8 г/л — у 44 % больных и более 8 г/л — у 59 % больных.
Многофакторный анализ содержания в крови СрБ, холестерина и фибриногена и дестабилизации течения ИБС показал, что существует прямая зависимость между содержанием СрБ и холестерина и, особенно, фибриногена.
С учетом того, что уровень СрБ представляет индикатор воспалительного процесса, а увеличение уровня фибриногена в крови отражает скорость развития ИБС, изменение этих показателей может служить показателем прогрессирования заболевания и дестабилизации нестабильной стенокардии.
Повышенный уровень СрБ является маркером увеличения образования ИЛ1бета и 6, провоспалительных цитокинов, которые обладают и протромботическими свойствами. Кроме того, СрБ активирует моноциты, стимулируя образование тканевых факторов, и вызывает выброс интерлейкинов моноцитами и эндотелиальными клетками [9].
Конкретные механизмы островоспалительных реакций связаны с окислением липопротеинов низкой плотности и персистированием инфекции, что приводит к хроническому воспалению, о чем свидетельствует наличие положительной корреляции между титром антител к Chlamydia pneumonie у больных нестабильной стенокардией в условиях дестабилизации стенокардии, а также в условиях повышенного уровня фибриногена, как отражения активации протромбогенных механизмов развития нестабильной стенокардии.
На основании полученных данных можно сделать выводы о том, что уровень СрБ сыворотки крови повышен почти у половины больных нестабильной прогрессирующей стенокардией и это повышение точно коррелирует с возможным ухудшением течения стенокардии. Не было установлено зависимости между повышением содержания общего холестерина сыворотки крови и частотой ухудшения течения стенокардии. И, наконец, существует зависимость между повышением уровней фибриногена и СрБ с дестабилизацией течения ИБС (нестабильная стенокардия).
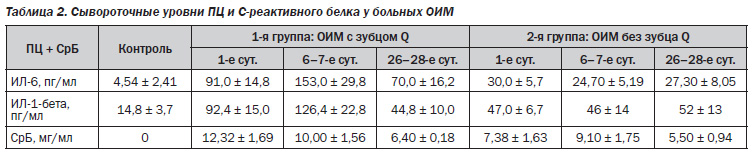
Уровни исследования ПЦ и СрБ в обеих группах больных с ОИМ и в группе контроля представлены в табл. 2.
Как видно из полученных данных, в первые сутки заболевания уровень ИЛ6 был выше у больных 1й группы, чем у больных 2й группы и группы контроля. На 6–7е сутки уровень сывороточного ИЛ6 был выше в 1й группе по сравнению со 2й группой, а на 26–28е сутки сохранялось повышение содержания ИЛ6 в 1й группе по сравнению со 2й группой.
Более выраженное увеличение сывороточных уровней ИЛ6 и 1бета у больных ОИМ с зубцом Q, нежели их значений у больных ОИМ без зубца Q, свидетельствовало о том, что глубина и площадь поражения миокарда зависят от способности ПЦ увеличивать адгезивность лейкоцитов к сосудистому эндотелию, вызывать инфильтрацию сосудистой стенки воспалительным процессом, усиливая атерогенез и стимулируя коагулянтную активность эндотелия, и тем самым воздействовать на метаболизм липидов. ПЦ также способны формировать признаки неблагоприятного течения сердечной недостаточности, обусловленной ИБС. При этом дисфункция левого желудочка стимулирует выброс ПЦ, тем самым включается цепная реакция патологических процессов, характерных для ОИМ с зубцом Q.
В целом полученные данные свидетельствуют о том, что провоспалительные цитокины играют важную роль в развитии ОИМ и нестабильной стенокардии, повышение их концентрации в крови является показателем тяжелого поражения коронарных сосудов, при этом воспалительная реакция, обусловленная ПЦ, более выражена у больных 1й группы с ОИМ и зубцом Q, а пик сывороточной концентрации ИЛ6 и 1бета на 6–7е сутки свидетельствует об окончании формирования зоны некроза при ОИМ с зубцом Q.
Взаимосвязь ПЦ и СРБ свидетельствует об ухудшении патологических процессов при нестабильной стенокардии и прогноза при ОИМ вследствие нарушения целостности атеросклеротической бляшки в местах атеросклеротического поражения.
Таким образом, нами обнаружена прямая зависимость между повышением уровней фибриногена, ЛПНП, СрБ и ПЦ, что требует разработки новых терапевтических подходов к лечению острого коронарного синдрома, направленному на комплекс терапевтических воздействий с устранением воспаления, блокированием активации ИЛ1бета, вызванного действием фермента каспаза1 и антигенами, компонентами комплемента, простагландином, тромбином и белками острой фазы воспаления.
В последнее время появились данные о том, что СрБ имеет самостоятельное патогенетическое значение в процессах атерогенеза и последующего тромбообразования, а не только является отражением системного воспаления, так как он связывается с ЛПНП, особенно с его модифицированными формами, и способен накапливаться в местах атеросклеротического поражения артерий, и в этом плане важное значение имеют профилактика и терапия острого коронарного синдрома гиполипидемическими препаратами. Последние наряду со снижением уровня ЛПНП улучшают свойства эндотелия, в том числе влияя на его защитные барьерные функции, в частности активизируя защитные функции эндотелиоцитов. Гиполипидемические препараты, как патогенетические эффективные средства, оказывают позитивное воздействие на окисленные ЛПНП, способны подавлять локальный синтез холестерина в сосудистой стенке, активизировать продукцию NO и цАМФ эндотелием, а также уменьшать оксидативный стресс по показателям снижения малонового диальдегида и повышать активность антиоксидантных ферментов, в частности каталазы [3].
В соответствии с рекомендациями Европейского общества кардиологов (2003) больным, перенесшим инфаркт миокарда, в качестве обязательной профилактики острого коронарного синдрома и в случае его проявлений в форме нестабильной стенокардии и повторного инфаркта миокарда как обязательное лечение требуется липидоснижающая терапия, в частности прием аториса по 10 мг/сут на протяжении 6 мес. Эффект этого препарата связан со снижением воспалительных процессов в атеросклеротических бляшках, улучшением эндотелиальной дисфункции, уменьшением активности протромботических факторов.
Важно придерживаться положений, одобренных в настоящее время международной кардиологической практикой [4]:
— Врачи общей практики назначают статины больным, перенесшим острый коронарный синдром.
— Больные склонны к постоянному лечению, если препараты назначаются им сразу после выписки из стационара.
— Терапия статинами не должна прерываться в период острого коронарного синдрома, а также не должно быть смены препарата или уменьшения его дозы.
— Сегодня решается вопрос о выборе конкретного препарата из группы статинов, особенно в случае отсутствия нарушений липидного обмена.
— Доза препарата не может быть ниже средней для лиц без нарушений липидного обмена (например, симвастатин 20 мг/сут) и должна быть высокой при наличии нарушений в липидном спектре.
— В настоящее время накоплено достаточно фактов для внедрения стандартов лечения острого коронарного синдрома в режиме раннего назначения статинотерапии как метода для ускоренной стабилизации критического поражения сосудов и системных иммунных и воспалительных реакций организма.
1. Мазуров В.И., Столов С.В., Линецкая И.Э. Динамика уровней провоспалительных цитокинов у больных в зависимости от различных форм ИБС // Клиническая медицина. — 1999. — № 11. — С. 2327.
2. Нетяженко В., Барна О. Керівництво до лікування пацієнтів зі стабільною стенокардією // АКК/АСС. — 2004. — № 10(87). — С. 1013.
3. Шумаков В.О. Сучасне уявлення про патогенез та лікування гострого коронарного синдрому // Нова медицина. — 2003. — № 4(9). — С. 3234.
4. Дзяк Г.В., Коваль О.А., Каплан П.А., Півняк А.Г. Запалення та імунопатологічні зміни при гострих коронарних синдромах: чи необхідна зміна стандартів терапії? // Нова медицина. — 2003. — № 4(9). — С. 2631.
5. Biasucci L.M., Liuzzo G., Grillo R.L. et al. Elevated levels of Creactive protein at dischage in pts with unstable angina predict recurrent instability // Circulation. — 1999. — 99. — 855860.
6. Hasdai D., Scheinowitz M., Leibovitz E. Increased serum concentration of interleukin1beta in pts with coronary artery disease // Heart. — 1996. — 76. — 2428.
7. Kanda T., Inoue M., Kotajima N. et al. Circulating interleukin6 and interleukin6 receptors in pts with acute and recent myocardial infarction // Cardiol.+ Ads. — 2008. — 93(3). — 191196.
8. Palmer J.N., Hartogenesis W.E. Patten M et al. Interleukin1 beta induces cardiac myocyte growth but inhibits cardiac // J. Clin. Invest. — 1995. — 95(6). — 25552564.
9. Vanderheden M., Kerschot E., Paulus W. Proinflamatory cytokines and endothelium dependent vasodilatation in the foream. Serial assessment in pts with congestive heart failure // Eur. Heart J. — 1998. — 19. — 747752.