Журнал «Актуальная инфектология» Том 7, №5-6, 2019
Вернуться к номеру
Гострий тонзилофарингіт у дітей. Сучасний стан проблеми
Авторы: Крамарьов С.О. (1), Євтушенко В.В. (1), Іванова Л.А. (2), Горбатюк І.Б. (2)
1 - Національний медичний університет імені О.О. Богомольця, м. Київ, Україна
2 - Буковинський державний медичний університет, м. Чернівці, Україна
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
Гострий тонзилофарингіт — одне з найпоширеніших інфекційних захворювань у дітей. Найбільш поширена вірусна етіологія. Серед бактеріальних причин основним збудником є Streptococcus pyogenes, або β-гемолітичний стрептокок групи A, що спричиняє близько 30 % епізодів. Дифтерія і некробацильоз нечасті, але пов’язані з тяжким перебігом захворювання. У процесі діагностики шкали клінічної оцінки можуть допомогти клініцистам краще прогнозувати підозрювану бактеріальну етіологію шляхом вибору пацієнтів. Використання алгоритмів діагностики може бути корисним для виявлення й скринінгу випадків, що не потребують антибіотикотерапії. Для лікування стрептококового тонзилофарингіту рекомендуються бета-лактамні антибіотики або макроліди. Правильна діагностика бактеріального тонзилофарингіту й правильне використання антибіотиків на основі наявних наукових даних мають вирішальне значення.
Острый тонзиллофарингит является одним из самих распространенных инфекционных заболеваний у детей. Наиболее распространена вирусная этиология. Среди бактериальных причин основным возбудителем является Streptococcus pyogenes, или β-гемолитический стрептококк группы A, который вызывает около 30 % эпизодов. Дифтерия и некробациллез нечасты, но ассоциируются с тяжелым течением заболевания. В процессе диагностики шкалы клинической оценки могут помочь клиницистам лучше прогнозировать предполагаемую бактериальную этиологию путем отбора пациентов. Использование алгоритмов диагностики может быть полезно для выявления и скрининга случаев, не требующих антибиотикотерапии. Бета-лактамные антибиотики или макролиды рекомендуются для лечения стрептококкового тонзиллофарингита. Правильная диагностика бактериального тонзиллофарингита и правильное использование антибиотиков на основе имеющихся научных данных имеют решающее значение.
Acute tonsillopharyngitis is one of the most common infectious diseases in children. Viral etiology is the most common. Among bacterial causes, the main causative agent is Streptococcus pyogenes or group A beta-hemolytic Streptococcus, which causes about 30 % of episodes. Diphtheria and necrobacillosis are infrequent but they are associated with severe course of disease. In the process of diagnosis, clinical evaluation scales can help clinicians better predict suspected bacterial etiology by selecting patients. The use of management algorithms may be useful for identifying and screening cases that do not require antibiotic therapy. Beta-lactam antibiotics or macrolides are recommended for the treatment of streptococcal tonsillopharyngitis. Proper diagnosis of bacterial tonsillopharyngitis and correct use of antibiotics based on available scientific evidence are crucial.
тонзилофарингіт; лікування; діти
тонзиллофарингит; лечение; дети
tonsillopharyngitis; treatment; children
Терміни «тонзиліт» і «фарингіт» використовують для визначення гострого запалення піднебінних мигдаликів або слизової оболонки глотки відповідно. З огляду на близьке анатомічне розташування й часте залучення до запального процесу обох структур одночасно в літературі й практичній діяльності також застосовується термін «тонзилофарингіт». Донедавна у вітчизняній літературі для визначення гострого запалення структур лімфоглоткового кільця також часто використовувався термін «ангіна». Гострий тонзилофарингіт належить до поширених інфекційних захворювань у педіатричній практиці й становить у структурі гострих респіраторних захворювань не менше ніж 15 % [1].
Етіологія
У переважній більшості випадків причиною гострого тонзилофарингіту є інфекційне ураження. Збудниками захворювання можуть бути віруси, бактеріальні патогени й гриби.
Вважається, що 50–80 % усіх випадків гострого тонзилофарингіту обумовлені вірусною етіологією [2]. З гострим тонзилофарингітом може асоціюватись широке коло вірусів, зокрема вірус Епштейна — Барр, риновірус, аденовірус, віруси грипу й парагрипу, віруси Коксакі, коронавірус, еховірус, цитомегаловірус та інші [3]. У більшості випадків клінічні симптоми гострого тонзилофарингіту є частиною більш широкого симптомокомплексу гострої респіраторної інфекції. Клінічна картина даних захворювань, як правило, неспецифічна, хоча для деяких інфекцій характерні специфічні симптоми.
При аденовірусній інфекції гострий тонзилофарингіт є доволі постійним симптомом. Інфекція частіше зустрічається серед дітей молодшого віку, але може викликати захворювання і в дорослих, а інколи стає причиною серйозних спалахів. З респіраторними захворюваннями зазвичай пов’язані типи аденовірусу 1, 2, 4, 5, 6, зрідка — 3 і 7. Підвищення захворюваності частіше реєструється в зимово-весняний сезон. Симптоматика захворювання, як правило, включає лихоманку, ринорею, кашель і біль у горлі. Тривалість гострого періоду, як правило, становить 3–5 днів. Було відзначено, що більшість тонзилітів асоціюється з 4-м серотипом аденовірусу. Типовим для аденовірусної інфекції є також залучення до запального процесу очей у вигляді кон’юнктивіту. Поєднання ураження очей і респіраторного тракту отримало назву синдрому фарингокон’юнктивальної лихоманки, що належить до найбільш відомих клінічних форм аденовірусної інфекції. Даний синдром частіше викликається серотипами 3, 4 і 7. Захворювання характерне для дітей шкільного віку. Випадки фарингокон’юнктивальної лихоманки можуть бути спорадичними, але трапляються й масові спалахи в дитячих колективах. Інкубаційний період зазвичай становить близько 5 днів. Початок захворювання гострий. При фарингоскопії на мигдаликах може виявлятись білуватий ексудат, а запальні зміни кон’юнктив зазвичай супроводжуються гіпертрофією лімфатичних фолікулів. Патогномонічною ознакою вважається збільшення пре–аурикулярних лімфатичних вузлів (синдром Паріно, Parinaud syndrome). Зрідка перебіг хвороби також може супроводжуватися висипанням на шкірі, діареєю і ускладнюватись енцефалітом. Гострий період захворювання триває близько 5 днів і, як правило, самостійно закінчується повним одужанням. Для аденовірусної інфекції характерна відносно тривала лихоманка, часто інфекція асоціюється з лейкоцитозом, істотним підвищенням швидкості осідання еритроцитів і рівня С-реактивного білка, що може спричиняти труднощі в диференціальній діагностиці з бактеріальними інфекціями [4].
Часто причиною тонзилофарингітів у дитячому віці є вірус Епштейна — Барр, зокрема гостра інфекція у вигляді інфекційного мононуклеозу (ІМ). Захворювання характеризується тріадою клінічних симптомів — лихоманка, тонзиліт/тонзилофарингіт, гепатоспленомегалія — і гематологічними змінами у вигляді лейкоцитозу з появою атипових мононуклеарів. На початку протягом 3–5 днів можуть спостерігатися продромальні явища у вигляді помірного головного болю, млявості. Потім з’являються основні клінічні прояви: лихоманка, біль у горлі, фарингіт, лімфаденопатія, гепатоспленомегалія, гепатит, висип на шкірі. Лихоманка звичайно триває протягом 5–10 днів, але може утримуватися 2 тижні та більше. Температура тіла здебільшого підвищується до 39–40 °С; проте в деяких дітей захворювання може перебігати при нормальній або субфебрильній температурі тіла. Біль у горлі є типовою ознакою ІМ. Під час огляду ротоглотки відмічається збільшення мигдаликів. Іноді мигдалики настільки збільшені, що дотикаються один до одного. Через ураження носоглоткового мигдалика відмічається утруднення носового дихання, здавленість голосу й дихання з хропінням. На мигдаликах у перші дні хвороби можуть з’явитися нашарування різної величини й характеру. Як правило, їх поява зумовлена активацією супутньої бактеріальної флори. Важливою ознакою ІМ є лімфаденопатія. Найбільш характерне збільшення шийних лімфовузлів. Лімфаденопатія може тривати від кількох днів до кількох тижнів і навіть місяців. Спленомегалія відмічається приблизно в 50 % хворих. Збільшення селезінки спостерігається частіше на 2–3-му тижні захворювання. Гепатомегалія відмічається в переважної більшості хворих. Максимальних розмірів печінка досягає на 4–10-й день захворювання. У 3–19 % хворих може спостерігатись висип на шкірі. Він з’являється в розпалі захворювання, переважно на тулубі й руках, тримається декілька днів, за характером може бути плямисто-папульозним (короподібним), дрібноточковим (скарлатиноподібним), еритематозним, уртикарним або геморагічним.
Ентеровірусна інфекція також може спричинювати своєрідне ураження глотки, що завдяки характерним симптомам отримало назву «герпангіна». Герпангіну можуть викликати різноманітні серотипи ентеровірусів, зокрема серотипи вірусів Коксакі (А1-А10, А16-А32, В1-В5), рідше еховіруси серотипів 3, 6, 9, 16, 17, 25 і 30. Здебільшого хворіють діти віком 3–10 років. Захворювання характеризується раптовим початком, швидким підвищенням температури тіла, болем у горлі, особливо під час прийому їжі й ковтання. Температура може підвищуватися до високих значень. Патогномонічним симптомом є поява на мигдаликах, м’якому піднебінні, задній стінці горла поодиноких, дрібних (1–2 мм) везикул або виразок, які протягом наступних 2–3 днів збільшуються і сягають розмірів 3–4 мм. У більшості випадків гострий період хвороби триває 1–4 дні, повністю симптоми зникають на 3-тю — 7-му добу.
Приблизно 30 % гострих тонзилофарингітів у дітей виникають унаслідок бактеріальної інфекції [1]. Серед бактеріальних збудників у багатьох випадках етіологічну роль відіграє бета-гемолітичний стрептокок групи А (БГСА). Рідше захворювання викликають Pneumococcus, Staphylococcus aureus, Haemophilus influenzae, Moraxella catarrhalis, Fusobacterium necrophorum, Streptococcus (групи B, C, G), Chlamydia pneumoniae, Corynebacterium diphtheriae, гриби (Candida albicans, Rhinosporidium, Cryptococcus, Histoplasma) [5].
Найбільш важливу роль серед бактеріальних збудників гострого тонзилофарингіту відіграють бета-гемолітичні стрептококи групи А. Бета-гемолітичний стрептокок (Streptococcus pyogenes) належить до патогенних мікроорганізмів. Важливість даного збудника з медичного погляду обумовлена не лише частотою випадків гострої інфекції, але й тим, що він може провокувати тяжкі імунопатологічні захворювання, такі як гостра ревматична лихоманка й постстрептококовий гломерулонефрит. Максимальна захворюваність на стрептококовий фарингіт спостерігається в дітей віком від 5 до 15 років, у яких на цей збудник припадає до 20 % і більше випадків гострого фарингіту. Стрептококовий фарингіт значно рідше зустрічається серед дітей перших 3 років життя й у дорослих. Інфекція може викликати спорадичні випадки захворювання, а може бути причиною спалахів у дитячих колективах. Клінічна картина гострого БГСА-тонзилофарингіту зазвичай характеризується болем у горлі, високою лихоманкою, головним болем, нудотою, блюванням, болями в животі, яскравою гіперемією мигдаликів і піднебінних дужок, а також задньої стінки глотки, гнійними нашаруваннями на мигдаликах, петехіальною висипкою на твердому піднебінні (енантема), збільшенням підщелепних лімфатичних вузлів, появою скарлатиноподібної висипки на шкірі, сезонністю захворювання в холодну пору року [6]. За результатами дослідження Nishiyama [7], найбільш сильну кореляцію з БГСА-етіологією в дітей демонструють такі симптоми, як висипка, набряк регіонарних лімфатичних вузлів, набряк мигдаликів і/або наявність нашарувань, відсутність кашлю, а також холодна пора року.
Іншою важливою бактеріальною інфекцією глотки є Fusobacterium necrophorum (некробацильоз). Є повідомлення, що за етіологічною роллю в структурі гострих тонзилофарингітів він не поступається навіть стрептококу [8]. Даний мікроб асоціюється з тяжкими паратонзилярними абсцесами й синдромом Лам’єра. Останній являє собою тяжке, часто смертельне, захворювання, що характеризується розвитком тромбофлебіту внутрішньої яремної вени внаслідок прогресування бактеріального фарингіту [9]. Захворювання, як правило, починається з лихоманки, що досягає 39–41 °C, і може супроводжуватись ознобом. Раннім симптомом є біль у горлі, що частіше з’являється за 4–5 днів до появи всіх інших симптомів. Клінічна картина в глотці неспецифічна й може варіювати від незначних катаральних змін до тяжкого ексудативного тонзиліту з порушенням ковтання. Як правило, має місце реакція лімфовузлів. Регіонарна лімфаденопатія може бути одно- чи двобічною і супроводжуватись больовими відчуттями в шиї. Інколи хворі також скаржаться на відчуття ущільнення в ділянці яремної вени. Розвиток тромбофлебіту супроводжується дисемінацією септичних тромбів у різні органи, зокрема в легені, дещо рідше — в суглоби, мозкові оболонки, кістки, печінку з розвитком вогнищевих уражень [10].
Розглядаючи бактеріальні причини гострого тонзилофарингіту, слід також згадати про можливість дифтерійної інфекції. Захворювання викликається грампозитивною бактерією Corynebacterium diphtheriae. Форма хвороби з ураженням глотки належить до найбільш частого варіанта перебігу інфекції в періоди епідемічного підйому. Після інкубаційного періоду, що зазвичай триває 2–5 днів, з’являються перші симптоми захворювання у вигляді неспецифічних проявів, які нагадують звичайну гостру респіраторну інфекцію. При фарингоскопії в цей період можна виявити катаральні явища й збільшення мигдаликів. Згодом дифузія токсинів дифтерійної палички призводить до фібринозного запалення з формуванням на поверхні мигдаликів характерних щільних нашарувань, які складно відділяються від підлеглих тканин епітелію. Ці нашарування можуть розташовуватись на мигдаликах, а можуть поширюватись також на оточуючі тканини. Характерним для дифтерії є розвиток набряку, який з мигдаликів поширюється на паратонзилярну клітковину, м’яке піднебіння і згодом сходить на шию і верхню частину грудної клітки. Без лікування у хворих прогресують токсичні ураження, зокрема міокардит, нейропатія, ураження нирок, коагуляційні розлади, порушення гемодинаміки [11]. Захворювання характеризується високою летальністю, що коливається в межах 5–10 % [12].
У більшості випадків гострі тонзилофарингіти являють собою захворювання зі сприятливим перебігом, що самостійно закінчуються одужанням. Проте в деяких випадках можливий розвиток небезпечних ускладнень. Звичайно тяжкий перебіг притаманний тонзилофарингітам бактеріальної природи. Окрім описаних вище специфічних ускладнень певних бактеріальних збудників захворювання може супроводжуватись розвитком епіглотиту. В етіології даного захворювання відіграють роль гемофільна паличка (типів A, F і нетипована), стрептокок групи А, золотистий стафілокок і менінгокок [13]. Епіглотит характеризується симптомами інтоксикації, порушенням ковтання, слинотечею і порушенням дихання внаслідок обструкції верхніх дихальних шляхів. Зазвичай захворювання прогресує дуже швидко і без адекватного лікування може призвести до асфіксії. Окрім ураження надгортанника може відбуватись поширення гнійного запалення на підслизову клітковину з формуванням абсцесів. Розвиток ретрофарингеального абсцесу супроводжується сильними больовими відчуттями в горлі й шиї. Як правило, для захворюванню характерні лихоманка, утруднене ковтання й порушення дихання. Локалізація процесу по задній поверхні глотки часто спричиняє проблеми для діагностики під час фізикального обстеження й потребує додаткових методів візуалізації [14]. Накопичення гнійного ексудату навколо мигдаликів призводить до розвитку паратонзилярних абсцесів. Захворювання зазвичай є ускладненням бактеріального фарингіту, хоча можливий розвиток симптомів одночасно з катаральними проявами в глотці. Паратонзилярний абсцес характеризується формуванням випинання в ділянці задньої дужки піднебінного мигдалика, що супроводжується зміщенням м’якого піднебіння і язичка в контралатеральний бік. Процес, як правило, однобічний, хоча також є повідомлення про білатеральне ураження [15].
Діагностика
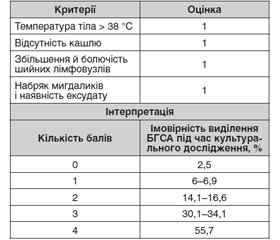
Для встановлення діагнозу гострого тонзилофарингіту зазвичай достатньо збору анамнезу й фізикального обстеження. Під час встановлення діагнозу найбільш важливим питанням стає оцінка ризику бактеріальної (зокрема, стрептококової) етіології захворювання. Для визначення ймовірності стрептококової етіології тонзилофарингіту під час клінічного обстеження створено декілька шкал. Серед них широкої популярності набула шкала Сентора (табл. 1).
Існують також модифікації даної шкали, що включають більше параметрів. Зокрема, у педіатричній практиці популярна шкала Мак-Айзека (McIsaac), що містить також віковий критерій (табл. 2) [16].
Серед додаткових обстежень, що можуть бути корисними для діагностики, можна виділити тести на стрептококову інфекцію. Це можуть бути як стандартні бактеріологічні методи, так і тести на антигени стрептококу, включно зі швидкими експрес-тестами. Дане обстеження може допомогти у визначенні етіологічної ролі бета-гемолітичного стрептококу групи А й призначенні адекватної терапії. На даний час обстеження на БГСА рекомендується проводити всім пацієнтам із високим ризиком стрептококового фарингіту за даними клінічного обстеження (3 або більше критерії шкали Сентора). За відсутності або при негативному результаті експрес-тесту показане бактеріологічне обстеження на стрептокок [17].
Бактеріологічне дослідження також відіграє важливу роль в уточненні діагнозу дифтерії. Хоча, як правило, лікувальна тактика при даній інфекції обумов–люється переважно клінічними симптомами. Загальні клінічні обстеження, такі як загальний аналіз крові з лейкограмою, можуть допомогти в діагностиці інфекційного мононуклеозу. Крім того, у підозрілих випадках є можливість провести тест на гетерофільні антитіла і/або визначення гострофазових антитіл класу М до збудників мононуклеозу. Рентгенографічні методи дослідження, у тому числі комп’ютерна томографія, застосовуються у випадках підозри на епіглотит або ретрофарингеальний абсцес, коли фізикальна діагностика пов’язана з труднощами [18].
Лікування
На даний час у світі опубліковано декілька нових настанов щодо лікування гострого тонзилофарингіту. Зокрема, це рекомендації National Institute for Health and Care Excellence «Sorethroat (acute): antimicrobial prescribing» (2018), Centers for Disease Control and Prevention «Pharyngitis (strepthroat)» (2018), Institute for Clinical Systems Improvement «Diagnosis and treatment of respiratory illness in children and adults» (2017). У даних настановах найбільше обговорюються питання обґрунтованого призначення антибактеріальних засобів. Це обумовлено проблемою широкого й не завжди раціонального використання антибіотиків, зростанням антибіотикорезистентності й ризиком ускладнень, асоційованих із прийомом антибіотиків. Зокрема, згідно із сучасними рекомендаціями, на даний час не рекомендується призначати антибактеріальні засоби у випадках, коли при об’єктивному огляді оцінка за шкалою Сентора становить 1 або 2 бали. У той же час при кількості балів за цією шкалою 3 або 4 слід розглядати призначення антибіотиків негайно або з відстрочкою на деякий час. Звичайно, у випадках підозри на септичний процес або за наявності симптомів гнійних ускладнень, таких як абсцеси, синдром Лам’єра, целюліт, антибіотикотерапія призначається негайно. У випадках підозри на дифтерію рекомендуються госпіталізація і лікування із застосуванням специфічної антитоксичної сироватки в комбінації з антибактеріальною терапією.
Щодо вибору антибактеріального засобу на даний час немає жорстких рекомендацій. Оскільки за результатами досліджень представники всіх основних груп антибіотиків, таких як пеніциліни, макроліди й цефалоспорини, продемонстрували схожу ефективність при бактеріальному тонзиліті, визначення оптимального засобу може базуватись на характеристиках безпеки, зручності прийому, даних фармакоекономіки [19].
Окремі сучасні рекомендації також наголошують на можливості застосування більш коротких курсів антибіотиків, ніж 10-денний прийом пеніциліну, за умови призначення більш сучасних антибактеріальних засобів [19]. Нижче наводяться основні лікарські засоби, що рекомендуються CDC [20] для лікування гострого стрептококового фарингіту (табл. 3).
Згідно з висновками експертної групи National Institute for Healthcare and Care Excellence (NICE), тонзилофарингіт є самообмежувальним захворюванням при задовільному самопочутті з покращанням стану пацієнта протягом тижня. Антибіотики слід використовувати в разі, якщо стан пацієнта поступово погіршується й не спостерігається покращання протягом 3–5 днів від початку захворювання. На сьогодні група експертів рекомендує використовувати клінічні шкали. При отриманні 0–2 балів рекомендована вичікувальна тактика.
Препаратом вибору є феноксиметилпеніцилін. На підставі даних доказів група рекомендує застосовувати дозування як двічі, так і чотири рази на добу за умови надання такої ж загальної добової дози. Альтернативним вибором антибіотика першого ряду є макроліди. При цьому вибір значною мірою повинен бути зумовлений мінімізацією ризику резистентності. Тривалість: курс застосування феноксиметилпеніциліну — 5–10 днів (довша терапія призначається у випадку рецидивуючих інфекцій). У разі застосування макролідів достатньо 5-денного курсу [19].
За даними кокранівського систематичного огля–ду, короткі курси азитроміцину (3–5 днів) при стрептококовому тонзилофарингіті в дітей мають високу ефективність, що не поступається такій у феноксиметилпеніциліну [21].
Азитроміцин є першим представником підкласу азалідів, що відрізняється за структурою від класичних макролідів. Він отриманий шляхом включення атома азоту в 14-членне лактонне кільце між 9-м і 10-м атомами вуглецю. Кільце перетворюється на 15-атомне, перестаючи при цьому бути лактонним. При введенні препарату (як всередину, так і парентерально) максимальна концентрація в крові досягається протягом 2–3 годин. Азитроміцин швидко розподіляється в тканинах організму, при цьому концентрація препарату в тканинах майже в 50 разів перевищує таку в плазмі крові. Біодоступність при прийомі всередину — 37 %, при внутрішньовенному введенні — до 50 %. Антибіотик добре проникає в тканини дихальних шляхів, сечостатевої системи, у шкіру та м’які тканини. Препарат має здатність накопичуватись у лейкоцитах (як у гранулоцитах, так і в моноцитах і макрофагах), що пояснює високу активність стосовно внутрішньоклітинних збудників [22]. Результати експериментальних і клінічних досліджень свідчать також, що макроліди, зокрема азитроміцин, мають протизапальну й імуномодулюючу дію [23]. Стимулюючий вплив на імунні й епітеліальні клітини включає взаємодію з фосфоліпідами й кіназою Erk1/2 (extracellular signal-regulated kinase) з наступною модуляцією транскрипції факторів AP-1 (activator protein-1), NFκB (nuclear factor kappa В), запальних цитокінів і продукції муцину [24].
Провідним виробником антибактеріальних препаратів в Україні є АТ «Київмедпрепарат» що входить до складу Корпорації «Артеріум». На фармацевтичний ринок України нею був випущений генеричний препарат, що містить азитроміцин, під торговою назвою Азимед®. Клінічні дослідження біоеквівалентності препаратів лінійки Азимед®, таблетки, вкриті плівковою оболонкою, 500 мг, порошок для пероральної суспензії 200 мг/5 мл у флаконі, пероральної суспензії 100 мг/5 мл у флаконі виробництва ПАТ «Київмедпрепарат» (Україна) і Сумамед® виробництва фірми Pliva (Хорватія) відповідних форм випуску були проведені на клінічній базі Національного фармацевтичного університету (НФаУ) в клініко-діагностичному центрі НФаУ.
Результатом проведеного дослідження стало те, що біоеквівалентність досліджуваних препаратів слід вважати встановленою. З точки зору доказової медицини біоеквівалентні препарати є взаємозамінними [25].
Основою лікування некробацильозу (синдром Лам’єра) також є антибіотикотерапія. Основними антибіотиками є бета-лактами, захищені від пеніцилінази молекулами сульбактаму або клавуланової кислоти, оскільки відомі факти резистентності даної бактерії до пеніцилінів через продукцію цього ферменту. Альтернативними препаратами можуть бути метронідазол і кліндаміцин. Курс антибіотикотерапії в середньому триває 6 тижнів [26]. У гострому періоді хвороби доцільне застосування парентерального шляху введення, а при покращенні стану можливий перехід на пероральний прийом препаратів. Оскільки синдром Лам’єра часто перебігає як сепсис із приєднанням інших мікроорганізмів, в антибіотикотерапії можуть призначатись комбіновані схеми лікування.
Серед інших напрямків лікування хворим із гострим тонзилофарингітом рекомендується забезпечувати адекватний прийом рідини для запобігання зневодненню. Для полегшення болю в горлі можливе застосування знеболювальних (парацетамол, ібупрофен) і місцевих засобів у вигляді спрея або льодяників із вмістом знеболювальних і/або антисептиків.
Конфлікт інтересів. Не заявлений.
1. Pediatric Pharyngitis: Background, Pathophysiology and Etiology, Epidemiology. URL: https://emedicine.medscape.com/article/967384-overview#a4 (Last accessed: 21.10.2019).
2. Wolford R., Schaefer T. Pharyngitis — StatPearls — NCBI Bookshelf. URL: https://www.ncbi.nlm.nih.gov/books/NBK519550 (Last accessed: 22.10.2019).
3. Regoli M., Chiappini E., Bonsignori F., Galli L., De Martino M. Update on the management of acute pharyngitis in children. Italian Journal of Pediatrics. 2011. Vol. 37.
4. Lion T. Adenovirus infections in immunocompetent and immunocompromised patients. Clin. Microbiol. Rev. 2014 Jul 1. 27(3). 441-62. URL: http://www.ncbi.nlm.nih.gov/pubmed/ 24982316 (Last accessed: 10.07.2017).
5. Kronman M.P., Zhou C., Mangione-Smith R. Bacterial Prevalence and Antimicrobial Prescribing Trends for Acute Respiratory Tract. Infections. Pediatrics. 2014 Oct 1. 134(4). e956-65. URL: http://www.ncbi.nlm.nih.gov/pubmed/25225144 (Last accessed: 03.03.2019).
6. Anjos L.M.M., Marcondes M.B., Lima M.F., Mondelli A.L., Okoshi M.P. Streptococcal acute pharyngitis. Rev. Soc. Bras Med. Trop. 2014 Jul 1. 47(4). 409-13.
7. Nishiyama M., Morioka I., Taniguchi-Ikeda M., Mori T., Tomioka K., Nakanishi K. et al. Clinical features predicting group A streptococcal pharyngitis in a Japanese paediatric primary emergency medical centre. J. Int. Med. Res. 2018 May 1. 46(5). 1791-800.
8. Van T.T., Cox L.M., Cox M.E., Bard J.D. Prevalence of fusobacterium necrophorum in children presenting with pharyngitis. J. Clin. Microbiol. 2017 Apr 1. 55(4). 1147-53.
9. Al Duwaiki S.M., Al Barwani A.S., Taif S. Lemierre’s syndrome. Oman Med. J. 2018. 33(6). 523-6.
10. Coultas J.A., Bodasing N., Horrocks P., Cadwgan A. Lemierre’s Syndrome: Recognising a Typical Presentation of a Rare Condition. Case Rep. Infect. Dis. 2015. 2015. 1-5.
11. Clinical manifestations, diagnosis, and treatment of diphtheria — UpToDate. URL: https://www.uptodate.com/contents/clinical-manifestations-diagnosis-and-treatment-of-diphtheria (Last accessed: 21.10.2019).
12. Diphtheria | Clinical Features | CDC. URL: https://www.cdc.gov/diphtheria/clinicians.html (Last accessed: 21.10.2019).
13. Epiglottitis (supraglottitis): Clinical features and diagnosis — UpToDate. URL: https://www.uptodate.com/contents/ epiglottitis-supraglottitis-clinical-features-and-diagnosis?search= pharyngitis children&topicRef=6457&source=see_link (Last accessed: 22.10.2019).
14. Jain H., Knorr T.L., Sinha V. Retropharyngeal Abscess. StatPearls. 2019. URL: http://www.ncbi.nlm.nih.gov/pubmed/ 28722903 (Last accessed: 22.10.2019)
15. Boon C., Wan Mohamad W.E., Mohamad I. Bilate–ral peritonsillar abscess: A rare emergency. Malaysian Fam. Рhysician: Off. J. Acad. Fam. Physicians Malaysia. 2018. 13(1). 41-4. URL: http://www.ncbi.nlm.nih.gov/pubmed/29796210 (Last accessed: 22.10.2019).
16. Fine A.M., Nizet V., Mandl K.D. Large-scale validation of the centor and mcisaac scores to predict group A streptococcal pharyngitis. Arch. Intern. Med. 2012 Jun 11. 172(11). 847-52.
17. Short S., Bashir H., Marshall P., Miller N., Olmschenk D., Prigge K. et al. Respiratory Illness in Children and Adults, Diagnosis and Treatment of | ICSI. Institute for Clinical Systems Improvement, 2017. URL: https://www.icsi.org/guideline/respiratory-illness (Last accessed: 22.10.2019).
18. Shulman S.T., Bisno A.L., Clegg H.W., Gerber M.А., Kaplan E.L., Lee G. et al. PSPED — INFECT — LG — IDSA pharyngitis 2012. Clin. Infect. Dis. 2012 Nov. 55(10). e86-102. URL: http://www.ncbi.nlm.nih.gov/pubmed/22965026 (Last accessed: 22.10.2019).
19. Overview | Sore throat (acute): antimicrobial prescribing | Guidance | NICE. 2018. URL: https://www.nice.org.uk/gui–dance/ng84 (Last accessed: 22.10.2019).
20. Group A Strep | Strep Throat | For Clinicians | GAS | CDC. URL: https://www.cdc.gov/groupastrep/diseases-hcp/strep-throat.html (Last accessed: 23.10.2019).
21. Altamimi S., Khalil A., Khalaiwi K.A., Milner R.A., Pusic M.V., Al Othman M.A. Short versus standard duration antibiotic therapy for acute streptococcal pharyngitis in children. Altamimi S., editor. Cochrane Database of Systematic Reviews. Chichester, UK: John Wiley & Sons, Ltd, 2009. URL: http://doi.wiley.com/10.1002/14651858.CD004872.pub2 (Last accessed: 24.10.2019).
22. Drugs.com. Azithromycin Uses, Dosage & Side Effects. URL: https://www.drugs.com/azithromycin.html (Last accessed: 25.02.2019).
23. McMullan B.K., Mostaghim M. Prescribing azithromycin. Aust. Prescr. 2015 Jun 1. 38(3). 87-9. URL: https://www.nps.org.au/australian-prescriber/magazine/38/3/87/9 (Last accessed: 23.04.2018).
24. Parnham M.J., Haber V.E., Giamarellos-Bourboulis E.J., Perletti G., Verleden G.M., Vos R. Azithromycin: Mechanisms of action and their relevance for clinical applications. Pharmacol. Ther. 2014 Aug 1. 143(2). 225-45. URL: https://www.sciencedirect.com/science/article/pii/S0163725814000552?via%3Dihub (Last accessed: 25.04.2018).
25. Зупанец И., Безуглая Н., Либина В., Орлова И., Кудрис И., Кувайсков Ю. Оценка взаимозаменяемости Азимеда — биоэквивалентность доказана! Ліки України. 2013. 1(167). 80-3.
26. Allen B., Bentley T. Lemierre Syndrome — StatPearls — NCBI Bookshelf. URL: https://www.ncbi.nlm.nih.gov/books/NBK499846 (Last accessed: 23.10.2019).

/239-1.jpg)
/239-2.jpg)
/240-1.jpg)