Септичний шок (СШ) у дітей, попри наочні досягнення останніх років, лишається поширеним критичним станом, що нерідко закінчується летально. Імовірність настання летального наслідку визначається переважно розвитком поліорганної недостатності або рефрактерних гемодинамічних порушень. Діти, які мешкають у країнах із низьким рівнем доходів, також є дуже вразливою для сепсису популяцією. Попри значну кількість ініціатив щодо покращання діагностики та раннього лікування сепсису в дітей, летальність лишається високою — у межах 40 % [1]. Незадовільні результати в той же час більшою мірою залежать не від обмеженості ресурсів, а від затримки з розпізнаванням та раннім лікуванням сепсису. У розвинених країнах летальність при СШ у дітей залишається достатньо високою. Разом із тим у США летальність від СШ у дітей протягом останніх років знизилась до 8,9 %, що певною мірою пов’язується з удосконаленням алгоритмів невідкладної допомоги та інтенсивної терапії (ІТ) [2]. Одним із провідних напрямків ІТ СШ у дітей є гемодинамічна підтримка, що суттєво відрізняється від такої в дорослих пацієнтів. Існує певна кількість повідомлень щодо її впливу на наслідки при СШ. Наприклад, у ретроспективному дослідженні продемонстроване значуще зростання летальності в дітей із менінгококовим CШ, яке пов’язане з призначенням неадекватної інотропної підтримки (OR 23,7, 95% CI 2,6–213, p = 0,005) [3]. Отже, своєчасна та адекватна гемодинамічна підтримка є одним із фундаментальних напрямків ІТ СШ. Вона активно обговорюється у світових виданнях та, попри суттєвий прогрес, викликає значну кількість складних запитань та істотно контроверсійних рекомендацій. На жаль, вітчизняна ІТ певною мірою лишається осторонь цієї дискусії через недосконалість доступного гемодинамічного моніторингу та недоступність для лікувальних установ цілої низки препаратів, які згадуються в провідних зарубіжних рекомендаціях. Зважаючи на це, ми хотіли би привернути увагу медичного суспільства до цієї проблеми та зробити певні теоретичні обґрунтування щодо оптимальних підходів для гемодинамічної під–тримки в умовах вітчизняних відділень інтенсивної терапії.
Особливості гемодинамічних розладів при СШ у дітей та їх відмінність від гемодинамічних розладів у дорослих
Традиційні погляди на гемодинамічні розлади при СШ у дітей полягають у визнанні їх головним чинником гіповолемії. Відомими роботами було продемонстровано ефективність агресивної волемічної підтримки при СШ у дітей. Також було показано, що летальні наслідки в дітей асоціюються з низьким серцевим викидом (СВ) [4, 5]. Натомість у дорослих переважним механізмом СШ, що суттєво впливає на летальність, є неконтрольована вазоплегія [6]. Крім того, у дорослих спостерігається систолічна дисфункція лівого шлуночка, яка проявляється зменшенням фракції викиду, але СВ підтримується за рахунок тахікардії та дилатації шлуночків серця. Низкою досліджень було показано, що відсутність цих компенсаторних реакцій у дорослих супроводжується поганим прогнозом при СШ [7, 8]. Таким чином, одним із терапевтичних напрямків лікування СШ у дітей, що може сприяти покращанню наслідків, є підтримка серцевого індексу (CІ) у межах 3,3–6,0 л/хв/м2 [9, 10]. Дуже важливим є визнання того факту, що в дітей на відміну від дорослих головним чинником адекватного споживання кисню (VO2) є його висока доставка, але не екстракція, тому цільовим показником VO2 при СШ у дітей є значення понад 200 мл/хв/м2, що також може бути пов’язано з покращанням наслідків [9].
Надзвичайно цінними для розуміння гемодинамічних розладів при СШ у дітей були результати відомої роботи Ceneviva et al. (1998), в якій було проаналізовано стан гемодинаміки в 50 дітей із рідинно-рефрактерним, допамінрезистентним СШ. З’ясувалося, що в більшості (58 %) дітей був низький СВ/високий загальний периферичний судинний опір (ЗПСО), а у 22 % — низький СВ та низький ЗПСО. Лише у 20 % дітей гемодинамічні розлади відповідали профілю «високий СВ/низький ЗПСО» [10]. Також дуже корисним було спостереження, яке показало, що гемодинамічний профіль протягом перших 48 годин може змінюватися. Персистенція СШ була відзначена в третини пацієнтів. Хоча в більшості хворих із персистенцією СШ спостерігалася тенденція до зниження серцевого викиду, що потребувало інфузії інотропів та вазодилататорів, у певної кількості пацієнтів стан гемодинаміки трансформувався у високий СВ/низький ЗПСО. Пізніше в дослідженні із застосуванням моніторингу гемодинаміки методом ультразвукової допплерометрії було показано, що в дітей із позагоспітальним розвитком СШ частіше спостерігається низький СВ, який асоціюється з більшою смертністю, тоді як при госпітальному, катетерасоційованому СШ із високим СВ смертність була нижчою [5].
Варто відзначити, що в доступній нам літературі містяться результати досліджень переважно систолічної функції лівого шлуночка (ЛШ), тоді як діастолічна функція при септичних станах досліджена значно менше. Між тим існують деякі теоретичні передумови, які дають можливість прогнозувати наявність не лише систолічної, але і діастолічної дисфункції (ДД) ЛШ. Певна кількість досліджень підтверджує наявність ДД міокарда в дорослих хворих на СШ [11–13]. Серед можливих чинників ДД варто відзначити: ішемію міокарда, скорочення часу діастоли через тахікардію, електролітні розлади та синдром капілярного витоку, розлади споживання міокардом ацильних фрагментів через ушкодження карнітинового човника та деякі інші фактори [8, 14, 15]. Також наочним є той факт, що тривалість діастоли та кінцево-діастолічний тиск є факторами, що лімітують кровопостачання ЛШ, що, зі свого боку, забезпечує кисневий баланс та ефективність роботи ЛШ в умовах підвищеної гемодинамічної потреби [16].
Не менш важливим, але таким, що часто лишається поза увагою, є стан кровообігу в малому колі та правих відділах серця. СШ нерідко супроводжується розвитком легеневої гіпертензії (ЛГ) із збільшенням легеневого судинного опору, що утруднює роботу правого шлуночка [17]. У низці досліджень установлено залежність між фракцією викиду правого шлуночка і легеневим судинним опором та наслідком при септичних станах [17, 18]. Через механізм бівентрикулярного феномена ЛГ суттєво впливає на роботу лівих відділів серця, зменшуючи викид із ЛШ та викликаючи системні гемодинамічні розлади і циркуляторну гіпоксію, які здатні утворити порочне коло і збільшити ЛГ. Отже, некомпенсована правошлуночкова недостатність внаслідок ЛГ та вторинне ушкодження циркуляції у великому колі кровообігу є важливими факторами пато- та –танатогенезу при СШ [18].
Проте аналіз гемодинамічних розладів був би неповним, якщо ми залишимо неописаним стан мікроциркуляції та її розладів, тобто мікроциркуляторний дистрес. Морфологічним субстратом мікроциркуляторного дистресу є взаємодія між судинним ендотелієм та активованими нейтрофілами, що відбувається в межах розвитку системної запальної відповіді. При СШ патологічні зміни стосуються всіх компонентів мікроциркуляторного русла. В артеріолах розвивається вазодилатація та знижується їх чутливість до вазопресорів, у капілярах спостерігається розвиток ендотеліальної дисфункції та мікротромбоутворення; у венулах — адгезія й агрегація активованих імунокомпетентних клітин [19]. Що ж саме відбувається з тканинною оксигенацією за таких змін мікроциркуляторного русла? На сього–дні описано п’ять типів тканинного кровотоку при критичних станах [20]. Кровотік при СШ характеризується гетерогенністю, тобто окремі капіляри не перфузуються або майже не перфузуються (stop flow), у них не відбувається газообмін, тобто виникає локальна ішемія. Натомість інші отримують ту частку кровопостачання, що не потрапила в капіляри з припиненим кровотоком. Але в цих капілярах екстракція кисню не зростає, адже в тканинах поруч із ними гіпоксії/ішемії немає. Отже, утворюється шунт, за умов якого сатурація змішаної венозної крові залишається нормальною або навіть зростає! Відповідно, гіпоксія залишається не розпізнаною і викликає ушкодження органів та розвиток синдрому поліорганної недостатності. Ще гірша ситуація відбувається в разі поєднання гетерогенності крово–току та зниження загального об’єму кровотоку (низький СВ), адже тяжкість гіпоксії подвоюється [21]. Важливо відзначити, що на відміну від несептичних критичних станів гетерогенність кровотоку при СШ виникає незалежно від показників серцевого викиду й артеріального тиску (АТ).
De Backer et al. (2002) показали, що у хворих із тяжким сепсисом кількість мікросудин, що перфузуються, вірогідно нижча порівняно зі здоровими волонтерами [22]. Підкреслюється, що навіть при гіпердинамічному СШ у печінці, слизовій кишечника, діафрагмі, скелетних м’язах виникає гіпоперфузія. Експериментальними та клінічними дослідженнями продемонстровано, що уповільнення кровотоку в мікросудинах не усувається після рідинної ресусцитації і викликає порушення споживання кисню [23]. В експериментальних моделях СШ за відсутності глобальних гемодинамічних зрушень та артеріальної гіпотонії виявляються зниження швидкості мікроциркуляторного потоку крові, утворення капілярів із зупиненим кровотоком, зростання гетерогенності кровотоку та зниження щільності капілярів. Отже, саме мікроциркуляторні розлади при СШ спричиняють розвиток тканинної гіпоксії та синдрому поліорганної недостатності і мають усуватися ІТ [19].
Клінічні та гемодинамічні ознаки СШ у дітей, які можуть бути використаними для його діагностики та ІТ
В останній редакції American College of Critical Care Medicine (ACCM) Guidelines (2017) з лікування СШ у дітей міститься висновок комітету авторів відносно того, що визначати СШ необхідно за клінічними, гемодинамічними змінами та змінами в споживанні кисню [24].
Також автори зазначають, що ідеал діагностики СШ у дітей базується на визначенні клінічних симптомів, які включають гіпотермію або гіпертермію, зміни ментального статусу та периферичну вазодилатацію (теплий шок) або вазоконстрикцію з часом заповнення капілярів понад 2 с (холодний шок). Ця діагностика має відбуватися до виникнення артеріальної гіпотонії!
Крім клінічних ознак, при СШ необхідно оцінювати показники гемодинаміки, серед яких найбільш важливими є перфузійний тиск (ПТ) (ПТ = САТ – ЦВТ) та СВ. Цільові значення ПТ визначаються за формулою: ПТ = 55 + вік (роки) × 1,5 [24]. Відповідно до закону Ома в системі кровообігу потік крові (Q) є прямо пропорційним перфузійному тиску (∆P), тобто градієнту тиску на вході та виході із системи циркуляції та обернено пропор–ційним — опору (R). Ця закономірність виражається рівнянням Q = ∆P/R. Якщо в це рівняння підставити клінічно доступні показники гемодинаміки, то ми отримаємо таку формулу: CВ = САТ – ЦВТ/ЗПСО. Саме це співвідношення є визначним для перфузії. Кровообіг усіх внутрішніх органів або прямо залежить від перфузійного тиску, або має авторегуляцію кровотоку в певних межах САТ (наприклад, голов–ний мозок та серце). За умов, коли перфузійний тиск знижується та виходить за межі авторегуляції, кровопостачання органів критично знижується. Відповідно до вищенаведених формул такий стан розвивається внаслідок зменшення САТ та/або збільшення ЦВТ [24].
Саме тому підтримка адекватного до віку дитини ПТ є важливою метою при проведенні ІТ СШ. Дуже повчальним є результат дослідження R. Kumar еt al. (2014), у якому було продемонстрована здатність ІТ, спрямованої на підтримку церебрального перфузійного тиску, знижувати летальність на 20 % у хворих із тяжкими інфекціями центральної нервової системи порівняно з терапією, що мала на меті підтримку внутрішньочерепного тиску [25]. Також добре відомим є факт позитивного впливу інфузії нор–епінефрину на діурез та кліренс креатиніну у хворих на гіпо–тензивний СШ [26].
В ACCM Guidelines (2017) з лікування СШ у дітей також було привернуто увагу до дуже важливого аспекту гемодинамічних розладів при СШ в окремій групі пацієнтів, а саме пацієнтів із синдромом внутрішньоабдомінальної гіпертензії або абдомінальним компартмент-синдромом. Для перфузії органів абдомінальної порожнини та заочеревинного простору критичною умовою адекватної перфузії є внутрішньоабдомінальний тиск (ВАТ), який не перевищує ЦВТ. Якщо ця умова не виконується, то ПТ органів черевної порожнини буде дорівнювати різниці між САТ та ВАТ [24]. Такий стан може виникати при асциті, набряку стінки кишечника та запускає порочне коло: ішемія — набряк — збільшення ВАТ — ішемія — набряк... Тобто, якщо збільшення ВАТ не компенсується зростанням САТ, спланхнічний перфузійний тиск знижується. Внутрішньоабдомінальною гіпертензією вважається збільшення ВАТ > 12 мм рт.ст. Виділяють 4 ступені інтраабдомінальної гіпертензії: І ступінь — 12–15 мм рт.ст.; ІІ — 16–20 мм рт.ст.; ІІІ — 21–25 мм рт.ст.; IV — понад 25 мм рт.ст. Доречно нагадати, що підвищений ВАТ вважають одним із можливих чинників катехоламінрезистентного СШ [24].
Але повернемося до АТ та СВ. Згідно із законом Ома в системі кровообігу АТ залежить від СВ та ЗПСО, отже може змінюватися під впливом цих показників. Саме тому, крім моніторингу САТ, що, до речі, рекомендують здійснювати інвазивним методом (що майже не використовують в умовах вітчизняних ВІТ) також рекомендується визначати СВ або кровотік у верхній порожнистій вені [24].
Крім того, кровотік в органах та тканинах залежить не лише від ПТ, але й від судинного опору. За умов адекватної систолічної функції шлуночків серця збільшення ЗПСО призводить до збільшення АТ при збереженому СВ, але за умов розвитку систолічної дисфункції нормальний АТ зі збільшеним ЗПСО відповідає зменшенню СВ. Отже, підвищення ЗПСО супроводжується зниженням кровотоку та розвитком шоку. Показано, що підтримання CІ у межах 3,3–6,0 л/хв/м2 асоціюється з покращанням результатів лікування в пацієнтів із СШ [5, 9]. Підтримання такого високого СІ нерідко може бути забезпечено лише за рахунок збільшення частоти серцевих скорочень (ЧСС). Проте надмірна ЧСС викликає зменшення часу діастоли, а отже, редукцію коронарного кровотоку в лівому шлуночку, який має перфузію лише під час діастоли. Перфузія коронарних артерій також зменшується через зниження діастолічного артеріального тиску (АТд), що є дуже специфічним для СШ, та/або високого рівня кінцево-діастолічного тиску у лівому шлуночку. Остання проблема виникає через збільшення жорсткості шлуночка, тобто через діастолічну дисфункцію.
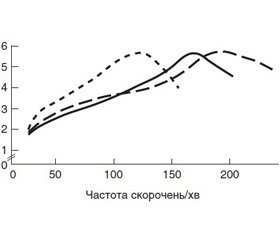
Одним із традиційних показників ефективності одного серцевого циклу вважається ударний об’єм (УО). Досягнення адекватних значень цього показника є одним із напрямків впливу на СВ, адже CВ = ЧСС × УО. У зв’язку з цим необхідно нагадати, що терапія, що спрямована на збільшення УО, часто рефлекторно зменшує ЧСС та покращує СВ. Також важливо пам’ятати, що діти мають обмежений резерв ЧСС порівняно з дорослими, тому що в них від початку ЧСС є високою. Наприклад, якщо УО знижується через викликану ендотоксином дисфункцію серця, доросла людина може компенсувати зменшення УО шляхом збільшення ЧСС у два рази — від 70 до 140 уд/хв, але в дитини не може збільшуватися ЧСС із 140 до 280 уд/хв, зазначається в ACCM Guidelines (2017) із лікування СШ у дітей [24]. Також зазначається, що, хоча тахікардія є важливим інструментом підтримання СВ у немовлят та дітей, вплив віку дитини реалізується таким чином, що чим дитина молодша, тим більше імовірно, що відповідь буде неадекватна та СВ знизиться. У такому разі компенсаторна відповідь на зниження СВ та скоротливої здібності ЛШ має звужувати судини для підтримання АТ. Підвищений судинний опір клінічно проявляється відсутністю або ослабленням периферичного пульсу, холодними кінцівками, тривалим часом заповнення капілярів та низьким пульсовим тиском із непропорційно збільшеним діастолічним тиском. У такому разі найбільш доцільним є використання вазодилататорів та додаткове навантаження рідиною відповідно до збільшення судинної ємності. Така терапія дає можливість краще наповнювати шлуночки серця при меншому тиску, сприяє збільшенню кінцево-діастолічного об’єму та СВ на тлі зменшення тахікардії.
/22-1.jpg)
З іншого боку, необхідно підтримувати ЧСС на рівні, що забезпечує максимальний СВ, адже CВ = ЧСС × УО.
Підтримка ЧСС забезпечується препаратом, що має позитивну інотропну та хронотропну дію. Також радять звертати увагу на АТд як важливий чинник коронарної перфузії. Якщо різниця між АТд та ЦВТ надто низька, то для покращання коронарного кровообігу під час діастоли доцільно додати норепінефрин. Навпаки, якщо в ЛШ хворого надмірний кінцево-діастолічний тиск, що можливе за умов рідинного перевантаження, то для покращання СВ може бути необхідним діуретик, який зсуне вліво криву Франка — Старлінга.
Таким чином, ми можемо дійти висновку, що високоефективна ІТ СШ у дітей базується на мультимодальному моніторингу, який має на меті постійну оцінку переднавантаження, післянавантаження, артеріального та перфузійного тиску, серцевого викиду та систолічної функції лівого шлуночка. Корисно додати до цього переліку показників оцінку стану перфузії/мікроциркуляції, легеневого кровотоку та діастолічної функції шлуночків. На жаль, технічне забезпечення вітчизняних відділень інтенсивної терапії дозволяє моніторинг лише вкрай обмеженого переліку гемодинамічних показників, який не відповідає навіть рекомендаціям щодо ІТ СШ у дітей у країнах з обмеженими ресурсами! [28] Отже, провідними орієнтирами для ІТ лишаються клінічні (стан перфузії, колір шкіри, діурез) та найпростіші інструментальні (артеріальний та центральний венозний тиск, ЧСС) показники. З огляду на реальний стан матеріально-технічного забезпечення вітчизняних установ охорони здоров’я ми хотіли б порадити максимально широко застосовувати приліжкову ультразвукову діагностику, яка може частково усунути дефіцит необхідної для ІТ СШ інформації [29].
Інотропні та вазоактивні засоби для підтримки гемодинаміки при СШ
На початку обговорення питання щодо застосування інотропних препаратів нагадаємо читачеві, що коло препаратів, які далі будуть обговорюватися, мають різноманітні механізми впливу на серцево-судинну систему. Їх використання завжди має бути цілеспрямованим та обґрунтованим клінічними та/або інструментальними оцінками типу розладів гемодинаміки, які можуть змінюватися протягом ІТ та потребувати відповідної корекції доз та комбінацій препаратів. За своїми характеристиками всі обговорювані засоби можуть визначатися як: вазопресори (норепінефрин, вазопресин, терліпресин, ангіотензин), вазодилататори (нітрати, нітропрусид натрію, L-аргінін), препарати з інотропною дією (добутамін) та препарати, які мають різноманітні впливи на серцево-судинну систему. Наприклад, допамін, епінефрин — інотропна, хронотропна, вазопресорна дія залежно від дози, інгібітори фосфодіестерази, кальцієві сенситизатори — інодилататори. Також варто звернути увагу на те, що у хворих на СШ через можливі розлади функції органів, які впливають на фармакокінетику та фармакодинаміку (нирки, печінка), тяжкий ацидоз, очікуваний клінічний ефект препаратів може значно відрізнятися від клінічного результату. Таким чином, дози, які рекомендовані для застосування, можуть розглядатися лише як початкові, орієнтовні дози для стартової терапії, які потребують переоцінки на підставі клінічної відповіді. Тому важливо розуміти необхідність безперервного моніторингу й оцінки показників переднавантаження, скоротливої здатності міокарда, серцевого викиду та післянавантаження для адекватного визначення доз, комбінацій препаратів та рідинної терапії.
Препарати для інотропної підтримки
Класичним та найбільш поширеним засобом для інотропної підтримки є допамін, що використовується в діапазоні доз (5–9 мкг/кг/хв). Допамін тривалий час вважався препаратом вибору для лікування рідинно-рефрактерного шоку в дітей [30, 31]. У пацієнтів із СШ допамін підвищує СІ, індекси ударної роботи лівого та правого шлуночків серця. Допамін має і низку суттєвих недоліків, а саме зниження ефективності на тлі ацидозу та в дітей першого року життя, негативний вплив на рівень пролактину, соматотропного гормона, тиреоїдних гормонів, і справляє катаболічну дію [32]. Навіть у дозах нижчих за 5 мкг/кг/хв він погіршує ниркову та спланхнічну перфузію, функціональний стан нирок та шлунково-кишкового тракту [33, 34]. Отже, не дивно, що в мультицентровому дослідженні, присвяченому ІТ СШ у дорослих, продемонстровано, що допамін збільшує госпітальну летальність у хворих на СШ на 8,2 %, а летальність у відділеннях інтенсивної терапії — на 7,2 % [35]. Пізніше в ретроспективному дослідженні, що було основане на аналізі бази даних, до якої увійшли 1050 дітей із СШ, які потребували інотропної/вазопресорної підтримки, було показано, що госпітальна летальність у хворих, які отримували інфузію допаміну, становила 53,8 %, добутаміну — 29,4 %, допаміну з добутаміном — 50 %, добутаміну з норадреналіном — 25 %. Загальна госпітальна летальність у хворих, які отримували допамін або комбіновану підтримку з допаміном, становила 66 %, якщо застосовувалися інші препарати, вона — лише 34 % [36].
Добутамін — β1-агоніст з інотропною дією. Кілька досліджень вивчали вплив добутаміну на функцію серця при сепсисі або СШ у дозі від 2 до 28 мкг/кг/хв. У більшості робіт підвищення СІ варіювало від 20 до 66 %. Проте ЧСС часто значно підвищувалася. Індекс ударної роботи лівого шлуночка підвищується на 23–37 % при середній дозі добутаміну від 5 до 12 мкг/кг/хв [37, 38]. Існують відомості про здатність добутаміну покращувати спланхнічну перфузію та збільшувати споживання кисню [39]. Через можливість зниження АТ при СШ вважається доцільним застосування добутаміну в поєднанні з норадреналіном або іншими симпатоміметиками [40].
Отже, з урахуванням того факту, що рідинно-рефрактерний шок у дітей найчастіше обумовлений збереженням низького СІ і переважною потребою в ефективній інотропній дії без небажаних сторонніх впливів, добутамін виглядає більш привабливим препаратом, ніж допамін. Допамін та добутамін можуть бути безпечно застосовані в периферичну вену.
Добутамін-допамін-рефрактерний СШ із низьким СВ можна ефективно лікувати за допомогою інфузії епінефрину (адреналiну) [41, 42]. Епінефрин у дітей використовують частіше, ніж у дорослих. Стартова iнотропна підтримка епiнефрином дозою 0,1–0,3 мкг/кг/хв є прийнятною альтернативою допаміну при СШ у дітей, та навіть сприяє зменшенню летальності при холодному гіподинамічному СШ [43]. Це обумовлено потужною інотропною та хронотропною дією епінефрину, що не залежить від віку та кислотно-основного стану. При низьких дозах (≤ 0,3 мкг/кг/хв) епінефрин має переважно β2-адренергічний ефект, збільшує СВ та, відповідно, знижує ЗПСО, покращує кровообіг у скелетних м’язах та шкірі. В низьких дозах епінефрин також покращує інтрамуральний рН слизової шлунка. У той самий час епінефрин здійснює суттєвий вплив на вуглеводний обмін через стимуляцію глюконеогенезу та глікогенолізу, контрінсулярну дію, чим спричиняє розвиток гіперглікемії. Епінефрин також може впливати на рівень лактату, що ускладнює інтерпретацію цього показника в дітей із СШ. Збільшення дози епінефрину понад 0,3 мкг/кг/хв супроводжується зростанням альфа-адренергічних ефектів, вазоконстрикцією, пресорною дією та погіршенням периферичного кровотоку [24]. Для безпечної інфузії епінефрину необхідно використання центрального венозного доступу, але за життєвими показаннями в критичній ситуації він може нетривалий час вводитися в периферичну вену або внутрішньокістково до забезпечення центрального венозного доступу [41]. При екстравазації епінефрину його дія може бути усунута антагоністами адренергічних рецепторів (фентоламін) [24].
Вазодилататори
Вазодилататори при СШ у дітей показані за умов низького СВ та нормотензії, що забезпечується високим ЗПСО, за умов відсутності ефекту від попереднього призначення добутаміну або низьких доз епінефрину. Вибір вазодилататорів короткої дії обмежується нітропрусидом натрію або нітрогліцерином, які продемонстрували здатність покращувати мікроциркуляцію при СШ у разі додання до інфузії інотропних препаратів [44]. Дозу вазодилататорів необхідно титрувати до досягнення бажаного ефекту під контролем САТ. Нітрати небезпечні у хворих із тяжкою внутрішньочерепною гіпертензією, а нітропрусид натрію — при зниженні ниркової функції, що певною мірою обмежує коло пацієнтів, у яких вони можуть бути застосовані. Також існують окремі повідомлення про застосування інших вазодилататорів, а саме простацикліну, пентоксифіліну, допексаміну та фенолдопаму.
Крім класичних вазодилататорів, при СШ у дітей використовувалися так звані інодилататори — препарати з групи інгібіторів фосфодіестерази III типу (ІФ), які одночасно забезпечують ізотропну, вазодилатуючу та люсотропну дію [45, 46]. Вони представлені трьома засобами: інамриноном, мілриноном та еноксимоном, які стимулюють збільшення внутрішньоклітинного циклічного аденозинмонофосфату (цАМФ) через запобігання його гідролізу. Дія ІФ не залежить від функціонального стану β-адренорецепторів, і вона синергічна до β-агоністів. Застосування інамринону обмежене у хворих із печінковою недостатністю, а мілринону — у хворих із нирковою недостатністю. Вазодилатація, що виникає після початку лікування ІФ, може змусити призначити додаткову інфузію рідини для підтримки стабільного АТ. Через тривалий час напіввиведення призначення ІФ необхідно припиняти при перших симптомах аритмії та/або артеріальної гіпотензії. Останню, крім додаткової інфузії, можна усунути титруванням норепінефрину, який через стимуляцію альфа-адренорецепторів протидіє впливу цАМФ. Еноксимон через особливості впливу на цАМФ має значно менший ризик гіпотонії при ефективному покращанні функції серця. Кількома дослідженнями було продемонстровано, що ІФ здатні значно та позитивно змінити наслідки катехоламінрефрактерного СШ у дітей. На жаль, мусимо зазначити, що жоден препарат із групи ІФ в Україні не зареєстрований, що не сприяє раціональній гемодинамічній підтримці у хворих на СШ.
Група сенситизаторів кальцію представлена єдиним засобом левосименданом, який збільшує чутливість комплексів «актин — тропоміозин» до кальцію та має властивості ІФ III типу. Через те, що одним із патогенетичних механізмів дисфункції серця при сепсисі є зменшення чутливості до кальцію комплексів «актин — тропоміозин», застосування цього засобу у хворих із СШ має фундаментальні підстави [47–49]. Окремі дослідження свідчать про здатність левосимендану збільшувати СІ та усувати прояви кардіальної дисфункції, покращувати мікроциркуляцію в дорослих із СШ [50]. На жаль, у єдиному порівняльному дослідженні левосимендан не продемонстрував при СШ більшої ефективності, ніж добутамін [51]. Широкому використанню цього препарату в дітей із СШ в Україні також заважає його висока вартість.
Вазопресори
Вазопресори також посідають своє місце в ІТ СШ у дітей, хоча значно частіше їх викори–стовують при СШ у дорослих. Головною метою застосування вазопресорів є підтримання САТ та, відповідно ПТ, що здебільшого показано при високому СВ/низькому ЗПСО. Збільшення ПТ сприяє оптимальному діурезу та збільшенню кліренсу креатиніну. Досягнення вазопресорного ефекту можливе при використанні високих (понад 15 мкг/кг/хв) доз допаміну, епі–нефрину в дозах понад 0,3 мкг/кг/хв та норепінефрину (норадреналіну) [24, 52]. Препаратом першого ряду для лікування теплого рідинно-рефрактерного СШ із високим СВ/низьким ЗПСО вважають норепінефрин. Також він є препаратом вибору дорослих із СШ у тому разі, коли спостерігаються низький діастолічний АТ (менше половини систолічного АТ) та, відповідно, знижений ЗПС як монотерапія. У той же час певна кількість авторів обстоює необхідність комбінації норепінефрину з добутаміном, що здатний через власні властивості вазодилататора компенсувати надмірну вазоконстрикцію. Останнім часом продемонстровані –імуномодулюючі властивості норепінефрину при СШ [53].
Норепінефрин має вводитися в центральні вени, але повідомляється можливість його введення протягом обмеженого часу в периферичні вени та внутрішньокістково [54].
За відсутністю ефекту від норепінефрину можна спробувати призначити вазопресин або терліпресин, які сприяють збільшенню САТ, ЗПСО у пацієнтів із СШ та діурезу в пацієнтів із СШ, який виражається у високому СВ/низькому ЗПСО [55–58]. Їх ефективність обумовлена вазоактивною дією, що здійснюється не через стимуляцію адренорецепторів, які при СШ нерідко стають резистентними до катехоламінів. Проте аналіз рандомізованих конт–рольованих досліджень у 2017 р. не продемонстрував позитивного впливу вазопресину/терліпресину на результати при септичному шоку в дітей, натомість отримані дані про зростання ризику розвитку ішемії тканин [59].
Ангіотензин також може бути використаний для підвищення артеріального тиску в пацієнтів, які нечутливі до норепінефрину; але його значення для клініки залишається не зовсім зрозумілим [60]. Фенілефрин — ще один відомий вазопресор із виключним впливом на альфа-адренорецептори [61]. Його переваги над епінефрином не були продемонстровані. У 2016 році опубліковано статтю, у якій проаналізовано наслідки дефіциту норепінефрину в лікарнях США протягом 2011 року та заміни його на фенілефрин, що супроводжувалося значним збільшенням летальності [62].
Проте цей огляд вазопресорів неможливо не завершити ремаркою щодо того, що в Україні з них був доступний лише норепінефрин, власне виробництво якого було припинено, а реєстрація імпортованого норепінефрину припинила діяти понад 5 років тому! З огляду на публікацію, в якій висвітлені наслідки дефіциту норепінефрину в США протягом 2011 р., ми маємо замислитися щодо наслідків відсутності будь-якого вазопресору понад 5 років у нашій країні!
Завершуючи огляд літератури, мусимо визнати, що, попри відверте бажання більшості фахівців з анестезіології та дитячої анестезіології керуватися у власній діяльності зарубіжними настановами щодо ІТ СШ у дітей, ми стикаємося з неможливістю це зробити, навіть у межах рекомендацій для країн з обмеженими економічними можливостями! Серед препаратів для гемодинамічної підтримки доступними є лише: допамін, адреналін (епінефрин), нітрати та умовно — левосимендан! До того ж на відміну від більшості країн світу в Україні доступним є 0,18% розчин адреналіну гідротартрату, а не 0,1% розчин адреналіну гідрохлориду, про застосування якого йдеться у всіх рекомендаціях. Тому жодного розуміння щодо біоеквівалентності, дозування, ефективності 0,18% адреналіну гідротартрату взагалі немає! Його застосування є вимушеним, результати цього прогнозувати складно.
Все ж, зважаючи на теоретичне підґрунття, власний досвід та наявні можливості, ми радимо розпочинати інотропну підтримку при СШ у дітей низькими (0,1–0,3 мкг/кг/хв) дозами адреналіну, спираючись на його більш надійний вплив порівняно з допаміном у дітей першого року життя та в умовах ацидозу. Збільшення дози адреналіну за необхідності може забезпечувати бажаний пресорний ефект. Використання допаміну бажано уникати. За умов поганої периферичної перфузії та збереженого АТ доцільно обережно титрувати нітрати з урахуванням їх сторонніх ефектів. Рефрактерний СШ із низьким серцевим викидом може бути підставою для призначення левосимендану.
Висновки
1. Сучасне розуміння характеру гемодинамічних розладів, їх діагностика, моніторинг та адекватна ІТ здатні істотно вплинути на зниження летальності при СШ у дітей.
2. Найбільш важливими показниками гемодинаміки, цільові значення яких важливо забезпечувати при ІТ СШ у дітей, є СВ, ЦВТ, САТ, ПТ, ЧСС.
3. Найбільш важливими препаратами для корекції гемодинамічних розладів при СШ у дітей є епінефрин, норепінефрин, добутамін, нітрати, інгібітори фосфодіестерази, левосимендан, вазопресин та допамін.
4. Сучасна оцінка гемодинаміки в дітей із СШ, застосування адекватних рекомендацій щодо ІТ її розладів із використанням прийнятих у світі препаратів в умовах відділень інтенсивної терапії в Україні є вкрай обмеженими та неадекватними.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Kawasakii T. Update on pediatric sepsis: a review / T. Kawasakii // Journal of Intensive Care. — 2017. — Vol. 7. — doi: 10.1186/s40560-017-0240-1.
2. Martin K. Initial resuscitation and management of pediatric septic shock / K. Martin, S. Weiss // Minerva Pediatr. — 2015. — Vol. 67(2). — Р. 141-158.
3. The role of healthcare delivery in the outcome of meningococcal disease in children: case-control study of fatal and non-fatal cases / N.Ninis, C. Phillips, L. Bailey et al. // BMJ. — 2005. — Vol. 330. — doi: 10.1136/bmj.330.7506.1475.
4. Brierly J. Hemodynamics of early pediatric fluid resistant septic shock using non-invasive cardiac output (USCOM) distinct profiles of CVC infection and community acquired sepsis / J. Brierly, T. Thiruchelvan, M. Peters // Crit. Care Med. — 2006. — Vol. 33. — P. 171-179.
5. Evolution of haemodynamics and outcome of fluid-refractory septic shock in children / A. Deep, C. Goonasekera, Y. Wang et al. // Intensive Care Med. — 2013. — Vol. 39. — P. 1602-1609.
6. Practice parameters for hemodynamic support of sepsis in adults patients: 2004 update / S. Hollenberg, T. Ahrens, D. Annane et al. // Crit. Care Med. — 2004. — Vol. 32. — P. 1928-1948.
7. Trof R. Global end-diastolic volume increases to maintain fluid responsiveness in sepsis-induced systolic dysfunction // R. Trof, I. Danad, J. Groeneveld // BMC Anesthesiology. — 2013. — Vol. 13. — doi: 10.1186/1471-2253-13-12.
8. Hunter J. Sepsis and the heart / J. Hunter, M. Doddi // British Journal of Anaesthesia. — 2010. — Vol. 104. — P. 3-11. — doi: 10.1093/bja/aep339.
9. Pollack M. Distributions of cardiopulmonary variables in pediatric survivors and nonsurvivors of septic shock / M. Pollack, A. Fields, U. Ruttimann // Crit. Care Med. — 1985. — Vol. 13. — P. 454-459.
10. Hemodynamic support in fluid-refractory pediatric septic shock / G. Ceneviva, J. Paschall, F. Maffei et al. // Pediatrics. — 1998. — Vol. 102. — Р. 19.
11. Diastolic dysfunction and mortality in severe sepsis and septic shock / G. Landesberg, D. Gilon, Y. Meroz et al. // Europen Heart Journal. — 2012. — Vol. 33. — P. 895-903.
12. Diastolic dysfunction and mortality in early severe sepsis and septic shock: a prospective, observational echocardiography study / S. Brown, J. Pittman, E. Hirshberg et al. // Clinical Ultrasound Journal. — 2012. –Vol. 4. — P. 2-9.
13. Elisen L. Left ventricular diastolic dysfunction in the intensive care unit: trends and perspectives. Review Article / L. Elisen, P. Davlouros, D. Karakitsos // Hindawi Publishing Corporation Critical Care Research and Practice. — 2012. — doi: 10.1155/2012/964158.
14. Management of Myocardial Dysfunction in Severe Sepsis / M. Jozwiak, R. Persichini, X. Monnet, J.-L. Teboul // Semin. Respir. Crit. Care Med. — 2011. — Vol. 32. — P. 206-214.
15. Pathophysiology of Sepsis-Related Cardiac Dysfunction: Driven by Inflammation, Energy Mismanagement, or Both? / K. Drosatos, A. Lymperopoulos, P. Johannes Kennel et al. // Cur. Heart Fail. Rep. — 2015. — Vol. 12. — P. 130-140.
16. Георгіянц М. Стан систолічної та діастолічної функції міокарду при сепсисі у дітей. Клінічні та прогностичні аспекти. / М. Георгіянц, В. Корсунов, К. Столяров // Медицина неотложных состояний. — 2016 — № 1(72). — С. 103-111.
17. Moloney E. Pathophysiology and pharmacological treatment of pulmonary respiratory distress syndrome / E. Moloney, T. Evans // Eur. Respir. J. — 2003. — Vol. 21. — P. 720-727.
18. Right ventricular function of patients with septic shock: cli–nical significance / D. Liu, B. Du, Y. Long et al. // Zhonghua Wai Ke Za Zhi. — 2000. — № 7. — P. 488-492.
19. Resuscitating the microcirculation in sepsis: The central role of nitric oxide, emerging concepts for novel terapies, and challenges for clinical trials / S. Trzeciak, I. Cinel, R.P. Dellinger et al. // Ac. Emerg. Med. — 2008. — Vol. 15. — P. 399-413.
20. Elberts P. Bench-to-bedside review: Mechanisms of critical illness — classifying microcirculatory flow abnormalities in distributive shock / P. Elbers, C. Ince // Crit. Care. — 2006 — Vol. 10. — P. 221-227.
21. Microvascular blood flow is altered in patients with sepsis / D. De Backer, J. Creteur, J.-C. Preiser et al. // Am. J. of Resp., Crit. Care Med. — 2002. — Vol. 166. — P. 98-104.
22. Bateman R. Bench-to-bedside review: Microvascular dysfunction in sepsis — hemodynamics, oxygen transport, and nitric oxide / R. Bateman, M. Sharpe, C. Ellis // Crit. Care. — 2003. — Vol. 7. — P. 359-373.
23. Bridges E. Cardiovascular Aspects of Septic Shock / E. Brid–ges, M. Dukes // Critical Care Nurse. — 2005. — Vol. 25. — P. 14-40.
24. American College of Critical Care Medicine Clinical Practice Parameters for Hemodynamic Support of Pediatric and Neonatal Septic Shock / A. Davis, J. Carcillo, R. Aneja et al. // Critical Care Medicine. — 2017. — Vol. 45 — P. 1061-1093.
25. Randomized controlled trial comparing cerebral perfusion pressure-targeted therapy versus intracranial pressure-targeted therapy for raised intracranial pressure due to acute CNS infections in children / R. Kumar, S. Singhi, P. Singhi et al. // Crit. Care Med. — 2014. — Vol. 42. — P. 1775-1787.
26. The effects of norepinephrine on hemodynamics and renal function in severe septic shock states / E. Redl-Wenzl, C. Armbruster, G. Edelmann et al. // Intensive Care Med. — 1993. — Vol. 19. — P. 151-154.
27. Морган Дж.E. мл. Клиническая анестезиология. Кн. 2-я.: Пер. с англ. / Дж.E. Морган мл., М.С. Михайл. — М.; СПб.: БИНОМ; Невский диалект, 2010. — 366 с.
28. Recommendations for sepsis management in resource-limited settings / M. Duűnser, E. Festic, A. Dondorp et. al. // Intensive Care Med. — 2012. — Vol. 38. — P. 557-574.
29. McLean S. Echocardiography in shock management / S. McLean // Critical Care. — 2016. — Vol. 20. — 275. DOI: 10.1186/s13054-016-1401-7.
30. Surviving Sepsis Campaign: International Guidelines for Management of Severe Sepsis and Septic Shock: 2012 / R. Dellinger, M. Levy, A. Rhodes et al. // Crit. Care Med. — 2013. — Vol. 41. — P. 580-637.
31. Khilnani P. Recent advances in sepsis and septic shock / P. Khilnani, S. Deopujari, J. Carcillo // Indian J. of Ped. — 2008. — Vol. 8. — P. 821-830.
32. Growth hormone secretion in critical illness: effect of dopamine / G. Van den Berg, F. de Zegher, P. Lauwers et al. // J. Clin. Endocrinol Metab. — 1994. — Vol. 79. — P. 1141-1146.
33. Effect of dopamine on gastrointestinal motility during critical illness / A. Dive, F. Foret, J. Jamart et al. // Intensive Care Med. — 2000. — Vol. 26. — P. 901-907.
34. Holmes C. Low-dose dopamine in the ICU / C. Holmes, K. Walley // Chest. — 2003. — Vol. 123. — P. 1266-1275.
35. Does dopamine administration in shock influence outcome? Results of the Sepsis Occurrence in Acutely Ill Patients (SOAP) study / Y. Sakr, K. Reinchart, J.-L. Vincent et al. // Crit. Care Med. — 2006. — Vol. 34. — P. 589-597.
36. Influence of vasopressor agent in pediatric septic shock mortality / C. Mangia, L. Jose, F. Monteiro et al. // Critical Care. — 2011. — Vol. 15. — P. 16. — doi: 10.1186/cc10164.
37. Vincent J.-L. Dobutamine administration in septic shock: addition to standard protocol / J.-L. Vincent, A. Roman, R. Kahn // Crit. Care Med. — 1990. — Vol. 18. — P. 689-693.
38. Arikan A. Pediatric shock / A. Arikan // Signa Vitae // Journal for Intensive Care and Emergency medicine. — 2008. — Vol. 3. — P. 13-23.
39. Vallet B. How to titrate vasopressors against fluid loa–ding in septic shock / B. Vallet, H. Tytgat, G. Lebuffe // Advances in Sepsis. — 2007. — Vol. 6. — P. 34-44.
40. Hauser G.J. Early goal-directed therapy of pediatric septic shock in the emergency department / G.J. Hauser // Israeli J. of Emergency Medicine. — 2007. — Vol. 7. — P. 5-17.
41. Double-blind prospective randomized controlled trial of dopamine versus epinephrine as firstline vasoactive drugs in pediatric septic shock / A. Ventura, H. Shieh, A. Bousso et al. // Crit. Care Med. — 2015. — Vol. 43. — P. 2292-2302.
42. Dopamine versus epinephrine for cardiovascular support in low birth weight infants: Analysis of systemic effects and neonatal clinical outcomes / E. Valverde, A. Pellicer, R. Madero et al. // Pediatrics. — 2006. — Vol. 117. — P. 1213-1222.
43. Double-Blind Randomized Clinical Trial Comparing Dopamine and Epinephrine in Pediatric Fluid-Refractory Hypotensive Septic Shock / K. Ramaswamy, S. Singhi, M. Jayashree et al. // Pediatric Critical Care Medicine. — 2016 — Vol. 17 — P. 502-512.
44. Nitroglycerin in septic shock after intravascular volume resuscitation / P. Spronk, C. Ince, M. Gardien et al. // Lancet. — 2002. — Vol. 360. — P. 1395-1396.
45. Hemodynamic effects of i.v. milrinone lactate in pediatric patients with septic shock. A prospective, double-blinded, randomized, placebo-controlled, interventional study / P. Barton, J. Garcia, A. Kouatli et al. // Chest. — 1996. — Vol. 109. — P. 1302-1312.
46. Milrinone: Systemic and pulmonary hemodynamic effects in neonates after cardiac surgery / A. Chang, A. Atz, G. Wernovsky et al. // Crit. Care Med. — 1995. — Vol. 23. — P. 1907-1914.
47. Successful reversal of resistent hypodynamic septic shock with levosimendan / M. Matejovic, A. Krouzecky, J. Radej et al. // Acta Anaesthesiol Scand. — 2005. — Vol. 49. — P. 127-128.
48. Levosimendan in septic cardiac failure / A. Noto, M. Giacomini, A. Palandi et al. // Intensive Care Med. — 2005. — Vol. 31. — P. 1164-1165.
49. Early experience with Levosimendan in children with ventricular dysfunction / P. Namachivayam, D. Crossland, W. Butt et al. // Pediatr. Crit. Care Med. — 2006. — Vol. 7. — P. 445-448.
50. The use of Levosimendan in myocardial dysfunction due to sepsis / J.Vaitsis, H. Michalopoulou, C. Thomopoulos et al. // Сrit. Care. — 2009. — Vol. 13 (Suppl.). — P. 165.
51. Alhashemi J. Levosimendan versus dobutamine in septic shock / J. Alhashemi, Q. Alotaibi // Сrit. Care. — 2009. — Vol. 13 (Suppl.). — P. 171.
52. Noradrenaline for management of septic shock refractory to fluid loading and dopamine or dobutamine in full-term newborn infants / P. Tourneux, T. Rakza, A. Abazine et al. // Acta Paediatr. — 2008. — Vol. 97. — P. 177-180.
53. Potentially Inadvertent Immunomodulation: Norepinephrine Use in Sepsis / R. Stolk, T. van der Poll , D. Angus et al. // American Journal of Respiratory and Critical Care Medicine. — 2016. — Vol. 194. — doi: 10.1164/rccm.201604-0862CP.
54. Noradrenaline use for septic shock in children: Doses, routes of administration and complications / M. Lampin, J Rousseaux, A. Botte et al. // Acta Paediatr. — 2012. — Vol. 101. — P. 426-430.
55. Use of vasopressin in refractory hypotension in children with vasodilatory shock: Five cases and a review of the literature / J. Liedel, W. Meadow, J. Nachman et al. // Pediatr. Crit. Care Med. — 2002. — Vol. 3. — P. 15-18.
56. Vasopressin infusion in children with catecholamine-resistant septic shock / A. Vasudevan, R. Lodha, S. Kabra et al. // Acta Paediatr. — 2005. — Vol. 94. — P. 380-383.
57. Terlipressin for catecholamine-resistant septic shock in children / A. Rodriguez-Nńűez, M. Fernández-Sanmartin, F. Martinуn-Torres et al. // Intensive Care Med. — 2004. — Vol. 30. — P. 477-480.
58. Terlipressin as rescue therapy for intractable hypo-
tension during neonatal septic shock / I. Matok, L. Leibovitch, A. Vardi et al. // Pediatr. Crit. Care Med. — 2004. — Vol. 5. — P. 116-118.
59. Role of vasopressin and terlipressin in refractory shock compared to conventional therapy in the neonatal and pediatric population: a systematic review, meta analysis, and trial sequential analysis / R. Masarwa, G. Paret, A. Perlman et al. // Critical Care. — 2017. — Vol. 21. — DOI: 10.1186/s13054-016-1589-6.
60. Yunge M. Angiotensin for septic shock unresponsive to noradrenaline / M. Yunge, A. Petros // Arch. Dis. Child. — 2000. — Vol. 82. — P. 388-389.
61. Experience with phenylephrine as a component of the pharmacologic support of septic shock / J. Gregory, M. Bonfiglio, J. Dasta et al. // Crit. Care Med. — 1991. — Vol. 19. — P. 1395-1400.
62. Effects of a national norepinephrine shortage on patients with septic shock / V. Emily, G. Hayley, H. May et al. // Critical Care Medicine. — 2016. — Vol. 44 — P. 208. — doi: 10.1097/01.ccm.0000509203.00209.75.

/22-1.jpg)