Журнал «Актуальная инфектология» 2 (7) 2015
Вернуться к номеру
Использование результатов ГеноФиброТеста в повседневной клинической практике
Авторы: Анастасий И.А. — Национальный медицинский университет имени А.А. Богомольца, г. Киев
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
В статье представлено значение результатов ГеноФиброТеста для прогнозирования возможности достижения устойчивого вирусологического ответа у пациентов с хроническим гепатитом С 1-го генотипа. Результаты ГеноФиброТеста необходимо учитывать при принятии решения о противовирусной терапии. Информирование пациента об активности и стадии заболевания увеличивает его приверженность к терапии. Результаты ГеноФиброТеста позволяют модифицировать длительность лечения в зависимости от достижения быстрого вирусологического ответа.
У статті представлено значення результатів ГеноФіброТесту для прогнозування можливості досягнення стійкої вірусологічної відповіді в пацієнтів із хронічним гепатитом С 1-го генотипу. Результати ГеноФіброТесту необхідно враховувати при прийнятті рішення про противірусне лікування. Інформування хворого про активність і стадію захворювання підвищує його прихильність до терапії. Результати ГенофіброТесту дозволяють модифікувати тривалість лікування залежно від досягнення швидкої вірусологічної відповіді.
The value of GenoFibroTest results for predicting the possibility of achieving sustained virological response in patients with chronic hepatitis C genotype 1 is presented in this article. The results of GenoFibroTest must be taken into account to make a decision about antiviral therapy. Patient’s awareness about the activity and the stage of the disease increases the adherence to treatment. The results of GenoFibroTest enable to modify treatment duration depending on achievement of rapid virological response.
гепатит С, устойчивый вирусологический ответ, ГеноФиброТест.
гепатит С, стійка вірусологічна відповідь, ГеноФіброТест.
hepatitis C, sustained virological response, GenoFibroTest.
Статья опубликована на с. 13-17
В структуре инфекционной патологии вирусные гепатиты занимают одно из первых мест. Угроза для здоровья населения обусловлена прежде всего высокой вероятностью развития хронических форм поражения печени — хронического гепатита, цирроза печени, гепатоцеллюлярной карциномы (ГЦК). ГЦК составляет 5,4 % от всех злокачественных новообразований человека и 95 % — от всех первичных злокачественных опухолей печени. Хроническая НСV-инфекция в последнее десятилетие занимает ведущее место в этиологии ГЦК [1]. В 2002 году специалистами Национального института здоровья США (National Institutes of Health) было сделано следующее заявление: «Если не будут приняты безотлагательные меры, то через 10–20 лет смертность от НСV-инфекции и ее последствий увеличится в 3 раза и значительно превысит этот показатель при ВИЧ-инфекции. За это время хронический гепатит С (ХГС) станет главной проблемой национальных органов здравоохранения» [2]. Современные реалии подтверждают прогноз, сделанный в 2002 году.
В настоящее время, по разным данным, гепатитом С (ГС) в мире инфицировано от 170 до 200 млн человек [3]. Не менее чем у 25–30 % из них разовьется цирроз печени (ЦП), а у 10 % — гепатоцеллюлярная карцинома [1]. В Украине вирусом гепатита С (HCV) инфицировано не менее 3 % населения [4]. Некоторые эпидемиологические исследования показывают, что среди населения Украины в возрасте старше 15 лет количество больных ХГС составляет 8,9 % [5–7].
Представленные факты объясняют актуальность диагностики и лечения хронических вирусных гепатитов.
Основной путь прогрессирования этих заболеваний — развитие последовательных стадий фиброза с формированием в конечном итоге цирроза и рака печени, что предопределяет плохой жизненный прогноз и короткие сроки выживаемости этой категории больных [8–10].
Раннее выявление и уточнение стадии фиброза позволяет своевременно назначить терапию, направленную на уменьшение темпов его прогрессирования, и не допустить развитие цирроза и рака печени [9–11]. В повседневной клинической практике хорошо себя зарекомендовал неинвазивный метод оценки фиброза печени ФиброТест/АктиТест (компания BioPredictive, Париж, Франция). Результаты этого теста позволяют оценить стадии фиброза (F0, F1, F2, F3, F4) и степень некровоспалительного процесса (А0, A1, A2, А3) по шкале METAVIR [12].
Эффективность противовирусной терапии (ПВТ) зависит от факторов хозяина (организма больного) и вируса. Главными факторами вируса, определяющими эффективность ПВТ, являются генотип, вирусная нагрузка. Полиморфизм гена IL28B (rs12979860) определяет вероятность излечения от гепатита С больных, инфицированных 1-м или 4-м генотипом вируса. У пациентов с генотипом СС она максимальна. Наименьшие шансы имеют больные с СТ и ТТ вариантами аллели этого гена [13]. Вторым по важности фактором является выраженность фиброза. Наибольшие шансы на излечение имеют пациенты с начальными стадиями фиброза, наименьшие — пациенты с ЦП. Больные с высокой гистологической активностью гепатита имеют большие шансы на излечение, нежели пациенты с минимальной выраженностью воспаления [1].
Главный критерий эффективности лечения гепатита С — устойчивый вирусологический ответ (УВО) — неопределяемая РНК HCV через 24 недели после завершения лечения. Инфекция излечивается у более 99 % пациентов, достигших УВО, считающегося как неопределяемые уровни РНК ВГС через 24 недели после окончания лечения [13]. Современный стандарт терапии — комбинация пегилированного интерферона-альфа (пегилированный ИФН-альфа) и рибавирина (в дальнейшем — пегИФН/РБВ) [14, 15]. При таком режиме лечения пациенты, инфицированные ВГС 1-го генотипа, имели частоту УВО приблизительно 40 % в Северной Америке и 50 % в Западной Европе. Более высокая частота УВО достигается у пациентов, инфицированных ВГС генотипов 2, 3, 5 и 6 (максимум 80 %, причем больше для генотипа 2, чем для генотипов 3, 5 и 6), а промежуточная частота УВО были достигнута у пациентов с ГС 4-го генотипа [13].
Недостаточно эффективные результаты лечения пациентов, инфицированных 1-м генотипом, стимулировали разработку новых лекарств для лечения гепатита С. В 2011 году в Европе и США, а позже и в Украине были зарегистрированы боцепревир (БОЦ) и телапревир (ТВР) — первые противовирусные препараты прямого действия (ППД) — ингибиторы вирусной NS3/4-протеазы. Комбинация пегИФН/РБВ с БОЦ или ТВР позволила увеличить вероятность достижения УВО на 20–30 % для пациентов, как ранее не получавших лечение, так и не ответивших на предшествующий курс терапии [16]. В 2014 году в США и Европе стали применяться противовирусные ППД 2-го поколения (симепревир и софосбувир), отличающиеся большей эффективностью и лучшим профилем безопасности [13]. В настоящее время активно обсуждаются безынтерфероновые схемы лечения ХГС, эффективность которых будет превышать 90 %. В Европе и США эти схемы терапии уже доступны [17].
С 2013 года в Украине реализуется Государственная программа лечения больных хроническими вирусными гепатитами [16]. Выделение бюджетных средств на закупку противовирусных препаратов прямого действия пока не планируется. Соответственно, применение современных схем лечения гепатита С (тройная терапия, безынтерфероновые схемы) в нашей стране ограничивается финансовыми возможностями пациента.
Необходимо отметить, что, несмотря на применение ППД в лечении гепатита С, стандартная схема терапии гепатита С (пегИФН/РБВ) остается актуальной для пациентов с 1-м генотипом вируса. Так, согласно последним рекомендациям Европейской ассоциации по изучению печени (ЕASL), стандартная терапия гепатита С (пегИФН/РБВ) может быть с успехом применена и у больных с 1-м генотипом вируса. «Двойная терапия может быть целесообразна для некоторых пациентов, ранее не получавших лечение, с исходными характеристиками, предвещающими высокую вероятность быстрого вирусологического ответа (БВО) и УВО на пегИФН/РБВ. Следует учитывать экономность и лучшую переносимость двойной терапии» [13].
Больные с компенсированным ЦП и тяжелым фиброзом должны рассматриваться как пациенты с неотложными показаниями к проведению ПВТ независимо от активности гепатита и наличия кофакторов прогрессии заболевания. Больным с умеренным фиброзом лечение должно быть настоятельно рекомендовано, особенно при умеренной/высокой активности гепатита, а также наличии кофакторов. В случае минимального фиброза, но при наличии высокой активности и кофакторов прогрессии заболевания возможность лечения также должна быть рассмотрена [13].
Указанные обстоятельства обусловливают особенную актуальность обоснованного отбора пациентов на лечение и требуют учета всех вышеперечисленных факторов организма больного и вируса, определяющих в конечном счете эффективность ПВТ.
Наиболее значимыми предикторами для оценки эффективности ПВТ до начала терапии являются генотип вируса, вирусная нагрузка, стадия заболевания печени (наличие или отсутствие ЦП), полиморфизм гена IL28B. ФиброТест/АктиТест (компания BioPredictive, Париж, Франция) позволяет определить активность и стадию заболевания и представить их в терминах шкалы METAVIR. В случае рассмотрения вопроса о лечении пациента с 1-м генотипом вируса гепатита С неоценимую помощь может оказать ГеноФиброТест (BioPredictive, Париж, Франция). Для выполнения теста в венозной крови у больного гепатитом С определяются содержание гаптоглобина, альфа-2-макроглобулина, билирубина, аполипопротеина и АЛТ, необходимых для неинвазивной диагностики активности и стадии гепатита (АктиТест и ФиброТест соответственно), вариант аллели гена IL28B, вирусная нагрузка и генотип вируса. После соответствующей математической обработки полученных данных выдается результат теста в виде значения вероятности достижения устойчивого вирусологического ответа в результате лечения. Дополнительными учитываемыми параметрами являются возраст и пол пациента.
В данном контексте мы считаем целесообразным приведение наших клинических наблюдений за течением НСV-инфекции у двух пациентов.
Пациентка К., 31 год, врач. В 2012 году ей установлен диагноз «гепатит С». Выявлены суммарные антитела к ВГС при сдаче крови в качестве донора. При дальнейшем обследовании методом ПЦР выявлена РНК НСV, генотип 1а.
При объективном обследовании: масса тела 61 кг, рост 177 см, кожа и видимые слизистые без особенностей. Язык влажный, чистый. Со стороны сердечно-сосудистой системы, органов дыхания патологических изменений не выявлено. АД 110/70 мм рт.ст. Живот при пальпации мягкий, безболезненный. Печень не увеличена. Селезенка не пальпируется. Физотправления в норме.
Эластография печени: F0 (METAVIR). При УЗИ щитовидной железы патологических изменений не выявлено. ЭКГ — возрастная норма.
При лабораторном исследовании: Hb — 143 г/л, эритроциты — 4,42 x 1012/л, лейкоциты — 4,4 x 109/л, тромбоциты — 155 x 109/л, СОЭ — 5 мм/час. Биохимический анализ крови: АЛТ — 84 Ед/л, показатели АСТ, ГГТП, ТП, билирубина, сывороточного железа, мочевины, креатинина, глюкозы — вариант нормы. Гормоны щитовидной железы без патологических изменений. Функция щитовидной железы не нарушена. Данных по аутоиммунному тиреоидиту, гепатиту не выявлено. Результаты обследования на HBV, HGV отрицательные.
ПЦР-исследование: вирусная нагрузка 3,3 x 105 МЕ/мл, генотип 1а. Обследование на антитела к НІV отрицательные.
С учетом клинико-лабораторных данных больной установлен диагноз «хронический гепатит С (РНК HСV+, генотип 1а), репликативная стадия».
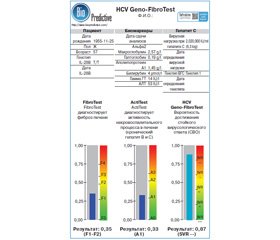
Больной проведен ГеноФиброТест (рис. 1).
/15/15.jpg)
Получены следующие результаты: IL28B C/C, F0, A0, вероятность достижения УВО 72 %.
Было принято решение начать лечение, несмотря на отсутствие фиброза и низкую гистологическую активность гепатита. Одним из мотивирующих факторов была высокая вероятность достижения УВО — 72 %.
23 января 2014 года начато лечение пегИФН/РБВ. Переносимость лечения удовлетворительная. После первой инъекции пегИФН наблюдались лихорадка, ломота в теле, повышение температуры тела до 39,4 °С. После принятия парацетамола состояние нормализовалось. После второй инъекции пегИФН — субфебрильная температура тела, общая слабость. При дальнейших введениях интерферона пирогенные реакции не наблюдались. На протяжении лечения гематологических изменений (анемия, лейко-, тромбоцитопения), которые бы потребовали коррекции лечения, не наблюдалось.
При проведении ПЦР через 4 недели лечения РНК НСV не выявлена, т.е. достигнут БВО. Отрицательные результаты ПЦР на выявление РНК НСV получены также на 12-й и 24-й неделе лечения. По результатам ГеноФиброТеста вероятность достижения УВО составляла 72 %. В рекомендациях Европейской ассоциации по изучению печени (ЕASL) сообщается: «При двойной терапии лечение следует сокращать лишь в том случае, если исходные уровни РНК ВГС меньше 400 000 МЕ/мл, БВО достигнут и отсутствуют какие-либо другие предикторы неблагоприятного исхода лечения» [13]. Согласно данным F. Poordad, главными факторами, влияющими на результаты как стандартной терапии (пегИФН/РБВ), так и тройной (пегИФН/РБВ + ППД), оказались возраст, вирусная нагрузка, выраженность фиброза, полиморфизм гена IL28B, ожирение и стеатоз печени [18]. У нашей пациентки отсутствовали фиброз и стеатоз печени, ожирение, полиморфизм гена IL28B был наиболее благоприятным для достижения УВО. ГеноФиброТест — 72 %. Было принято решение сократить курс терапии до 24 недель. При проведении ПЦР через 24 недели после окончания лечения вирус гепатита С не обнаружен, т.е. достигнут УВО.
Пациентка О., 58 лет, пенсионерка. В 2010 году выявлены суммарные антитела к ВГС. При дальнейшем обследовании методом ПЦР выявлена РНК НСV, генотип 1b.
При объективном обследовании: масса тела 81 кг, рост 166 см, кожа и видимые слизистые без особенностей. Язык влажный, чистый. Со стороны сердечно-сосудистой системы, органов дыхания патологических изменений не выявлено. АД 130/80 мм рт.ст. Живот при пальпации мягкий, безболезненный. Печень до +2 см из-под края реберной дуги. Селезенка не пальпируется. Физотправления в норме.
При УЗИ гепатобилиарной зоны выявлены УЗ-признаки умеренных диффузных изменений паренхимы печени. При УЗИ щитовидной железы патологических изменений не выявлено. ЭКГ — возрастная норма.
При лабораторном исследовании: Hb — 133 г/л, эритроциты — 4,15 x 1012/л, лейкоциты — 4,8 x 109/л, тромбоциты — 185 x 109/л, СОЭ — 5 мм/час. Биохимический анализ крови: АЛТ — 53 Ед/л, показатели АСТ, ГГТП, ТП, билирубина, сывороточного железа, мочевины, креатинина, глюкозы — вариант нормы. Гормоны щитовидной железы без патологических изменений. Функция щитовидной железы не нарушена. Данных по аутоиммунному тиреоидиту, гепатиту не выявлено. Результаты обследования на HBV, HGV отрицательные.
ПЦР-исследование: вирусная нагрузка 2,2 x106 МЕ/мл, генотип 1b. Обследование на антитела к НІV отрицательные.
С учетом клинико-лабораторных данных больной установлен диагноз «хронический гепатит С (РНК HСV+, генотип 1b), репликативная стадия».
Больной проведен ГеноФиброТест (рис. 2).
/16/16.jpg)
Получены следующие результаты: IL28B Т/Т, F1–2, A1, вероятность достижения УВО 13 %. Факторами, снижающими вероятность УВО, были: 1-й генотип вируса, неблагоприятный вариант аллели IL28B, возраст пациентки, низкая гистологическая активность гепатита (А1 по шкале METAVIR), высокая вирусная нагрузка. Совокупность данных факторов снизила вероятность достижения УВО с 40–45 % [13] до 13 %.
Пациентка приняла решение о проведении терапии, несмотря на результаты ГеноФиброТеста, так как была высокомотивирована на лечение, отсутствовали сопутствующие заболевания других органов и систем. Немаловажным фактором был опыт успешного излечения гепатита С у дочери пациентки. Собственно, и обследование на гепатит С было произведено в связи с болезнью дочери. Применение ППД для лечения не рассматривалось в связи с ограниченными финансовыми возможностями пациентки.
14 марта 2013 года начато лечение пегИФН/РБВ. Переносимость лечения удовлетворительная. После первой инъекции наблюдались субфебрильная температура тела, общая слабость. При проведении ПЦР через 4 недели лечения РНК НСV 3,29 x 103 МЕ/мл. БВО не был достигнут. Cнижение вирусной нагрузки произошло на 3 log10. Следует отметить, что, согласно рекомендациям Европейской ассоциации по изучению печени, если HCV РНК снижается более чем на 2 log10 от исходного значения через 12 недель терапии, лечение может быть продолжено [13]. А в нашем случае (при наличии всех вышеперечисленных предикторов достижения УВО) этот результат достигнут после 4 недель лечения.
При дальнейших введениях интерферона пирогенные реакции не наблюдались. На протяжении лечения гематологических изменений (анемия, лейко-, тромбоцитопения), которые бы потребовали коррекции лечения, не наблюдалось. Контроль показателей аутоиммунного процесса, гормонов щитовидной железы проводился каждые 12 недель терапии. Данных относительно аутоиммунной патологии, поражения щитовидной железы не было.
Результат ПЦР на выявление РНК НСV на 12-й неделе лечения: менее 25 МЕ/мл (аналитическая чувствительность тест-системы 20 МЕ). Результат ПЦР на 24-й неделе терапии: вирус гепатита С не обнаружен, т.е. получен замедленный вирусологический ответ. Полученный результат ПЦР позволил продолжить лечение гепатита, с пролонгацией до 72 недель [13]. После 72 недель терапии отмечались такие гематологические показатели: Hb — 101 г/л, эритроциты — 3,46 x 1012/л, лейкоциты — 2,3 x 109/л, тромбоциты — 127 x 109/л. Биохимический анализ крови: АЛТ — 17 Ед/л. Масса тела 62 кг. ПЦР: РНК НСV не выявлена. При проведении ПЦР через 24 недели после окончания лечения вирус гепатита С не обнаружен. Достигнут УВО.
Приведенные клинические примеры свидетельствуют, что результаты ГеноФиброТеста необходимо учитывать при принятии решения о противовирусной терапии у пациентов с 1-м генотипом вируса. Информирование пациента об активности и стадии заболевания увеличивает его приверженность к терапии. Результаты ГеноФиброТеста позволяют модифицировать длительность лечения в зависимости от достижения быстрого вирусологического ответа.
1. Андрейчин М.А. Вірусні гепатити і рак печінки / М.А. Андрейчин, В.І. Дрижак, О.В. Рябоконь, В.С. Копча. — Тернопіль: ТДМУ, 2010. — 188 с.
2. Management of hepatitis C: National Institutes of Health Consensus Development Conference Statement // Hepatology. — 2002. — 36 (suрpl. 1). — S. 3–20.
3. Mitchell A.E., Colvin H.M., Beasley R.P. Institute of Medicine Recommendations for The Prevention and Control of Hepatitis B and C // Hepatology. — 2010. — Vol. 51, № 3. — P. 729–733.
4. Zeuzem S. Interferon-based therapy for chronic hepatitis C: current and future perspectives. Nature Clinical Practice // Gastroenterology and Hepatology. — 2008. — № 5. — P. 610–622.
5. Голубовская О.А. Проблемы оказания медицинской помощи больным ВИЧ-инфекцией и вирусными гепатитами в Украине // Клиническая инфектология и паразитология. — 2013. — № 4. — С. 9–12.
6. Голубовська О.А., Пронюк Х.О. Стеатоз, інсулінорезистентність і хронічний гепатит С: патогенетичні механізми та клінічне значення // Сучасна гастроентерологія. — 2012. — № 5. — C. 102–110.
7. Щербак И. Тройная терапия в борьбе с вирусным гепатитом С: достижения и перспективы // Український медичний часопис. — 2013. — № 2(94). — 15–18.
8. Ивашкин В.Т. Оценка функционального состояния печени // Болезни печени и желчевыводящих путей / Под ред. В.Т. Ивашкина. — 2-е изд., испр. и доп. — М.: Изд. дом «М-Вести», 2005. — С. 66–84.
9. Павлов Ч.С., Золоторевский В.Б., Томкевич М.С. и др. Возможность обратимости цирроза печени (клинические и патогенетические предпосылки) // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2006. — Т. 16, № 1. — С. 20–29.
10. Павлов Ч.С., Ивашкин В.Т. Как оценить и уменьшить риск фиброза, цирроза и гепатоцеллюлярной карциномы у пациентов с хронической инфекцией вирусами гепатитов В и С // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2007. — Т. 17, № 5. — С. 16–23.
11. Павлов Ч.С., Золоторевский В.Б., Ивашкин В.Т. и др. Современные методы ранней диагностики фиброза печени // Клин. мед. — 2005. — Т. 83, № 12. — С. 58–60.
12. Poynard T. et al. Overview of diagnostic value of biochemical markers of liver fibrosis (FibroTest, HCVFibroSure) and necrosis (ActiTest) in patients with chronic hepatitis С // Comparative Hepatology. — 2004. — 3. — 8.
13. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of hepatitis C virus infection // Journal of Hepatology. — 2014. — Vol. 60. — P. 392–420.
14. Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) медичної допомоги. Вірусний гепатит С. — МОЗ України, 2013 [Електронний ресурс]. — Режим доступу: http://www.moz.gov.ua_106.htm
15. Ghany M.G., Strader D.B., Thomas D.L., Seef L.B. Diagnosis, management, and treatment of hepatitis C: An update AASLD practice guidelines // Hepatology. — 2009. — Vol. 49, № 4. — P. 1335–1374.
16. Голубовская О.А., Корчинский Н.Ч. Актуальность и некоторые проблемы «тройной» терапии больных хроническим гепатитом С // Клиническая инфектология и паразитология. — 2014. — № 1. — С. 59–69.
17. Tania Mara Welzel, Georg Dultz, Stefan Zeuzem Interferon-free antiviral combination therapies without nucleosidic polymerase inhibitors // Journal of Hepatology. — 2014. — Vol. 61. — P. 98–107.
18. Poordad F. Boceprevir for untreated chronic HCV genotype 1 infection / F. Poordad, J. McCone Jr, B.R. Bacon et al. // N. Engl. J. Med. — 2011. — Vol. 31, № 364(13). — P. 1195–1206.