Журнал «Здоровье ребенка» 3 (54) 2014
Вернуться к номеру
Клінічна ефективність вітчизняного препарату урсодеоксихолієвої кислоти в комплексному лікуванні гіпербілірубінемій у недоношених немовлят
Авторы: Добрянський Д.О. - Львівський національний медичний університет імені Данила Галицького;
Бонецька Л.В., Носова І.О., Орел К.В., Тєлєгіна Т.В., Безпалько О.В., Дубровна Ю.Ю., Процик С.В., Децик О.Я. - Львівська обласна клінічна лікарня
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
Результати кількох невеликих пілотних клінічних досліджень свідчать, що використання урсодеоксихолієвої кислоти (УДХК) може полегшувати перебіг неонатальних жовтяниць. Метою роботи була оцінка клінічної ефективності препарату Укрлів® суспензія в комплексному лікуванні гіпербілірубінемій у недоношених немовлят. У відкрите рандомізоване дослідження були залучені 35 передчасно народжених дітей (19 — в основній, 16 — у контрольній групі). Критеріями включення були передчасне народження й гіпербілірубінемія (загальний білірубін сироватки крові > 225 мкмоль/л) у ранній неонатальний період. Новонародженим в основній групі на додаток до фототерапії призначали Укрлів® суспензію в добовій дозі 20 мг/кг упродовж 14 днів. Сформовані групи не відрізнялися за основними клінічними показниками й вихідними концентраціями білірубіну в сироватці крові. У дітей з обох груп відбувалося вірогідне зниження початкових концентрацій загального білірубіну сироватки крові. За перші 3 дні лікування відповідна динаміка становила 44% в основній проти 32% в контрольній групі, забезпечуючи досягнення вірогідної відмінності між групами за рівнем загального і прямого білірубіну на момент закінчення курсу УДХК. У немовлят з основної групи жовтяниця була менш тривалою. Препарат добре переносився немовлятами, не зауважено будь-яких побічних ефектів його призначення. Таким чином, отримані результати дозволяють зробити висновки про доцільність застосування Укрлів® суспензії в комплексному лікуванні гіпербілірубінемій у передчасно народжених немовлят.
Результаты нескольких небольших пилотных клинических исследований свидетельствуют, что использование урсодеоксихолиевой кислоты (УДХК) может облегчить течение неонатальных желтух. Целью работы была оценка клинической эффективности препарата Укрлив® суспензия в комплексном лечении гипербилирубинемий у недоношенных младенцев. В открытое рандомизированное исследование были привлечены 35 преждевременно рожденных детей (19 — в основной, 16 — в контрольной группе). Критериями включения были преждевременное рождение и гипербилирубинемия (общий билирубин сыворотки крови > 225 мкмоль/л) в ранний неонатальный период. Новорожденным в основной группе в дополнение к фототерапии назначали Укрлив® суспензию в суточной дозе 20 мг/кг в течение 14 дней. Сформированные группы не отличались по основным клиническим показателям и исходным концентрациям билирубина в сыворотке крови. У детей обеих групп происходило достоверное снижение начальных концентраций общего билирубина сыворотки крови. За первые 3 дня лечения соответствующая динамика составила 44% в основной против 32% в контрольной группе, обеспечивая достижение достоверного отличия между группами по уровню общего и прямого билирубина на момент окончания курса УДХК. У младенцев из основной группы желтуха была менее продолжительной. Препарат хорошо переносился младенцами, не отмечено каких-либо побочных эффектов его назначения. Таким образом, полученные результаты позволяют сделать выводы о целесообразности применения Укрлив® суспензии в комплексном лечении гипербилирубинемий у преждевременно рожденных младенцев.
Several small pilot clinical studies suggest that the use of ursodeoxycholic acid (UDCA) may facilitate the course of neonatal jaundice. The aim of the work was to evaluate the clinical efficacy of Ukrliv® suspension in comprehensive treatment of hyperbilirubinemia in premature infants. In an open randomized study there were enrolled 35 preterm infants (19 — in the study, 16 — in the control group). Inclusion criteria were premature birth and hyperbilirubinemia (total serum bilirubin levels > 225 mmol/l) in the early neonatal period. Newborns in the study group, in addition to phototherapy, received Ukrliv® suspension in a daily dose of 20 mg/kg for 14 days. Formed groups did not differ in the main clinical characteristics and baseline concentrations of serum bilirubin. Children in both groups had a significant reduction in the initial concentrations of total serum bilirubin. During the first 3 days of treatment related dynamics was 44% in the study group versus 32% in the control one, ensuring the achievement of significant differences between the groups in the level of total and direct bilirubin at the time of completion of UDCA course. In infants from the study group jaundice was less prolonged. The drug was well tolerated by infants, no adverse effects of its use were revealed. Thus, the obtained results allow us to draw conclusions about the appropriateness of Ukrliv® suspension administration in comprehensive treatment of premature infants with hyperbilirubinemia.
Статья опубликована на с. 45-50
Незважаючи на значну поширеність непрямої гіпербілірубінемії в передчасно народжених дітей, у більшості випадків її перебіг є неускладненим. Такі класичні ознаки хронічної білірубінової енцефалопатії як хореоатетоз і/або порушення слуху рідко є домінуючими клінічними проблемами за даними катамнестичного спостереження [1], а на автопсії в недоношених новонароджених останніми роками практично не виявляють «ядерну жовтяницю» [2]. Водночас невідомо, чи така ситуація є результатом загального покращення перинатальної допомоги і/або ж пов’язана з раннім рутинним профілактичним застосуванням фототерапії, що дозволяє ефективно контролювати рівень білірубіну й суттєво зменшує потребу замінних переливань крові [3, 4]. Застосування ранньої агресивної фототерапії в дітей масою тіла при народженні 751–1000 г також вірогідно зменшує частоту атетозу і значних порушень слуху, однак у найменших немовлят масою 501–750 г таке втручання на 5% збільшує смертність [5]. За даними ретроспективного аналізу, існує майже 90% імовірність того, що така фототерапія підвищує ризик смерті найменших новонароджених, нівелюючи її позитивний ефект стосовно віддалених неврологічних наслідків [5]. Водночас сучасні рекомендації з використання фототерапії й замінного переливання крові в недоношених новонароджених є здебільшого емпіричними, недостатньо ґрунтуються на результатах відповідних наукових досліджень [2, 6, 7].
Тим не менш, випадки хронічного ураження ЦНС, спричиненого токсичною дією непрямого білірубіну, продовжують виявлятись у недоношених немовлят із відносно низькими концентраціями білірубіну в сироватці крові [8, 9] і за відсутності клінічних ознак гострої білірубінової енцефалопатії [10]. Дослідники також висловлюють припущення, що помірна гіпербілірубінемія в недоношених дітей може асоціюватися з легшими формами віддалених дисфункцій ЦНС [2]. Описані сучасні серії випадків ядерної жовтяниці в передчасно народжених немовлят [8–11], включаючи двох дітей із терміном гестації 31 і 34 тижн. у задовільному стані з максимальним рівнем загального білірубіну у сироватці крові відповідно 224 і 251 мкмоль/л, свідчать про актуальність проблеми лікування гіпербілірубінемії і профілактики хронічного білірубінового ураження ЦНС у цій групі новонароджених високого перинатального ризику [8].
Результати кількох невеликих пілотних клінічних досліджень продемонстрували, що застосування урсодеоксихолієвої кислоти (УДХК) підсилює екскрецію прямого білірубіну в недоношених новонароджених із холестазом [12–15], що може позитивно впливати на перебіг неонатальних жовтяниць. УДХК — природна гідрофільна дигідроксильована жовчна кислота, відома своєю гепатопротекторною, холеретичною, антихолестатичною, антиоксидантною, антифібротичною, протизапальною, імуномодулю–ючою й антиапоптичною активністю. Важливою з огляду на наведені вище дані є здатність УДХК та її кон’югованих дериватів блокувати апоптоз нервових клітин, спричинений токсичною дією білірубіну [16]. Отже, призначення УДХК недоношеним немовлятам із гіпербілірубінемією може полегшувати перебіг останньої і сприяти досягненню кращих результатів лікування.
Метою роботи була оцінка клінічної ефективності вітчизняного препарату УДХК (Укрлів® суспензія) в комплексному лікуванні гіпербілірубінемій у недоношених немовлят.
Матеріал і методи
У відкрите рандомізоване дослідження були залучені 35 передчасно народжених дітей (19 — в основній, 16 — у контрольній групі). Критеріями залучення були передчасне народження й гіпербілірубінемія (загальний білірубін сироватки крові > 225 мкмоль/л) у ранній неонатальний період. Рандомізацію пацієнтів у групи здійснювали за допомогою генерованого комп’ютером ряду випадкових чисел. Лікування дітей основної групи відрізнялось тим, що на додаток до фототерапії всі вони отримували вітчизняний препарат УДХК Укрлів® суспензія. Фототерапію в усіх дітей застосовували відповідно до вимог вітчизняного протоколу [17].
Укрлів® суспензію призначали всередину з розрахунку 5 мг/кг кожні 6 год (20 мг/кг/добу) безпосередньо перед годуванням протягом 14 днів. У кількох дослідженнях за кордоном доведено ефективність і безпечність саме такої добової дози і схеми призначення суспензії УДХК недоношеним новонародженим [12–15].
У всіх дітей визначали вміст загального й прямого білірубіну в сироватці крові приблизно через 3, 7 і 14 днів після залучення в дослідження. Активність трансаміназ (ТА) крові визначали у немовлят, яким призначали Укрлів® суспензію, а також у дітей із рівнем прямого білірубіну понад 35 мкмоль/л. Активність лужної фосфатази (ЛФ) у сироватці крові досліджували в новонароджених з основної групи відразу після призначення УДХК і в динаміці. Усім немовлятам проводили ультразвукове сканування печінки, а також робили загальні аналізи крові й сечі в динаміці.
Клінічну ефективність лікування з використанням Укрлів® суспензії оцінювали за впливом на динаміку концентрації білірубіну в крові, тривалість жовтяниці й застосування фототерапії, а також на швидкість досягнення добового об’єму ентерального харчування 160 мл/кг. Визначали також динаміку зазначених вище лабораторних показників на тлі лікування препаратом УДХК.
Додатково вивчали порівняльну поширеність основних перинатальних факторів ризику. Зокрема, брали до уваги стан здоров’я матері, особливості перебігу вагітності й пологів, потребу й обсяг невідкладної допомоги після народження. Крім того, ураховували гестаційний вік і масу тіла немовлят при народженні. Патологічні стани неонатального періоду діагностували за стандартними критеріями. Під час дослідження використовували стандартні протоколи спостереження за станом життєвих функцій, обстеження, харчування й лікування.
У роботі використано стандартні методи описового й порівняльного статистичного аналізу із застосуванням критеріїв x2, Стьюдента і Манна — Уїтні. Показники, що характеризують нормальний розподіл даних, представлено як середнє ± стандартне квадратичне відхилення (SD). Непараметричні дані представлено як медіану [нижній і верхній квартилі]. Усі результати вважали вірогідними, якщо р < 0,05.
Результати та їх обговорення
Сформовані групи не відрізнялися за поширеністю основних перинатальних чинників ризику (таблиця 1) і захворюваністю до моменту виписки з відділення (таблиця 2). Середній гестаційний вік дітей в основній і контрольній групі становив відповідно 33,00 ± 1,33 тижн. проти 32,56 ± 1,75 тижн., а маса тіла при народженні — 1848,95 ± 319,56 г проти 1810,00 ± 293,21 г (р > 0,05 для обох показників). Групи також не відрізнялися між собою за частками дітей, які потребували лікування в умовах відділення інтенсивної терапії новонароджених із використанням парентерального харчування, методики самостійного дихання під постійним позитивним тиском і/або штучної вентиляції легень (таблиця 3). Усіх дітей, залучених у дослідження, лікували за допомогою фототерапії.
Більшість немовлят починали годувати ентерально сумішшю (таблиця 3) приблизно в однаковому віці (1,53 ± 0,84 дня в основній проти 1,75 ± 1,18 дня в контрольній групі; р > 0,05). Не було відмінностей між групами і за віком на момент досягнення мінімального повного добового об’єму (160 мл/кг/добу) ентерального харчування (14,89 ± 6,43 дня в основній проти 13,31 ± 6,27 дня в контрольній групі; р > 0,05).
Сформовані групи не відрізнялися за початковим (відповідно 262,65 ± 52,52 мкмоль/л проти 276,81 ± 34,26 мкмоль/л; р > 0,05) і максимальним (відповідно 279,88 ± 36,61 мкмоль/л проти 279,31 ± 38,16 мкмоль/л; р > 0,05) рівнями загального білірубіну в сироватці крові. Вік на момент досягнення максимальної концентрації загального білірубіну сироватки крові становив 4,50 ± 1,72 дня в основній проти 3,94 ± 1,39 дня в контрольній групі (р > 0,05). Максимальні концентрації прямої фракції білірубіну також були майже однаковими в дітей, які отримували УДХК або стандартне лікування (відповідно 10,5 [7,7–21] мкмоль/л проти 10,5 [10,25–26,25] мкмоль/л; р > 0,05), і виявлялись у віці відповідно 10,75 ± 5,16 дня проти 9,13 ± 5,54 дня (р > 0,05). Середній вік дітей на момент початку терапії Укр–лів® суспензією становив 5,53 ± 2,55 дня.
У дітей з обох груп відбувалося вірогідне зниження початкових концентрацій загального білірубіну сироватки крові (р < 0,001). За перші 3 дні лікування динаміка зменшення відповідного показника становила 44% в основній проти 32% в контрольній групі (р > 0,05), забезпечуючи досягнення на цей момент вірогідної відмінності між групами за рівнем загального білірубіну (відповідно 146,72 ± 59,14 мкмоль/л проти 187,46 ± 48,66 мкмоль/л; р < 0,05).
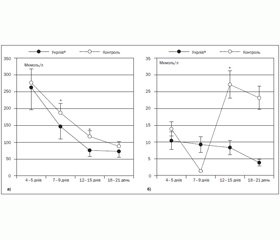
Рівень загального білірубіну в сироватці крові дітей з основної групи був також вірогідно нижчим у віці 12–15 днів, на момент закінчення курсу УДХК (відповідно 75,80 ± 30,89 мкмоль/л проти 117,04 ± 47,86 мкмоль/л у дітей, які не отримували Укрлів® суспензію; р < 0,05). У цьому ж віці встановлено також вірогідну відмінність між групами і за сироватковими концентраціями прямого білірубіну (відповідно 4,3 [0,6–9,1] мкмоль/л проти 10,5 [9,65–44,6] мкмоль/л; р < 0,05). У немовлят, які отримували препарат УДХК, спостерігалось стале зниження сироваткових концентрацій прямого білірубіну в динаміці спостереження (рисунок 1).
Інтенсивніше зменшення рівня загального білірубіну в сироватці крові немовлят з основної групи визначало коротший період клінічно явної жовтяниці (7,5 [6–11] дня проти 10,0 [7,5–11,5] дня; р > 0,05) і незначно меншу тривалість фототерапії (відповідно 5,53 ± 1,61 дня проти 6,25 ± 1,73 дня; р > 0,05).
Лікування з використанням Укрлів® суспензії супроводжувалось зменшенням активності трансаміназ і незначним зростанням активності лужної фосфатази, однак динаміка жодного показника не була вірогідною (рисунок 2).
В абсолютній більшості випадків рівні активності ТА і ЛФ коливались у фізіологічних межах. Активність ЛФ, що в недоношених немовлят є не лише маркером холестазу, а й відображає особливості метаболізму кісткової тканини [18], типово зростала протягом перших 2 тижн. життя, після чого починала знижуватись (рисунок 2б). Аналогічні дані стосовно динаміки ТА і ЛФ попередньо отримано іншими авторами, які також зробили висновок, що призначення УДХК забезпечує раннє і стабільне зниження рівня білірубіну в передчасно народжених дітей із холестазом, асоційованим із тривалим парентеральним харчуванням [12].
Ми не визначали в наших пацієнтів активності y-глутамілтранспептидази — мікросомального ферменту, що вважається найбільш раннім і специфічним маркером холестазу [19]. Однак іншими дослідниками було продемонстровано здатність УДХК зменшувати активність цього ферменту в недоношених новонароджених перших тижнів життя, які перебували на парентеральному харчуванні, що пов’язували з можливістю профілактики холестазу [14, 15]. Значне і стале зниження концентрації загального і прямого білірубіну на тлі позитивної динаміки ферментативної активності в наших пацієнтів також свідчать на користь того, що використання Укр–лів® суспензії у комплексному лікуванні недоношених немовлят із гіпербілірубінемією може запобігати виникненню холестазу, пов’язаного з недостатнім об’ємом ентерального харчування, незрілою або порушеною функцією печінки і/або підвищеним умістом білірубіну в сироватці крові.
Як і в інших дослідженнях, препарат УДХК добре переносився немовлятами, ми не бачили будь–яких побічних ефектів його призначення.
Таким чином, додаткове призначення передчасно народженим немовлятам із гіпербілірубінемією (рівень загального білірубіну сироватки крові > 225 мкмоль/л) наприкінці першого тижня життя Укрлів® суспензії в дозі 5 мг/кг кожні 6 год упродовж 14 днів забезпечує інтенсивніше зменшення концентрацій загального і прямого білірубіну в сироватці крові, скорочення загальної тривалості жовтяниці, а також позитивну динаміку сироваткової активності трансаміназ і лужної фосфатази.
Отримані результати дозволяють зробити висновок про доцільність застосування УДХК у комплексному лікуванні гіпербілірубінемій у передчасно народжених немовлят.
1. Cashore W.J. Bilirubin and jaundice in the micropremie // Clin. Perinatol. — 2000. — V. 27. — P. 171–179.
2. Watchko J.F. Enduring controversies in the management of hyperbilirubinemia in preterm neonates / J.F. Watchko, M.J. Maisels // Seminars in Fetal & Neonatal Medicine. — 2010. — V. 15. — P. 136–140.
3. Maisels M.J. Treatment of jaundice in low birthweight infants / M.J. Maisels, J.F. Watchko // Arch. Dis. Child Fetal. Neonatal. Ed. — 2003. — V. 88. — P. 459–463.
4. Maisels M.J. Phototherapy — traditional and non–traditional // J. Perinatol. — 2001. — V. 21. — P. S93–S97.
5. Aggressive vs. conservative phototherapy for infants with extremely low birth weight / B.H. Morris, W. Oh, J.E. Tyson [et al.] // N. Engl. J. Med. — 2008. — V. 359. — P. 1885–1896.
6. American Academy of Pediatrics. Subcommittee on hyperbilirubinemia. Clinical practice guideline: management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation // Pediatrics. — 2004. — V. 114. — P. 297–316.
7. National Collaborating Centre for Women’s and Children’s Health. Neonatal jaundice. London (UK): National Institute for Health and Clinical Excellence (NICE); 2010 May. — 53 p. (Clinical guideline; no. 98)
8. Sugama S. Magnetic resonance imaging in three children with kernicterus / S. Sugama, A. Soeda, Y. Eto // Pediatr. Neurol. — 2001. — V. 25. — P. 328–331.
9. Kernicterus in preterm infants / A. Okumura, H. Kidokoro, H. Shoji [et al.] // Pediatrics. — 2009. — V. 123. — P. e1052–e1058.
10. Bhutani V.K., Johnson L.H., Shapiro S.M. Kernicterus in sick and preterm infants (1999–2002): a need for an effective preventive approach / V.K. Bhutani, L.H. Johnson, S.M. Shapiro // Semin. Perinatol. — 2004. — V. 28. — P. 319–325.
11. Serial brain MRI and ultrasound findings: relation to gestational age, bilirubin level, neonatal neurologic status and neurodevelopmental outcome in infants at risk of kernicterus / K. Gkoltsiou, M. Tzoufi, S. Counsell [et al.] // Early Hum. Dev. — 2008. — V. 84. — P. 829–838.
12. Parenteral nutrition–associated cholestasis in preterm neonates: evaluation of ursodeoxycholic acid treatment / A. Levine, A. Maayan, R. Shamir [et al.] // J. Pediatr. Endocrinol. Metab. — 1999. — V. 12. — P. 549–553.
13. Ursodeoxycholic acid (UDCA) therapy in very–low–birth–weight infants with parenteral nutrition associated cholestasis / C.Y. Chen, P.N. Tsao, H.L. Chen [et al.] // J. Pediatr. — 2004. — V. 145. — P. 317–321.
14. A controlled trial of erythromycin and UDCA in premature infants during parenteral nutrition in minimizing feeding intolerance and liver function abnormalities / T. Gokmen, S.S. Oguz, S. Bozdag [et al.] // J. Perinatol. — 2012. — V. 32. — P. 123–128.
15. Ursodeoxycholic acid treatment in preterm infants: a pilot study for the prevention of cholestasis associated with total parenteral nutrition / S. Arslanoglu, G.E. Moro, H.–D. Tauschel, G. Boehm // J. Pediatric Gastroenterol. and Nutrition. — 2008. — V. 46. — P. 228–231.
16. Rodrigues C.M.P. The therapeutic effects of ursodeoxycholic acid as an anti–apoptotic agent / C.M.P. Rodrigues, C.J. Steer // Expert Opin. Invest. Drugs. — 2001. — V. 10. — P. 1243–1253.

/47/47.jpg)
/48/48_2.jpg)
/48/48.jpg)
/49/49.jpg)