Значна поширеність і зростання захворюваності на цукровий діабет (ЦД) дозволили експертам ВООЗ визнати наявність епідемії неінфекційного характеру. Загальна кількість людей із ЦД збільшиться, за прогнозом експертів Міжнародної діабетичної федерації, з 463 млн у 2019 році до 578 млн у 2030 році та 700 млн в 2045 році [1]. У багатьох країнах світу питанням організації допомоги хворим на ЦД належить особлива роль, адже це захворювання є моделлю для відпрацювання нових підходів у забезпеченні наступності первинної і спеціалізованої медичної допомоги людям із хронічною патологією. Крім того, останніми роками у світі відзначаються істотні зміни вікової структури населення. Найбільш характерним демографічними явищем сучасної епохи залишається прогресуюче зістарення людей. На цей час на планеті проживає 8,5 % людей (617 млн) віком понад 65 років, а за прогнозами, до 2050 року цей показник збільшиться до 17 % населення (1,6 млрд) [www.nia.nih.gov/news/worlds-older-population-grows-dramatically]. При збільшенні віку значно зростає поширеність ЦД 2-го типу, чому сприяє і більша тривалість життя населення. За даними 9-го видання Атласу діабету Міжнародної діабетичної федерації (2019), 20 % людей віком понад 65 років мають ЦД [1]. Отже, коли йдеться про ЦД 2-го типу, ні у когоё не виникає сумнівів, що це масштабне багатофакторне захворювання — одна з найсерйозніших медико-соціальних і економічних проблем сучасної охорони здоров’я.
Прогресування при ЦД макроваскулярних (ішемічна хвороба серця, цереброваскулярна хвороба, хронічні облітеруючі захворювання периферичних артерій) і мікроваскулярних (діабетична ретино-, нефро- і нейропатія) ускладнень виводить цю патологію на третє місце серед причин смертності після серцево-судинної та онкологічної патології. Смертність від серцево-судинних причин у хворих на ЦД 2-го типу втричі вища, ніж у популяції загалом. В умовах пандемії COVID-19 хворі на ЦД 2-го типу більш вразливі до зараження й тяжчого перебігу патології [2].
При встановленні діагнозу ЦД понад 50 % хворих уже мають мікро- і макросудинні діабетичні ускладнення, а вартість амбулаторної медичної допомоги за наявності ускладнень зростає від 3 до 13 разів [3]. Тільки рання ефективна багатофакторна терапія ЦД здатна забезпечити довгострокові переваги для пацієнтів.
Мета лікування ЦД 2-го типу — безпечне досягнення метаболічного контролю, тобто підтримання оптимальних для пацієнта цільових значень глікемії, показників ліпідного обміну і цифр артеріального тиску (АТ). При цьому обов’язковий індивідуальний підхід до лікування хворих.
Розглядаючи результати міжнародних і вітчизняних досліджень, а також враховуючи тривалий власний досвід лікування пацієнтів із ЦД, на підставі сучасних настанов та алгоритмів [4, 5] можна подати деякі підсумки.
Підходи до вибору цукрознижувальної терапії для досягнення ідеального глікемічного статусу змінюються з огляду на появу нових даних про патогенез ускладнень ЦД. На сьогодні прийнята концепція індивідуалізації цукрознижувальної терапії, тобто підбору схеми лікування з урахуванням відомостей про конкретного пацієнта, особливостей перебігу й ризику розвитку діабетичних ускладнень. При цьому на перший план, крім ефективності цукрознижувальної дії, виходить безпека здійснюваної терапії, насамперед щодо частоти й тяжкості гіпоглікемій. Рішення про вибір препарату для ініціації цукрознижувальної терапії приймається клініцистом у кожному конкретному випадку виходячи з індивідуального статусу пацієнта.
Сучасне управління захворюванням передбачає низку заходів: навчання й самоконтроль, досягнення цільових показників вуглеводного обміну без ризику гіпоглікемії, корекція факторів ризику розвитку серцево-судинних захворювань (ССЗ), зниження маси тіла. Воно передбачає індивідуальний підхід до визначення цільових рівнів показників і вибору антигіперглікемізуючого препарату. Пріоритетом у його виборі є ефективність і безпека щодо ризику розвитку гіпоглікемії, а також відсутність впливу на масу тіла, зручність прийому, доступність, наявність плейотропних ефектів, тривалість позитивного ефекту, сприятливий вплив на перебіг ЦД.
З огляду на збільшення частки людей похилого віку лікування ЦД 2-го типу в цій віковій категорії є однією з важливих медико-соціальних проблем. Антигіперглікемізуюча терапія в цій популяції становить труднощі через підвищений ризик гіпоглікемії, наявність поліорганної і коморбідної патології, що істотно впливає на перебіг ЦД 2-го типу. У пацієнтів із ЦД 2-го типу похилого віку частіше діагностують такі супутні ССЗ, як артеріальна гіпертензія, порушення серцевого ритму, ішемічна хвороба серця, цереброваскулярні розлади. На тлі менеджменту як ЦД 2-го типу, так і коморбідної патології формується проблема поліпрагмазії [6].
У пацієнтів із ЦД 2-го типу старшої вікової категорії набагато частіше, ніж у літніх осіб без цього захворювання, відзначаються когнітивні порушення. Зазвичай вони полягають у швидкій втомлюваності, неадекватних емоційних реакціях, погіршенні пам’яті, уваги, більш повільному засвоєнні нових навичок тощо. На поступове прогресування когнітивної дисфункції впливають тривалість ЦД 2-го типу, незадовільний контроль глікемії, явища гіпоглікемії [7]. Важливо підкреслити, що когнітивна дисфункція є фактором низької прихильності людини до будь-якої терапії (у тому числі цукрознижувальної), погіршення глікемічного контролю, що, безумовно, потребує простішої схеми лікування. Раціональна, безпечна щодо гіпоглікемій цукрознижувальна терапія уповільнює процес розвитку когнітивної дисфункції.
До 25–35 % хворих на ЦД 2-го типу в літньому віці страждають від епізодів депресії, що значно перевищує аналогічний показник у загальній популяції. Наявність депресивних станів погіршує глікемічний контроль, що обумовлено зниженням фізичної активності, збільшенням маси тіла, а також недостатнім виконанням рекомендацій лікарів.
У людей літнього й похилого віку (частіше жінок) нерідко спостерігається нетримання сечі, що також негативно впливає на якість життя. T.V. Huyen у своєму дослідженні за участю 322 пацієнтів із ЦД 2-го типу (середній вік 74,80 ± 8,28 року) виявив значну поширеність нетримання сечі (65,2 %). Встановлено, що похилий вік, тривалість ЦД 2-го типу, рівень глікемії натще, глікованого гемоглобіну (HbA1c), когнітивні порушення й наявність поліпрагмазії пов’язані з підвищеним ризиком розвитку нетримання сечі в літніх хворих із ЦД 2-го типу [8].
З віком збільшується ризик зневоднення, чому сприяють зменшення кількості води в організмі на тлі старіння, зниження порогу сприйняття спраги в гіпоталамусі, зміни й хвороби сечовидільної системи. Хронічна гіперглікемія, поліурія додатково можуть посилювати порушення водного балансу в пацієнтів із ЦД 2-го типу.
Літні пацієнти з ЦД 2-го типу схильні до вищого ризику розвитку гіпоглікемії порівняно з особами більш молодого віку. Добре відомо, що вік пацієнта сам по собі є важливим фактором ризику гіпоглікемії. Згідно з результатами досліджень ACCORD і ADVANCE, на кожен додатковий рік життя частота тяжкої гіпоглікемії збільшується на 3 і 5 % відповідно. Особливо високий ризик гіпоглікемії відзначається в осіб старечого віку. Гіпоглікемії в будь-якому віці збільшують ризик кардіоваскулярної і загальної смертності, але зазвичай особливо чутливими залишаються пацієнти літнього й старечого віку, для яких навіть легка або безсимптомна гіпоглікемія є серйозною небезпекою. Гіпоглікемічні епізоди можуть мати несприятливі наслідки не лише для серцево-судинної системи (гострий інфаркт міокарда, інсульт, гіпертонічний криз, порушення серцевого ритму); вони часто супроводжуються падіннями та їх наслідками (переломи, травми голови, субдуральні гематоми тощо), погіршують когнітивну функцію, сприяють деменції [9].
Лікування ЦД 2-го типу потребує ретельного розгляду супутніх синдромів і станів, які збільшують ризик ускладнень. Однак, окрім урахування небезпеки гіпоглікемії в літньому віці, глікемічний контроль залишається важливим чинником запобігання діабетичним ускладненням (часто летальним), продовження життя, а також покращання якості життя. Відомо, що ризик розвитку макросудинних ускладнень у літніх пацієнтів значно вищий, ніж у хворих молодого й середнього віку із ЦД 2-го типу [10]. На сьогодні все ще обмежена кількість опублікованих досліджень з вивчення впливу антигіперглікемізуючої терапії на серцево-судинні та інші ускладнення, смертність у цій популяції пацієнтів. Зокрема, навіть у дослідження UKPDS не були включені особи віком понад 65 років.
До цукрознижувальних препаратів, що застосовуються в осіб похилого віку, висуваються особливі вимоги: мінімальний ризик розвитку гіпоглікемії, серцево-судинна безпека, відсутність нефро-, гепатотоксичності, простий, зручний режим прийому; побічні ефекти терапії повинні бути незначними [11]. До того ж у літніх хворих значно частіше трапляється хронічна хвороба нирок (ХХН), що обмежує вибір цукрознижувального препарату. При цьому також слід враховувати супутні захворювання і способи їх лікування.
У клінічній практиці для визначення HbA1c у більшості випадків пацієнти змушені самостійно оплачувати дане дослідження. Крім того, з цієї причини для контролю глікемії використовуються глікемічний профіль або епізодичне визначення глюкози натще, що призводить до збільшення частоти як гіпер-, так і гіпоглікемічних станів. У більшості пацієнтів відсутня адекватна оцінка цукрознижувальної терапії, оскільки її корекція нерідко проводиться на підставі епізодичного визначення рівня глікемії (табл. 1).
Незалежно від вибору лікарського препарату зміна способу життя хворого є головним чинником і повинна супроводжувати будь-який варіант терапії. Модифікація способу життя і гіпокалорійне харчування неодмінно сприятимуть зниженню маси тіла, зменшенню інсулінорезистентності і, відповідно, покращанню глікемічного контролю. Крім позитивного впливу на зазначені показники, схуднення й фізичні навантаження покращують прогноз щодо супутньої серцево-судинної патології, зменшуючи такі чинники ризику, як артеріальна гіпертензія, атерогенний профіль ліпідів крові тощо. Важливим аспектом менеджменту ЦД є формування в пацієнта навичок самоконтролю, адже людина з ЦД має вміти розпізнавати та вчасно усувати явища гіпоглікемії, а також змінювати терапію під керівництвом медичного персоналу для досягнення цільового рівня глікемії і HbA1c.
На початку медикаментозної терапії ЦД 2-го типу госпіталізація в стаціонар потрібна лише в окремих ситуаціях, коли його маніфестація супроводжується тяжкими метаболічними порушеннями: вираженим зниженням маси тіла, спрагою, поліурією, діабетичним кетоацидозом, гіперосмолярністю. В інших випадках ініціацію і корекцію терапії можна здійснювати в амбулаторних умовах.
Ініціація цукрознижувальної терапії — одне з актуальних питань сучасної діабетології. Загалом пропонується 3 основні варіанти стартової терапії ЦД залежно від рівня HbA1c. При рівні HbA1c, що не перевищує 7,5 %, рекомендується розпочинати лікування зі зміни способу життя й монотерапії метформіном. При виборі конкретного препарату слід виважено враховувати потенційну швидкість зниження HbА1с, очікувані віддалені переваги, безпеку, а також можливі побічні ефекти, переносимість, прихильність пацієнта до лікування й неглікемічні ефекти.
Препаратом першого вибору, згідно з практично всіма сучасними керівництвами, є метформін. Індивідуальний підхід до хворого і, відповідно, визначення індивідуального цільового рівня НbА1с лежать в основі вибору стратегії цукрознижувального лікування. Насамперед слід враховувати вік пацієнта, тривалість хвороби, наявність серйозних ускладнень, ризик розвитку тяжких гіпоглікемій. Доведено, що серцево-судинні ускладнення й летальний кінець найчастіше трапляються в пацієнтів із гіпоглікемічними епізодами (особливо з тяжкими гіпоглікеміями). Не підлягає сумніву доцільність встановлення індивідуального цільового рівня цукрознижувальної терапії за показником НbА1с.
Розпочинаючи лікування з невеликої дози (500 мг/добу), можна мінімізувати небажані ефекти метформіну з боку кишкового тракту, повільно збільшуючи дозу препарату протягом декількох тижнів. Використання метформіну обмежується порушенням функції нирок, він протипоказаний при швидкості клубочкової фільтрації (ШКФ) < 30 мл/хв/1,73 м2. Також слід пам’ятати, що добова доза метформіну не повинна перевищувати 1000 мг у разі ШКФ 30–44 мл/хв/1,73 м2.
Стани, які супроводжуються гіпоксією (гостра недостатність мозкового кровообігу, серцева, легенева недостатність, інфаркт міокарда, анемія тощо), печінкова недостатність, хронічний алкоголізм, гострі стани з порушенням функції нирок (дегідратація, гостра інфекція, шок), ацидоз будь-якого генезу є протипоказаннями щодо застосування метформіну [12]. Слід пам’ятати, що в частини хворих тривале лікування метформіном асоціюється зі зниженням сироваткових концентрацій вітаміну В12, що потенційно може призводити до збільшення наявних когнітивних порушень [13].
При непереносимості або наявності протипоказань щодо призначення метформіну альтернативою зазвичай є призначення похідних сульфонілсечовини (ПСС). Також їх найчастіше використовують для інтенсифікації цукрознижувальної терапії в разі неефективності монотерапії метформіном. Як уже зазначалося, вкрай небезпечним побічним ефектом цієї групи цукрознижуючих препаратів для хворих старшої вікової категорії є розвиток гіпоглікемії. Разом з тим показано, що ризик гіпоглікемії залежить від тривалості дії та особливостей метаболізму ПСС [14].
Інгібітори натрій-глюкозного котранcпортера 2, які блокують реабсорбцію глюкози в нирках і збільшують глюкозурію, мають високу ефективність і низький ризик розвитку гіпоглікемічних станів. Згідно з рекомендаціями, в літньому віці слід застосовувати ці препарати з обережністю й уникати поєднання з діуретиками. Необхідний ретельний контроль лікування з огляду на ризик розвитку дегідратації та ортостатичної гіпотонії, а також особлива обережність повинна бути щодо літніх пацієнтів з підвищеним ризиком сечостатевих інфекцій і нетриманням сечі. У нещодавньому метааналізі [15] вказується на відсутність системного огляду стосовно загальної безпеки інгібіторів натрій-глюкозного котранcпортера 2 (порівняно з плацебо) при їх використанні в клінічних умовах.
Концепція зниженого ефекту інкретинів при ЦД 2-го типу стала підґрунтям для впровадження в клінічну практику інгібіторів дипептидилпептидази-4 (іДПП-4) [16]. З моменту появи в клінічній практиці іДПП-4 увага до них не слабшає. Наявність у іДПП-4 передбачуваного цукрознижувального ефекту без ризиків гіпоглікемій, доброї переносимості, сприятливого серцево-судинного потенціалу дозволяє широко використовувати їх у пацієнтів з ЦД 2-го типу літнього й похилого віку [17]. При цьому в пацієнтів похилого віку, крім метформіну, перевагу мають препарати з групи іДПП-4, які відзначаються найбільш сприятливим профілем безпеки, у тому числі щодо розвитку гіпоглікемії.
Механізм дії іДПП-4 полягає в пригніченні активності ферменту ДПП-4, завдяки чому сповільнюється руйнування глюкагоноподібного пептиду 1 (ГПП-1) і глюкозозалежного інсулінотропного поліпептиду (ГІП), пролонгується взаємодія цих гормонів зі специфічними рецепторами і дія на рівні органів-мішеней [18]. Для клінічної практики важливо, що іДПП-4 мають глюкозозалежний механізм дії, завдяки чому їх прийом асоційований з низьким ризиком гіпоглікемії. Це є незаперечною перевагою для осіб похилого віку, особливо з макросудинною патологією, пацієнтів з високим ризиком гіпоглікемії (наприклад, при ХХН).
Усе ще залишається відкритим питання про можливі плейотропні ефекти іДПП-4, незалежні від впливу на глікемію. Вони можуть мати певне клінічне значення для запобігання розвитку хронічних ускладнень ЦД 2-го типу і привести до покращання прогнозу захворювання. Інгібування ГПП-1 і ГІП за допомогою ДПП-4 — це не єдиний процес, де задіяний цей фермент. До його субстратів належать ще й інші молекули, у тому числі нейропептиди, хемокіни, вазоактивні пептиди, цитокіни (нейропептид Y, пептид Y, стромальний клітинний фактор 1α/SDF-1α і 1β/CXCL12, хемотаксичний білок гранулоцитів-2/CXCL6, макрофагальний хемокін CCL22/MDC тощо), які беруть участь у різних біологічних процесах, серед яких особливо важливі запальні, імунні реакції, регенерація, чутливість тканин до інсуліну.
Поряд з контролем глікемії зазначені ефекти в довгостроковій перспективі можуть позитивно впливати на кардіопротективні механізми [19]. Опубліковані відомості про здатність іДПП-4 покращувати ендотеліальну функцію, збільшувати кількість і активність ендотеліальних клітин, знижувати концентрації прозапальних маркерів, вираженість окислювального стресу, зменшувати альбумінурію [20].
Разом з тим оцінка і аналіз реальної клінічної практики лікування ЦД 2-го типу дозволяють дізнатися пріоритети лікарів у виборі тактики для пацієнтів похилого й старечого віку з огляду на різноманітність цукрознижувальних засобів.
На підставі даних, отриманих за допомогою електронної бази США (MarketScan, Medicare Supplemental Database), ініційовано дослідження з метою отримання інформації про рутинну практику ведення хворих на ЦД 2-го типу похилого віку на старті цукрознижувальної терапії [21]. Критеріями включення пацієнтів було підтвердження діагнозу ЦД 2-го типу, вік понад 65 років, наявність електронної карти пацієнтів у базі даних не менше від одного року до початку призначення цукрознижуючих препаратів. У дослідження не включали пацієнтів, які отримують ін’єкційну цукрознижувальну терапію. Пацієнти (n = 155 388) були розподілені на три категорії залежно від лікування: початок монотерапії, перехід до подвійної і потрійної комбінованої терапії.
Оцінка структури цукрознижувальної терапії, призначеної вперше хворим із ЦД 2-го типу, показала, що більшості (52,1 %, n = 80 929) була призначена монотерапія. Аналіз цукрознижувальної терапії у хворих, які раніше отримували таку терапію, показав, що 36,8 % (n = 57 206) пацієнтів призначали подвійну цукрознижувальну терапію, з них іДПП-4 — 7652 пацієнтам. Потрійна цукрознижувальна терапія використовувалася в 11,1 % (n = 17 253), з них іДПП-4 — у 4429 пацієнтів. У рамках кожної категорії цукрознижувальної терапії проводилося порівняння іДПП-4 з іншими цукрознижувальними препаратами в пацієнтів різних вікових груп: 65–74 роки, 75–84 роки і понад 85 років.
У хворих кожної групи детально аналізували супутні захворювання й стани (аритмія, застійна серцева недостатність, інсульт/транзиторні ішемічні атаки, когнітивні дисфункції, переломи, втрата слуху, артеріальна гіпертензія, інфаркт міокарда, нейропатія, захворювання периферичних судин, протеїнурія, ниркова недостатність, ретинопатія, захворювання очей, гіпоглікемія), зареєстровані протягом 12 місяців до дати початку або посилення цукрознижувальної терапії.
У результаті встановлено пріоритети лікарів у виборі пероральних антигіперглікемізуючих препаратів у літніх пацієнтів: іДПП-4 без вагань призначали літнім пацієнтам включно з особами похилого віку, а також тим, хто мав тяжку супутню патологію в анамнезі (аритмії, застійна серцева недостатність, ниркова недостатність, інсульт).
Це дослідження з великою вибіркою пацієнтів дозволило отримати цінні дані про реальну клінічну практику, яка сформувалася при лікуванні пацієнтів із ЦД 2-го типу похилого віку.
Певний інтерес становлять результати нещодавно опублікованого відкритого дослідження за участю 115 пацієнтів похилого віку, у якому оцінювали не тільки ефективність іДПП-4, але й задоволеність пацієнтів лікуванням, використовуючи «Опитувальник задоволеності лікуванням при діабеті» (Diabetes Treatment Satisfaction Questionnaire, DTSQ) [22]. У цьому моноцентровому перехресному порівняльному обсерваційному дослідженні хворі похилого віку із ЦД 2-го типу (які отримували цукрознижувальні препарати не менше ніж три місяці до включення в дослідження) були розділені на дві групи терапії.
Група 1 (n = 42, середній вік 64,9 ± 5,6 року) отримувала іДПП-4 у вигляді монотерапії або у складі комбінованої терапії (метформін, ПСС, піоглітазон, інсулін), група 2 (n = 73, середній вік 63,5 ± 3,5 року) отримувала інші цукрознижувальні препарати (крім іДПП-4) у вигляді монотерапії (метформін, ПСС, піоглітазон, інсулін) або у складі комбінованої терапії.
Через два місяці лікування між групами була отримана статистично значуща різниця за рівнем HbA1c (група 1 — 7,07 ± 1,22 %, група 2 — 7,68 ± 1,48 %; p = 0,034). Різниці за рівнем HbA1c між різними препаратами з групи іДПП-4 не було відзначено. Крім того, вірогідно більше пацієнтів групи 1 досягли HbA1c < 7 % порівняно з групою 2 (62 і 33 % відповідно; р = 0,002; 95% ДІ 11,8–48,1 %). Важливо відзначити, що, згідно з опитувальником DTSQ, відзначена статистично значуща позитивна динаміка задоволеності лікуванням у групі 1.
Порушення функції нирок є додатковим фактором, який сприяє виникненню частих гіпоглікемій, обмежує у виборі препаратів через протипоказання до терапії, що значно ускладнює лікування будь-якого захворювання. При зниженні ШКФ неухильно зростає число коморбідних станів, і цей взаємозв’язок особливо відчутний саме у хворих на ЦД 2-го типу старших вікових груп. Наявність ХХН значно погіршує прогноз життя в цих пацієнтів, визначає високу ймовірність фатальних серцево-судинних ускладнень. Крім того, альбумінурія і зниження ШКФ виступають незалежними предикторами дисфункції головного мозку в літньому віці. Особливості фармакокінетики вілдагліптину: 85 % дози виводиться із сечею і 15 % дози — з калом, ниркове виведення незміненого вілдагліптину становить 23 % від перорально прийнятої дози [23, 24].
Рання комбінована терапія вілдагліптином і метформіном у пацієнтів із ЦД 2-го типу
Останнє дослідження VERIFY оприлюднене у вересні 2019 року в Барселоні на 55-й конференції Європейської асоціації з вивчення діабету (European Association for the Study of Diabetes, EASD) професором Девідом Метьюзом (David Matthews), президентом EASD і почесним професором медицини Оксфордського університету, Велика Британія (University of Oxford, UK). «Результати дослідження VERIFY однозначно демонструють, що рання комбінована терапія гарантує більш значущі й довгострокові переваги для пацієнтів порівняно з рекомендованим нині методом стартової монотерапії з подальшою інтенсифікацією при лікуванні пацієнтів із ЦД 2-го типу», — сказав професор Девід Метьюз [25].
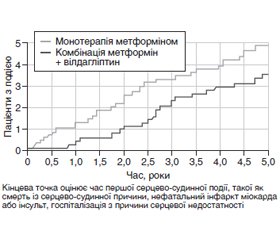
VERIFY — унікальне п’ятирічне подвійне сліпе багатоцентрове рандомізоване плацебо-контрольоване клінічне дослідження довгострокових результатів ранньої комбінованої терапії вілдагліптином і метформіном. Дослідження проводилося на базі 254 центрів 34 країн світу за участю 2001 пацієнта різної етнічної приналежності з первинно виявленим ЦД 2-го типу, які раніше не отримували лікування (рівень HbA1c від 6,5 до 7,5 %) або отримували метформін не більше ніж 1 місяць (рис. 1).
/38.jpg)
Пацієнти були розділені на дві групи: перша отримувала терапію метформіном + плацебо, друга — комбінацію метформіну з вілдагліптином. Основним критерієм дослідження був час до невдачі терапії і необхідності переходу на інсулінотерапію. При першій невдачі терапії (HbAlс > 7 % за двома вимірюваннями поспіль) пацієнтів першої групи переводили на терапію метформін + вілдагліптин, при повторній невдачі — переводили на інсулінотерапію. У пацієнтів другої групи (метформін + вілдагліптин) декомпенсацію (HbAlс > 7 % за двома вимірюваннями поспіль) у подальшому також коригували інсулінотерапією згідно з локальними протоколами. У дослідженні VЕRIFY (NCT01528254) ранньої комбінованої терапії вілдагліптином (50 мг 2 рази/добу) і метформіном (1000–2000 мг/добу) була досягнута первинна кінцева точка зі статистично значущим 49% зменшенням відносного ризику (ВР) за часовим інтервалом до моменту настання неефективності комбінованої терапії (визначалася за рівнем HbAlс ≥ 7,0 %, вимірюваним двічі з інтервалом 13 тижнів) порівняно з монотерапією метформіном (BP 0,51; 95% довірчий інтервал (ДІ) 0,45–0,58; p < 0,0001).
/38_2.jpg)
Стратегія ранньої комбінованої терапії також показала нижчу частоту повторної невдачі, оцінювану в період, коли всі пацієнти отримували комбіноване лікування (BP 0,74; 95% ДІ 0,63–0,86; p < 0,0001). У пацієнтів, які отримували ранню комбінацію метформіну з вілдагліптином, відзначалися нижчі рівні HbA1с (< 6,0; < 6,5 або < 7,0 % залежно від цільових значень) протягом 5 років порівняно з тими, кому комбінована терапія була призначена тільки після втрати контролю вуглеводного балансу при невдалій монотерапії метформіном.
Хоча дослідження VERIFY не було дослідженням з оцінки ризику серцево-судинних подій, проте спостереження показало користь раннього комбінованого лікування метформіном з вілдагліптином порівняно з монотерапією метформіном [29].
Отже, рання комбінована терапія вілдагліптином з метформіном на 49 % знижує ризик втрати глікемічного контролю, перевершує стратегію поетапної інтенсифікації, забезпечує стійкий контроль HbA1с протягом 5 років, стабільно нижчий рівень HbA1c, що особливо важливо в перший рік терапії для уповільнення прогресування ускладнень ЦД 2-го типу. 75 % пацієнтів на ранній комбінованій терапії вілдагліптином з метформіном досягають рівня HbA1с < 6,5 % уже через 3 місяці й утримують його не менше ніж рік, 54 % пацієнтів — на поетапній терапії. Отже, рання комбінована терапія вілдагліптином і метформіном у пацієнтів із ЦД 2-го типу має переваги над стратегією поетапної інтенсифікації [26–28].
Висновки
Останніми роками відбуваються істотні зміни в підходах до лікування пацієнтів із ЦД 2-го типу. Сучасні знання про патогенетичні механізми ЦД 2-го типу дозволяють запропонувати нові схеми лікування.
В арсеналі ендокринологів на сьогодні є широкий перелік цукрознижувальних препаратів. Зміна парадигми лікування ЦД 2-го типу з глюкоцентричної на пацієнт-орієнтовану передбачає пошук оптимальної лікувальної тактики, у тому числі щодо впливу на ниркову функцію.
У менеджменті ЦД 2-го типу, у тому числі з коморбідною патологією, важлива роль належить терапії іДПП-4. Препарати цієї групи добре вивчені, з доведеним низьким ризиком гіпоглікемії, зі сприятливим профілем переносимості, що дозволяє покращити прогноз захворювання.
Першим вітчизняним генериком вілдагліптину в Україні є препарат Гліптар, таблетки по 50 мг, виробництва АТ «Київмедпрепарат», виготовлений із якісної європейської субстанції. Препарат Гліптар співставний за ефективністю й безпекою з оригінальним, що дозволяє широко застосовувати його для лікування пацієнтів із ЦД 2-го типу в Україні.
Конфлікт інтересів. Не заявлений.
/38_2.jpg)

/38.jpg)