Вступ
Найбільш активно в сучасних умовах розвивається напрям медицини, що базується на оцінці рівня здоров’я з точки зору теорії адаптації. Стан здоров’я розглядається як здатність організму адаптуватися до умов зовнішнього середовища, а хвороба — як стрес і порушення адаптації [1–5]. Останніми десятиліттями в усьому світі відмічається посилення ролі психосоціальних чинників у порушенні здоров’я населення, а також зростання кількості хвороб адаптації (психосоматичних розладів або психосоматозів). До категорії цих захворювань відносять гастроентерологічну патологію. Більшість вітчизняних і зарубіжних фахівців, які займаються питаннями патофізіології захворювань шлунково-кишкового тракту (ШКТ), приходять до висновків, що порушення з боку нервової системи носять психовегетативний характер з переважним порушенням на рівні центральної ланки вегетативної регуляції. Іншою особливістю вегетативної дисфункції є її полісистемний характер, в рамках якого відзначається порушення вегетативного регулювання роботи травної системи, що призводить до порушення адаптаційних механізмів в цілому [6]. Отримані дані підтверджують думку вчених про те, що вегетативна дисфункція практично ніколи не обмежується одним органом і системою. Значна варіабельність результатів, отриманих при вивченні стану вегетативної нервової системи (ВНС) у гастроентерологічних хворих, може бути пов’язана з високою мінливістю вегетативної сфери в цілому і застосуванням різних методик для оцінки її функціонального стану. Наприклад, у хворих на виразкову хворобу дванадцятипалої кишки виявлені складні порушення адаптивної регуляції, що проявляються змінами нейропсихологічного статусу, ерго- і трофотропної систем, вегетативними дисфункціями, гормональними порушеннями, вторинним імунодефіцитом. Стресорний вплив, що нерідко відзначається в анамнезі хворих на виразкову хворобу дванадцятипалої кишки, призводить до значних морфофункціональних порушень в організмі, зокрема в складних взаємодіях нервового і гуморального каналів вегетативної регуляції. На тлі виснаження компенсаторних механізмів, зриву адаптаційних можливостей, який проявляється, зокрема, імунодефіцитом та надмірною симпатикотонією, обтяжується перебіг хвороби і залучаються до патологічного процесу інші органи травної системи [7, 8].
Слід зазначити, що простих інформативних тестів для діагностики порушень вегетативної регуляції ШКТ на сьогодні не існує [9, 10]. Запропоновані методики з визначенням екскреторної і моторно-евакуаторної функції різних відділів ШКТ технічно складні, інвазивні й можуть бути пов’язані не тільки з вегетативним дисбалансом в межах усього організму, але й з окремо виявленою патологією будь-якого органа ШКТ. Стан ентеральної нервової системи можна оцінити тільки морфологічно. Анатомо-фізіологічні особливості ВНС травної системи такі, що зміни в межах одного органа або системи органів призводять до неузгодженості дії вегетативних апаратів інших систем, тому про функціональний стан ВНС при захворюваннях органів травлення часто судять за адекватністю вегетативної регуляції серцево-судинної системи (ССС) [11, 12].
У даний час для оцінки вегетативного статусу організму, крім рекомендацій А.М. Вейна [13], за допомогою яких за вивченням клінічних симптомів і функціональних проб оцінюється вегетативний тонус, вегетативна реактивність і вегетативна забезпеченість, застосовується метод кардіоритмографії, заснований на аналізі структури синусового серцевого ритму, що відкриває можливість до подальшого вивчення цієї проблеми [14].
У даному обзорі наведені сучасні уявлення про варіабельність серцевого ритму (ВСР), розглянуті класичні методи аналізу та можливості клінічного застосування для оцінки адаптаційних можливостей організму, стану ВНС або поточного рівня стресу в гастроентерологічних хворих. Були використані публікації, що містять актуальну інформацію щодо методів вивчення, можливостей оцінки й корекції показників ВСР в обстеженні здорових людей та при різних патологічних станах ШКТ.
Відомо, що в патогенезі хронічних захворювань шлунка та дванадцятипалої кишки поряд з місцевими причинами особливе значення мають порушення нейрогуморальної регуляції [7]. Вони містять в собі вплив з боку центральної нервової системи, ВНС, рефлекторно — з боку патологічно змінених органів черевної порожнини [15–17]. Однак до кінця не визначена роль симпатоадреналової системи і порушення холінергічних процесів як можливих патогенетичних механізмів розвитку хронічних захворювань органів гастродуоденальної зони. ВНС належить найважливіша роль у життєдіяльності організму. Вона підтримує сталість внутрішнього середовища організму та забезпечує різні форми психічної і фізичної діяльності. Зсув вегетативного гомеостазу порушує поведінку людини й обумовлює недостатню адаптацію.
Термін «гомеостаз», вперше сформульований W. Cannon для визначення поняття підтримки динамічної сталості внутрішнього середовища організму, знайшов подальший розвиток із виникненням системного підходу до оцінки стану організму. Вегетативний гомеостаз можна визначити як стабільне функціювання ВНС у фізіологічних межах в період спокою та при фізичних і психічних навантаженнях. Вихід за означені межі свідчить про наявність дисфункції ВНС. В результаті вегетативної дисфункції порушується іннервація внутрішніх органів, в них виникають стереотипні морфологічні зміни (спазм судин, дистрофія), пов’язані з виділенням нейромедіаторів, гормонів кори надниркових залоз, біологічно активних речовин. Ці гуморальні зміни, у свою чергу, поглиблюють вегетативний дисбаланс. Ще в роботах відомого вченого І.П. Павлова відображені механізми зв’язку двох важливих життєзабезпечуючих систем організму — нервової та травної. У сучасних дослідженнях найбільш вивчена роль ВНС у розвитку гострих уражень верхніх відділів ШКТ і, зокрема, виразкової хвороби. Вважається, що симпатичні імпульси викликають підвищений викид медіаторів (катехоламінів), що призводить до порушення трофіки тканин [18, 19]. Регуляція функцій ШКТ — складний процес, що визначається багатьма факторами, пов’язаними між собою. За даними О.М. Вейна (1998), механізми регуляції ШКТ включають кору та підкоркові утворення, в яких локалізуються вищі центри вісцеральної нервової системи — гіпоталамо-гіпофізарні структури, що здійснюють вплив на функціональний стан травного тракту через ВНС, а також за рахунок гуморальних та ендокринних механізмів. Частіше ВНС розглядають як відносно автономну частину нервової системи, що забезпечує автоматичну діяльність внутрішніх органів та підтримує вісцеральний гомеостаз за допомогою двох її відділів — симпатичного і парасимпатичного. Значного поширення набула теорія адаптаційно-трофічної функції нервової системи, яка доводить, що ВНС — керуюча система-регулятор, яка за допомогою біологічно активних речовин (нейромедіаторів) впливає на структури-мішені (рис. 1) [20].
/83.jpg)
Вегетативні розлади призводять до порушення іннервації внутрішніх органів, в яких виникають функціональні зміни, пов’язані з виділенням нейротрансмітерів, гормонів, біологічно активних речовин. Нейроендокринні зміни, в свою чергу, поглиблюють вегетативний дисбаланс. Значну роль в гуморальній регуляції травних функцій відіграють гастроінтестинальні гормони, які беруть участь в регуляції моторики, секреції, всмоктування, вивільнення інших регуляторних пептидів. Вони продукуються ендокринними клітинами слизової оболонки та являють собою аміни й пептиди. Ці речовини впливають на клітини-мішені по-різному: ендокринним (потрапляють до органів-мішеней загальним і регіонарним кровотоком) і паракринним механізмом (дифундують крізь інтерстиціальну тканину до близько розташованої клітини). Деякі з цих речовин продукуються нервовими клітинами й відіграють роль нейротрансмітерів. Вважають, що ряд гормонів одночасно є нейротрансмітерами та можуть досягати органів-мішеней як із кров’ю, так і нервовим шляхом. Так, пептиди нервового походження (соматостатин, субстанція Р, ендорфіни, енкефаліни) знайдено в клітинах, що продукують гормони ШКТ; холецистокінін, гастрин виявлено в ЦНС та нервових волокнах, що підтверджує тісний зв’язок травної та нервової систем [9]. Спонтанна рухова активність гладких м’язів кишечника зумовлена їх автоматизмом. Відомо два «датчики ритму» кишкових скорочень, один з яких знаходиться біля місця впадання загальної жовчної протоки в дванадцятипалу кишку (ДПК), інший — у клубовій кишці. Організована фазна скоротлива діяльність стінки кишки здійснюється також за допомогою нейронів ауербахівського нервового сплетення, які проявляють ритмічну фонову активність. Ці механізми перебувають під впливом нервової системи та гуморальних чинників. Парасимпатичні нерви в основному збуджують, а симпатичні — гальмують скорочення тонкої кишки. Ефекти подразнення вегетативних нервів залежать від вихідного стану м’язів, частоти і сили подразнення. Гуморальні речовини здійснюють регуляцію моторики кишки, безпосередньо впливаючи на міоцити або на ентеральні нейрони. Стимулюють моторику вазопресин, окситоцин, брадикінін, серотонін, гістамін, гастрин, мотилін, холіцистокінін, речовина Р, гальмують — секретин, вазоактивний інтестинальний поліпептид [21]. Велике значення для регуляції моторики тонкої кишки мають рефлекси з різних відділів травного тракту, які можна розділити на збуджувальні та гальмівні. До збуджувальних рефлексів належать стравохідно-кишковий, шлунково-кишковий і кишково-кишковий, до гальмівних — ректоентеральний, а також рецепторне гальмування тонкої кишки (рецепторна релаксація) під час їжі, яке потім змінюється посиленням її моторики. Рефлекторні дуги цих рефлексів замикаються на рівні як інтрамуральних гангліїв внутрішньоорганного відділу ВНС, так і ядер блукаючих нервів у довгастому мозку й вузлах симпатичної нервової системи. Враховуючи анатомо-фізіологічні особливості травного тракту, відомо, що м’язовий прошарок і судинна система кишечника дуже добре іннервуються гілками симпатичних і парасимпатичних нервів, мають розвинений рецепторний апарат, що, в свою чергу, визначає передумови для лабільності функціонування й можливого кореляційного зв’язку між станом ВНС та патологічним процесом у ШКТ. Регуляція рухової активності товстої кишки здійснюється переважно внутрішньоорганним відділом ВНС: інтрамуральними нервовими сплетеннями (ауербахівським і мейснерівським). У стимуляції моторної діяльності товстої кишки істотну роль відіграють рефлекси при подразненні рецепторів стравоходу, шлунка, тонкої та товстої кишки. Корекція місцевих рефлексів відбувається вищерозташованими центрами ВНС. Симпатичні нервові волокна, які проходять у складі черевних нервів, гальмують моторику; парасимпатичні, такі, що йдуть у складі блукаючих і тазових нервів, підсилюють [22].
Взаємодія між ШКТ і ССС являє собою безперечний інтерес. Захворювання верхнього відділу ШКТ може призводити до функціональних розладів ССС, що виникають опосередковано через ВНС. Далеко не останню роль у формуванні дизрегуляції ВНС відіграють захворювання ШКТ. Згідно з даними [7, 15], підвищення тонусу парасимпатичної нервової системи обумовлено загостренням хронічних захворювань внутрішніх органів (жовчнокам’яна хвороба, кіста стравохідного отвору діафрагми, виразкова хвороба (ВХ)). Порушення динамічної взаємодії між симпатичним і парасимпатичним відділами ВНС, що виникає при гастроезофагеальній рефлюксній хворобі (ГЕРХ) внаслідок постійного патологічного шлунково-стравохідного рефлюксу, призводить до вегетативної дизрегуляції серцевого ритму як шляхом формування патологічного езофагокардіального рефлексу, так і через загальне посилення тонусу вагусного або симпатичного нервів [23]. Визначено, що ГЕРХ пов’язана з підвищеним ризиком розвитку фібриляції передсердь. Як можливий пусковий механізм розвитку фібриляції передсердь при ГЕРХ багато вчених розглядають надлишкову стимуляцію вагуса [24]. Роль порушень вегетативного тонусу в патогенезі рефлюксної хвороби передбачена теоретично так: моторно-тонічні порушення гастродуоденальної зони, наявні при кислотозалежних захворюваннях шлунка, багато в чому пов’язані з розладами ВНС. При дослідженні вегетативного тонусу виявлено, що у 40 % хворих на ГЕРХ спостерігається парасимпатикотонія, у 30 % — ейтонія, у 30 % — симпатикотонія. У 50 % обстежуваних з рефлюксною хворобою визначалися ознаки вегетативної дистонії у вигляді абортивних або розгорнутих (панічні атаки) кризів, що поєднувалися з емоційною лабільністю та астенізацією. Однак у дорослих хворих захворювання було частіше асоційовано з парасимпатикотонією [25], а у дітей з кислим гастроезофагеальним рефлюксом частіше відзначались одночасно ознаки ваготонії та симпатикотонії [24]. За даними інших дослідників, у пацієнтів з ендоскопічно-позитивною ГЕРХ вірогідно частіше зустрічались різноманітні порушення ВНС, тобто механізм розвитку ГЕРХ є відображенням глобальної вегетативної дисфункції у вигляді порушення симпатико-парасимпатичних взаємовідношень, зриву сегментарних і компенсаторного підвищення надсегментарних механізмів регуляції [26]. Також доведено, що хронічний гастрит виникає в результаті виснаження захисних, адаптаційних механізмів, як можливий механізм у формуванні запалення розглядається превалювання парасимпатичної регуляції, що призводить до порушення секреторно-моторної функції шлунка [27]. Порушення трофіки слизової оболонки шлунка пояснюється зниженням активності симпатичної ланки ВНС. При дослідженні стану ВНС при хронічній гастродуоденальній патології (хронічний гастродуоденіт, ВХ шлунка, ВХ дванадцятипалої кишки) отримані суперечливі результати. Вегетативні порушення при ВХ гастродуоденальної зони зустрічаються у 75–82 % хворих [15]. За даними різних авторів, визначаються різноспрямовані вегетативні порушення при ВХ. Одні автори знайшли переважання тонусу парасимпатичного відділу ВНС [16], в інших дослідженнях визначено підвищення тонусу симпатичної нервової системи [28]. У хворих з переважанням симпатичної нервової системи процес загоєння виразок затягується. Деякі автори схиляються до думки, що дисбаланс у ВНС передує виникненню ВХ [7]. При ВХ дванадцятипалої кишки в 33,3 % випадків спостерігалась парасимпатикотонія, особливо у хворих з тривалим анамнезом захворювання і з ускладненим перебігом (75 %). У хворих з коротким анамнезом захворювання (< 5 років), без ускладнень, відзначалася симпатикотонія, що вказує на адекватні адаптаційні можливості організму [29]. Однак цілий ряд сучасних дослідників ставлять під сумнів абсолютну обов’язковість ваготонії при ВХ і відзначають більш часте переважання симпатичного тонусу, високу напругу регуляторних систем на тлі підвищення активності центрального контуру регуляції. M. Nomura зі співавт. [30] оцінювали зв’язок між мінливістю частоти серцевих скорочень та інфекцією Helicobacter pylori (НР). Функцію вегетативної нервової системи вивчали за допомогою добового моніторингу електрокардіограми (ЕКГ) за Холтером. Автори дійшли висновку, що дисфункція ВНС так само, як і інфекція НР, є необхідною умовою для утворення хронічної виразки. Будь-який вид вегетативного дисбалансу може впливати на виникнення рецидиву ВХ. При цьому ваготонія сприяє посиленню агресії, а симпатикотонія — порушенню мікроциркуляції, зниженню секреції слизу і бікарбонатів. Також ВНС є поєднаною ланкою між психікою і соматикою.
Відомий тісний взаємозв’язок між вегетативною регуляцією ШКТ й ССС. Роль вегетативних порушень в патогенезі функціональних захворювань ШКТ, за думкою А.М. Вейна, базується на взаємозв’язку вегетативних порушень з розвитком захворювання, де підкреслюється психовегетативний характер змін (зацікавленість надсегментарних утворень ВНС) [13]. Дослідження, проведені Н. Мазурак, показали, що всі пацієнти з функціональними порушеннями мають вегетативний дисбаланс з превалюванням парасимпатичних впливів [22]. Ряд дослідників підтверджують наявність ваготонії у половини досліджених хворих на синдром подразненого кишечника з підвищенням активності центральних вегетативних структур [31]. Є.М. Кульчицька із співавт., досліджуючи ВСР, довели превалювання парасимпатичних впливів у пацієнтів з діареєю та симпатикотонічних — при формі захворювання із запорами. Зміна якості вегетативного регулювання проявляється в ослабленні автономного контура регуляції (впливів ентеральної нервової системи) й підсиленні впливу вищих вегетативних центрів. За даними деяких вчених, вихідна симпатикотонія та підвищена симпатикотонічна реактивність є несприятливими прогностичними ознаками, поєднаними з більш частими та вираженими загостреннями [10]. Дослідження, проведені за кордоном, частіше демонструють превалювання симпатикотонії на тлі зниження активності парасимпатичного відділу ВНС [32]. Більшість зарубіжних дослідників, так само як і російські фахівці, звертають увагу на централізованість механізмів вегетативних розладів при функціональних розладах кишечника. A.V. Emmanuel et al. продемонстрували зв’язок між характеристиками високочастотного діапазону ВСР і кровотоком слизової оболонки товстої кишки [33]. У дослідженні стану ВНС за допомогою спектрального аналізу ВСР виявлено підвищення потужності спектра дуже низької частоти (VLF-діапазон). Дані зміни розцінюються авторами як посилення впливу центральних структур на функціонування кишечника. Суперечливість даних щодо характеру вегетативної дисфункції при функціональних розладах кишечника призвела до висловлення деякими фахівцями думки про неспецифічність порушень вегетативної сфери.
Оцінка стану організму та його окремих систем протягом багатьох століть аналізувалася пальпаторним визначенням частоти серцевих скорочень. За якістю пульсу діагностували велику кількість хвороб, які навіть не відносяться до ССС. З появою апаратів для отримання та аналізу ЕКГ діагностика вийшла на якісно інший рівень. Наступним етапом розвитку методу є розвиток математичного аналізу суміжних інтервалів RR і знаходження між ними певної залежності.
Аналіз варіабельності серцевого ритму — це сучасна методика, що використовується для визначення вегетативних впливів на серце, а також напруженості регуляторно-адаптаційних механізмів. Зміна ритму серця — універсальна оперативна реакція цілісного організму у відповідь на будь-який вплив зовнішнього середовища. В її основі лежить в першу чергу забезпечення балансу між симпатичною і парасимпатичною нервовою системою. На цьому і ґрунтуються численні методи вивчення ВСР, що оцінює стан механізмів регуляції фізіологічних функцій організму людини, а саме — загальної активності регуляторних механізмів, нейрогуморальної регуляції серця, а також співвідношення між симпатичним і парасимпатичним відділами ВНС [14]. Характерною особливістю методу є його неспецифічність по відношенню до нозологічних форм патології і висока чутливість до різноманітних внутрішніх і зовнішніх впливів. Метод заснований на розпізнаванні та вимірюванні часових проміжків між RR-інтервалами ЕКГ, побудові динамічних рядів кардіоінтервалів (кардіоінтервалограми) з подальшим аналізом отриманих числових рядів різними математичними методами [11].
Дослідження ВСР розпочато в 1965 р., коли дослідники Hon і Lee відзначили, що стану дистресу плода передувала альтернація інтервалів між серцевими скороченнями до того, як відбулися будь-які помітні зміни в серцевому ритмі. Лише через 12 років було виявлено взаємозв’язок високого ризику смерті у хворих, які перенесли інфаркт міокарда, зі зниженою ВСР [34, 35]. Результати Фремінгемського дослідження протягом 4-річного спостереження (736 осіб похилого віку) переконливо довели, що ВСР містить незалежну і прогностичну інформацію, що перебуває за межами традиційних факторів ризику. В 1981 р. Akselrod з колегами використали спектральний аналіз коливань серцевого ритму для кількісного визначення показників серцево-судинної системи від систоли до систоли. В 1996 р. робоча група експертів Європейського товариства кардіологів і Північноамериканського товариства кардіостимуляції та електрофізіології розробила стандарти використання показників ВСР у клінічній практиці та кардіологічних дослідженнях, відповідно до яких нині виконується більшість досліджень. Для визначення ВСР рекомендується використовувати ряд методів, що забезпечують найбільш повний аналіз при мінімальних витратах ресурсів і часу [11, 36].
Уперше ВСР виявив А. Галлер в 1760 р. [11]. В 1932 р. А. Флейш та Р. Бекман описали різні типи хвиль у послідовності RR-інтервалів [14]. За радянських часів математичний аналіз ВСР активно розвивали академік АМН СРСР В.В. Парін та професор Р.М Баєвській з колегами починаючи з 50-х років XX століття, тобто в період становлення космічної медицини [37]. «Друге дихання» цьому методу надало впровадження в клінічну практику і наукові дослідження комп’ютерної техніки. У даний час аналіз ВСР широко використовується в фізіології і медицині, а для його реалізації створені різні медичні діагностичні системи, що дозволяють проводити математичний аналіз результатів.
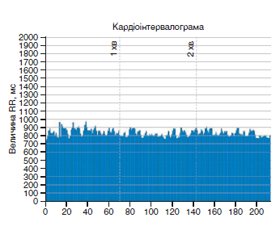
Робота серця, в тому числі частота серцевих скорочень (ЧСС), не є константою та змінюється залежно від зовнішніх і внутрішніх факторів. Саме ці коливання можуть охарактеризувати й вегетативну регуляцію ССС. ВСР можна охарактеризувати як вираженість коливань частоти ЧСС по відношенню до її середньої [4]. Також завдяки ВСР можна визначити ступінь та можливості адаптаційних процесів [2, 3]. На основі динамічного ряду інтервалів RR будується кардіоритмограма, або КРГ [11, 38], тобто діаграма тривалості ряду послідовних кардіоциклу. У КРГ кожен RR-інтервал поданий у вигляді стовпчика, висота якого відповідає тривалості цього інтервалу.
Математична обробка КРГ дозволяє отримати ряд тимчасових, спектральних і геометричних показників, завдяки яким здійснюється об’єктивна оцінка стану ВНС, в тому числі її симпатичного та парасимпатичного відділів (рис. 2).
У даний час існує велика кількість методик аналізу ВСР. Усі їх можна розподілити на три групи: методи часового аналізу (time domain methods), аналіз хвильової структури ритму серця (частотний аналіз, frequency domain methods), нелінійні методи аналізу ВСР (методи аналізу скатерограм) [39, 40].
На практиці найчастіше використовуються такі методики аналізу ВСР:
1. Методи часового аналізу, що складаються із статистичних і геометричних методів, які називаються ще методами варіаційної пульсометрії. Статистичні методи — це математичний аналіз ВСР, при якому розраховуються такі показники: мода (Мо, мс) — значення RR-інтервалу в максимальному розряді гістограми, основний рівень функціонування синусового вузла; амплітуда моди (Амо, %) — процентний вміст кардіоінтервалів у максимальному розряді гістограми; ΔX (мс) — різниця між максимальним і мінімальним значеннями інтервалу RR в гістограмі (ширина підстави інтервальної гістограми) (рис. 3).
/86.jpg)
Показники Мо і АМо відображають активність симпатоадреналової системи, а показник ΔX — рівень парасимпатичної регуляції. Ці показники застосовують для обчислення індексу напруження (ІН), або індексу напруження регуляторних систем, або стрес-індексу (SI). Цей показник запропонований ще в 1973 році Г.И. Сидоренко, а потім його модифікував Р.М. Баєвський та інші [12]. Це відношення ІН = АМо/Мо•2∆Х, що відображає взаємоактивність симпатичного та парасимпатичного відділів ВНС. При домінуванні симпатичної активності чисельник буде зростати, а знаменник зменшуватися, в результаті чого ІН буде зростати. ІН часто використовується для характеристики стресу. Також обчислюються: 1. Стандартне відхилення величин нормальних інтервалів NN — показник SDNN, мс, який використовується для оцінки довгострокових змін ЧСС і активності симпатичного відділу ВНС. SDNN є одним з основних показників ВСР, що характеризують стан механізмів регуляції серцевої діяльності [11, 14]. Його значення вказують на сумарний ефект впливу симпатичного та парасимпатичного відділів ВНС на синусовий вузол. При домінуванні симпатичного впливу на серце його значення зменшується, а при домінуванні парасимпатичного впливу — зростає. 2. RMSSD, мс — квадратний корінь із середнього квадратів різниць величин послідовних пар інтервалів NN. Цей показник характеризує здатність синусового вузла до концентрації ритму, оцінює короткочасні високочастотні зміни ЧСС та залежить від активності впливу парасимпатичного відділу ВНС на ритм серця, відображає синусову аритмію, пов’язану з диханням. При домінуванні симпатичного відділу ВНС на серце його значення знижується, а при домінуванні впливу парасимпатичного — зростає. 3. pNN50, % — відсоток послідовних інтервалів NN, відмінність між якими перевищує 50 мс, характеризує парасимпатичний контур регуляції.
Із геометричних методів наглядним є графік Лоренца — це графічне зображення послідовних пар інтервалів NN у двовимірній системі координат, в результаті чого будується кореляційна ритмограма (скатерограма) (рис. 4).
Даний точковий розподіл є показовим при порушеннях серцевого ритму та провідності, внаслідок чого його форма може змінюватись. Перевагою геометричних методів є легкість сприйняття та наочність. чутливість до якості аналізу серій інтервалів NN. Геометричні методи можуть служити альтернативою статистичним.
Спектральний аналіз дозволяє виявити періодичні складові ВСР [14]. У графічному вигляді частотний спектр періодичних коливань подається у вигляді спектрограми.
/87.jpg)
Спектрограма будується на основі обвідної кривої КРГ (функції варіації ритму) з використанням перетворень Фур’є (рис. 5).
Площа під цим графіком є потужністю КРГ. Прийнято ділити спектрограму на 3 ділянки (діапазони): високочастотні коливання (HF), низькочастотні коливання (LF), дуже низькочастотні коливання (VLF). Спектральний аналіз проводять за допомогою реєстрації таких показників: 1) ТР (total power) — загальна потужність спектра у досліджуваному діапазоні; 2) LF — спектр низької частоти з потужністю спектра 0,05–0,15 Гц. Характеризує активність обох відділів ВНС, більше симпатичного; 3) HF — потужність спектра на частоті 0,15–0,4 Гц. Відображає активність парасимпатичної ВНС; 4) LF/HF — співвідношення низько- і високочастотного компонентів. Використовується як показник балансу симпатичного та парасимпатичного відділів ВНС. Співвідношення LF- і HF-спектра може змінюватись залежно від вегетативної регуляції серця. Слід зазначити, що компоненти спектра вказують не на тонус окремих відділів ВНС, а на їх вплив на ритм серця [36]. У цілому спектральний аналіз ВСР дозволяє оцінити абсолютну й відносну активність симпатичного та парасимпатичного відділів ВНС, а також участь в процесах регуляції серцевого ритму гуморальних факторів. Перевагою спектрального аналізу є його точність відносно вкладу симпатичного або парасимпатичного відділів у ВСР.
Дуже важливо визначати також загальну потужність спектра, який відображає загальну ВСР, або сумарний вплив симпатичного та парасимпатичного відділів ВНС на серцевий ритм, і має той самий фізіологічний сенс, що і SDNN. При цьому збільшення активності симпатичної ланки ВНС, наприклад, при стресі, призводить до зменшення TP, а зростання активності вагальної ланки — до зростання ТР. Загальна потужність спектра відображає загальну варіабельність серцевого ритму, або сумарний вплив СО і ПО на серцевий ритм, і має той самий фізіологічний сенс, що і SDNN. При цьому збільшення активності СО ВНС, наприклад, при стресі, призводить до зменшення TP, а зростання активності ПО — до зростання ТР [41]. За літературними даними, збільшення LF/НF, що відображує симпатичні модуляції та зменшення показника SDNN, є ознакою активації симпатичної нервової системи і високого ризику раптової смерті [36].
Статистичні методи не дозволяють розмежувати вплив кожного відділу ВНС на ритм серця, а з цієї причини не дають можливість оцінити окремо стан різних відділів ВНС, в той час як методи хвильового, або спектрального, аналізу, на думку цих авторів, дозволяють це зробити. Однак на сьогодні не існує жодного конкретного кількісного показника ВСР, в тому числі і серед спектральних показників, які вірогідно характеризували б активність кожного відділу ВНС.
Методика оцінки ВСР у даний момент є чутливим діагностичним методом оцінки стану ВНС через аналіз ритмічності роботи серця як у здорових, так і у хворих на різну патологію. Застосування аналізу ВСР як методу оцінки адаптаційних можливостей організму або поточного рівня стресу становить практичний інтерес для різних галузей медицини. Розвиток донозологічної діагностики дозволив виділити серед практично здорових людей значну кількість осіб з високою й дуже високою напругою регуляторних систем. В осіб із хронічними захворюваннями підвищений ризик зриву адаптації та виснаження функціональних резервів організму може призвести до обтяження хвороби або її ускладнень.
Нещодавно, в 2018 р., в Україні було впроваджено PRECISE-діагностику, за допомогою якої проводиться аналіз ВСР з використанням хмарної технології автоматизованої інтерпретації ЕКГ з аналізом більше 700 параметрів на основі Мінесотського коду [42]. На відміну від решти способів інтерпретації ЕКГ, алгоритм PRECISE замість пошуку та аналізу окремих патернів аналізує кожен міліметр сигналу. Він не пропускає жодного відхилення і має досконалий фільтр перешкод. За допомогою PRECISE-діагностики аналізують стан ВНС, рівень стресу, адаптації та ризику ускладнень гастроентерологічних захворювань. Дані на основі ВСР з 4 до 12 відведень отримують упродовж 5 хвилин. Ця методика має міжнародний сертифікат, доказову базу і, за даними літератури, є високоефективним інструментом моніторингу факторів ризику ускладнень основного захворювання [43, 44]. PRECISE-діагностика впроваджена у науковій і практичній діяльності ДУ «Інститут гастроентерології НАМН України». Відомо, що більшість показників ВСР з використанням різних методик міцно корелюють один з одним, тому в новітній PRECISE-діагностиці аналізується обмежена кількість показників, які найбільш повно й вірогідно дають уявлення про адаптаційний потенціал організму: симпатовагальний баланс HF/LF для визначення вегетативного тонусу, стрес-індекс, RMSSD — квадратний корінь із середнього квадрата різниці величин послідовних пар інтервалів NN, який оцінює рівень адаптації (кількісна оцінка виснаження резервів адаптації); загальну потужність спектра, що відтворює сумарний ефект вегетативного впливу на серцевий ритм усіх рівнів регуляції та свідчить про можливості функціональних резервів організму, стрес-індекс (Stress index, SI), SDNN — стандартне відхилення всіх NN-інтервалів, що свідчить про наявність і вираженість серцево-судинного ризику (СС-ризик) (табл. 1).
/88.jpg)
За допомогою аналізу показників, отриманих при застосуванні PRECISE-діагностики, можна вивчати адаптаційний потенціал організму на основі визначення стресостійкості, функціональних резервів організму, вихідного вегетативного тонусу та можливого СС-ризику, тобто проводиться повна діагностика загального адаптаційного синдрому. Якщо організм гастроентерологічного хворого незалежно від нозологічної ознаки знаходиться у стані порушення адаптації, вегетативного дисбалансу у бік гіперсимпатикотонії, недостатніх компенсаторно-пристосувальних реакцій та підвищеного СС-ризику, то по відношенню до такого хворого в ДУ «Інститут гастроентерології НАМН України» застосовуються методи клінічної реабілітації, які ґрунтуються на технологіях віртуальної реальності. Використовується програмно-апаратний комплекс для парасимпатичної активації Pure Purr. Технологія віртуальної реальності полягає у поєднанні комп’ютерних технологій, що включають дисплей з оптичною системою, змонтований у шоломі з датчиками відслідковування рухів голови, навушники, а також пристрої керування та навігації, чим досягається ефект ізоляції від зовнішнього середовища та занурення у віртуальне середовище, в якому візуальні та слухові стимули створюють ефект присутності користувача. Останніми роками застосування технології віртуальної реальності поширилося з індустрії розваг на клінічну медицину. За результатами проведеного систематичного огляду досліджень, опублікованих з січня 2012 по липень 2017 року, через бази даних MEDLINE, Journal of Medical Internet Research, PsychINFO, Google Scholar, Science Direct, у який включалися лише дослідження, в яких використовували пристрої віртуальної реальності, монтовані на голові, без обмежень щодо їх апаратних характеристик, знайдено 81 дослідження з використанням загалом 18 моделей пристроїв у 6 сферах психічного здоров’я. Експозиційна терапія або релаксаційні практики, реалізовані у віртуальному середовищі, виявили ефективність, зіставну з ефективністю традиційних модальностей психологічної терапії, при тривожних розладах, посттравматичному розладі, фобіях, розладах харчування, залежностях, депресії, а також для знеболювання і зменшення наслідків психосоціального стресу. Результати ранніх досліджень лікування стресу вказують на те, що віртуальна реальність є ідеальною платформою для поєднання релаксації з психоосвітою [45, 46]. Технологія Pure Purr використовує відеоряд, який не містить ефектів переміщення користувача у віртуальному середовищі або обертальних чи коливальних рухів. Користувач у моделях віртуального середовища Pure Purr займає стаціонарну позицію спостерігача з поглядом, спрямованим перед собою. Доведено, що сеанси перебування у віртуальному природному середовищі знижують рівень стресу, когнітивного виснаження та викликають позитивні емоції в учасників, які щойно перенесли стресову подію [47, 48]. У результаті проведених досліджень встановлено, що після сеансів віртуальної реальності з імітацією занурення в природне середовище, порівняно з активним контролем, статистично значимо знижувалася електропровідність шкіри та покращувалися оцінки за опитувальником особистісного реагування Цукермана, що відображує зниження рівня стресу та переважання позитивних емоцій. Отже, сам факт присутності у віртуальному природному середовищі (що є частиною технології Pure Purr) чинить позитивний відновлювальний ефект безпосередньо після виконання стресового завдання. Результати дослідження вказують на те, що відчуття присутності, яке найбільшою мірою створює технологія віртуальної реальності, має важливе значення для досягнення мети втручання — стану глибокої релаксації та створення умов для відновлення після стресу [49].
Усього за 5 хвилин при застосуванні одного сеансу технології Pure Purr у хворих (за даними сліпого рандомізованого sham-контрольованого дослідження) спостерігалось збільшення парасимпатичної активації більш ніж на 30 % та зниження стрес-індексу на 34 %. У ДУ «Інститут гастроентерології НАМН України» пацієнтів з різними захворюваннями ШКТ обстежують за допомогою новітньої PRECISE-діагностики з метою визначення порушень адаптації та вегетативного гомеостазу з подальшим лікуванням із застосуванням технологій віртуальної реальності. Отримані результати будуть наведені у подальших публікаціях.
Висновки
Варіабельність серцевого ритму являє собою один з найбільш багатообіцяючих кількісних показників вегетативної активності. За допомогою компонентів часового домену аналізу ВСР визначають резерви адаптації та серцево-судинні ризики, а за допомогою частотного домену визначають симпатовагальний баланс ВНС. Порівняно нескладна модифікація методу робить його застосування все більш популярним. Дослідження ВСР має важливе прогностичне й діагностичне значення при обстеженні як практично здорових людей, так і для хворих з найрізноманітнішими патологіями: вегетативними дисфункціями, захворюваннями серцево-судинної, нервової, дихальної, ендокринної систем та захворюваннями ШКТ. Майже всі гастроентерологічні хворі знаходяться в стані порушення адаптації, тому поряд з базисною терапією їм слід призначати індивідуальний план реабілітації для надійної оцінки нейропсихологічного ефекту різних віртуальних технологій і для відновлення вегетативної регуляції у складі комплексної терапії порушень адаптації та стресових розладів.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
/83.jpg)
/85.jpg)
/86_2.jpg)
/87.jpg) Спектрограма будується на основі обвідної кривої КРГ (функції варіації ритму) з використанням перетворень Фур’є (рис. 5).
Спектрограма будується на основі обвідної кривої КРГ (функції варіації ритму) з використанням перетворень Фур’є (рис. 5). 
/86.jpg)
/88.jpg)