Неспецифический язвенный колит (НЯК) — это хроническое воспалительное заболевание кишечника с преимущественной манифестацией в молодом возрасте. Хотя по результатам популяционных когортных исследований у большинства больных НЯК идентифицируют легкое или среднетяжелое течение, приблизительно у 15 % пациентов болезнь имеет тяжелое агрессивное течение, а около 20 % больных требуют стационарного лечения, включая хирургическое. Пациенты со среднетяжелой и тяжелой формой НЯК и агрессивным течением, плохо поддающиеся медикаментозному лечению, уже через 5–10 лет после манифестации болезни имеют высокий риск колэктомии, достигающий 25–30 % [1–3]. Предикторами агрессивного течения и высокого риска колэктомии являются возраст до 40 лет на момент установления диагноза, субтотальное/тотальное поражение, высокая эндоскопическая активность (наличие больших и/или глубоких язв), внекишечные проявления, необходимость в раннем назначении кортикостероидов, высокий уровень воспалительных маркеров.
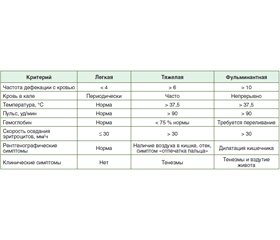
Для определения степени тяжести НЯК традиционно используют критерии Truelove и Witts (табл. 1), а оценка симптомов осуществляется по шкале Мейо (табл. 2). Среднетяжелый и тяжелый НЯК идентифицируют у тех пациентов, которые зависимы от кортикостероидной терапии или рефрактерны к ней (после исключения инфекционного поражения кишечника), имеют серьезные поражения кишечника, которые визуализируются при эндоскопии (наличие язв), а также высокий риск проведения колэктомии. Согласно клиническим и эндоскопическим критериям, 6–12 баллов по шкале Мейо и 2–3 балла по эндоскопическим критериям дают основание идентифицировать у больного среднетяжелую или тяжелую форму НЯК. Согласно шкале Truelove и Witts, тяжелая форма НЯК устанавливается в случае выявления у пациента следующих симптомов: частота дефекации с кровью ≥ 6 при наличии по крайней мере одного критерия системной интоксикации (частота сердечных сокращений > 90 уд/мин, температура тела > 37,8 °C), уровень гемоглобина < 10,5 г/дл и/или скорость оседания эритроцитов > 30 мм/ч [4].
/76.jpg)
Длительная терапия среднетяжелой и тяжелой формы НЯК проводится разными группами препаратов: антагонистами фактора некроза опухоли α (TNF-α), антиинтегриновыми средствами (ведолизумаб), ингибиторами янус-киназ (тофацитиниб), иммуномодуляторами (тиопурины, метотрексат). Большинство препаратов, которые применяются для индукции ремиссии НЯК, могут использоваться для дальнейшего поддержания ремиссии (кроме кортикостероидов и циклоспорина) [3].
В конце позапрошлого года (19 декабря 2018 года) состоялось заседание рабочей группы Американской гастроэнтерологической ассоциации (АГА), на котором был принят проект новых практических рекомендаций по ведению больных со среднетяжелым/тяжелым НЯК, основывающийся на методологии GRADE, в основе которой лежат сила и качество доказательств. Ниже представлены ключевые рекомендации данного документа.
Рекомендации по ведению амбулаторных взрослых пациентов со средне–тяжелой и тяжелой формой НЯК
Рекомендация 1. Для лечения амбулаторных взрослых пациентов со среднетяжелой и тяжелой формой НЯК рекомендовано применение инфликсимаба, адалимумаба, голимумаба, ведолизумаба, тофацитиниба или устекинумаба по сравнению с отсутствием лечения (сильная рекомендация, среднее качество доказательств).
Данная рекомендация основывается на результатах 16 рандомизированных контролируемых исследований (РКИ), в которых сравнивали TNF-α-антагонисты, ведолизумаб и тофацитиниб с плацебо. Индукция ремиссии оценивалась через 6–8 недель терапии, поддержание ремиссии — через 30–54 недели. Во всех исследованиях действующие вещества показали лучшие результаты в сравнении с плацебо — как для индукции ремиссии, так и для ее поддержания. Все препараты хорошо переносились пациентами, отмечена низкая частота появления серьезных нежелательных эффектов, которая не отличалась от группы плацебо.
Рекомендация 2а. С целью индукции ремиссии у амбулаторных взрослых пациентов со среднетяжелой и тяжелой формой НЯК, которые ранее не получали биологическую терапию, AГA предлагает использовать инфликсимаб или ведолизумаб вместо адалимумаба (условная рекомендация, умеренное качество доказательств). Комментарий: пациенты с менее тяжелым течением НЯК, для которых более значимо удобство, связанное с возможностью самостоятельно выполнять подкожные инъекции, и менее значима относительная эффективность лекарственных средств, обоснованно могут выбрать адалимумаб в качестве альтернативы.
Данные рекомендации основываются на данных 15 РКИ (3747 пациентов), в которых оценивалась эффективность разных агентов у пациентов со среднетяжелым и тяжелым НЯК (инфликсимаб — 4 исследования, 667 пациентов; адалимумаб — 4 исследования, 1046 пациентов; голимумаб — 2 исследования, 586 пациентов; ведолизумаб — 3 исследования, 630 пациентов; тофацитиниб — 2 исследования, 520 пациентов и устекинумаб — 1 исследование, 298 пациентов). Данный метаанализ продемонстрировал, что инфликсимаб был более эффективен, чем адалимумаб (умеренная достоверность); при сравнении инфликсимаба и ведолизумаба не было отмечено достоверной разницы. Важно отметить, что в исследованиях дозы препаратов, которые использовались для лечения пациентов, не были оптимизированы. Учитывая одинаковый механизм действия инфликсимаба и адалимумаба, возможно, в случае соблюдения адекватной концентрации лекарственного средства эффективность этих препаратов могла быть сопоставимой [5].
Рекомендация 2b. Для индукции ремиссии у амбулаторных взрослых пациентов со среднетяжелой и тяжелой формой НЯК, которые ранее не получали биологическую терапию, AГA рекомендует применение тофацитиниба только в рамках клинических исследований (рекомендация отсутствует, недостаточность доказательств). Комментарий: обновленные рекомендации FDA (07/26/2019) по показаниям использования тофацитиниба при неспецифическом язвенном колите предлагают его использование только в случае неэффективности или непереносимости антагонистов анти-TNF-α.
На наш взгляд, это связано с тем, что опыт постмаркетингового применения тофацитиниба в качестве первой линии терапии у пациентов со среднетяжелым и тяжелым НЯК, а также долгосрочные сведения о его безопасности ограниченны.
Рекомендация 2с. Для индукции ремиссии у амбулаторных взрослых пациентов со среднетяжелой и тяжелой формой НЯК, которые ранее получали терапию инфликсимабом (особенно в случае отсутствия первичного ответа на лечение), АГA предлагает использовать скорее устекинумаб или тофацитиниб, чем ведолизумаб или адалимумаб (условная рекомендация, низкое качество доказательств). Комментарий: пациенты, особенно с менее тяжелым течением болезни, для которых более значима потенциальная безопасность лекарственных средств и менее значима относительная эффективность лекарственных средств, обоснованно могут выбрать ведолизумаб в качестве альтернативы.
Рекомендация основывается на данных метаанализа 7 РКИ с участием 1580 пациентов, которые ранее получали терапию TNF-α-антагонистами. Имеются данные с невысокой достоверностью, показывающие более высокую эффективность тофацитиниба и устекинумаба по сравнению с адалимумабом (тофацитиниб в сравнении с адалимумабом: ОШ 11,05; 95% ДИ 1,79–68,41; устекинумаб против адалимумаба: OШ 10,71; 95% ДИ 2,01–57,20) и ведолизумабом (тофацитиниб против ведолизумаба: ОШ 6,18; 95% ДИ 1,00–38,00; устекинумаб против ведолизумаба: OШ 5,99; 95% ДИ 1,13–31,76) для индукции клинической ремиссии у пациентов с предшествующим применением TNF-α [5, 6].
Рекомендация 3а. У амбулаторных взрослых пациентов с активным НЯК средней и среднетяжелой степени для индукции ремиссии АГA не рекомендует использовать монотерапию тиопуринами (условная рекомендация, очень низкое качество доказательств).
Рекомендация 3b. У амбулаторных взрослых пациентов со среднетяжелым и тяжелым НЯК, которые находятся в стадии ремиссии, предпочтительнее применять монотерапию тиопуринами для поддержания ремиссии, чем оставлять без лечения (условная рекомендация, низкое качество доказательств).
Этот вывод основывается на результатах 3 клинических исследований, в которых сравнивали тиопурины с плацебо, и двух, в которых сравнивали тиопурины с 5-аминосалициловой кислотой (5-АСК) для индукции бесстероидной ремиссии [7–11]. Несмотря на то что применение тиопуринов ассоциировалось с более высокой частотой достижения бесстероидной ремиссии в сравнении с плацебо или 5-АСК, качество доказательств было очень низким. Ввиду медленного действия тиопуринов их применение в режиме монотерапии у пациентов в стадии обострения НЯК вряд ли позволит достичь бесстероидной ремиссии. Поддержание ремиссии при помощи тиопуринов было оценено в 7 клинических исследованиях (4 исследования — тиопурины в сравнении с плацебо и 3 исследования — тиопурины в сравнении с 5-АСК). Метаанализ данных исследований показал большую эффективность тиопуринов в предупреждении обострения болезни [8, 9, 12–15].
Рекомендация 3с. Применение монотерапии метотрексатом для индукции или поддержания ремиссии у амбулаторных взрослых пациентов со среднетяжелым и тяжелым НЯК не рекомендовано (условная рекомендация, низкое качество доказательств).
В метаанализе 3 исследований, в которых оценивалась эффективность применения метотрексата и 5-АСК или метотрексата и плацебо, не зафиксировано достоверной разницы между частотой индукции ремиссии [16, 17].
Рекомендация 4а. У амбулаторных взрослых пациентов с активной формой среднетяжелого и тяжелого НЯК для индукции ремиссии АГA рекомендует использовать скорее монотерапию средствами биологической терапии (TNF-α-антагонистами, ведолизумабом или устекинумабом) или тофацитинибом, чем монотерапию тиопуринами (условная рекомендация, низкое качество доказательств).
Рекомендация 4b. АГA не предоставляет никаких рекомендаций за или против выбора в пользу биологической терапии (TNF-α-антагонистами, ведолизумабом или устекинумабом) в сравнении с монотерапией тиопуринами для поддержания ремиссии у амбулаторных взрослых пациентов со среднетяжелым и тяжелым НЯК в стадии ремиссии (рекомендация отсутствует, недостаточность доказательств).
В результате клинического испытания UC-SUCCESS было выявлено, что монотерапия инфликсимабом показывает лучшие результаты относительно эндоскопической ремиссии НЯК, чем монотерапия тиопуринами. Согласно предыдущим рекомендациям АГA, для индукции ремиссии предпочтительными являются биологические лекарственные средства (TNF-α-антагонисты, ведолизумаб или устекинумаб), а не тиопурины. Ввиду того факта, что исследование UC-SUCCESS было прекращено преждевременно, сравнительные данные об эффективности биологической терапии и тиопуринов для поддержания ремиссии отсутствуют [18].
Рекомендация 5а. Для лечения амбулаторных взрослых пациентов со среднетяжелым и тяжелым НЯК предпочтительнее применение терапии TNF-α-антагонистами, ведолизумабом или устекинумабом, комбинированной с тиопурином или метотрексатом, а не биологическая монотерапия (условная рекомендация, низкое качество доказательств). Комментарий: пациенты, особенно с менее тяжелым течением болезни, для которых более значим меньший риск побочных реакций при монотерапии препаратами для биологической терапии и менее значима относительная эффективность и безопасность лекарственных средств, менее значима относительная эффективность комбинированной терапии, обоснованно могут выбрать монотерапию препаратами для биологической терапии.
Рекомендация 5b. Для лечения амбулаторных взрослых пациентов со среднетяжелым и тяжелым НЯК предпочтительнее применение терапии TNF-α-антагонистами, ведолизумабом или устекинумабом, комбинированной с тиопурином или метотрексатом, а не монотерапия тиопуринами (условная рекомендация, низкое качество доказательств).
В ходе исследования UC-SUCCESS, в котором сравнивалась эффективность монотерапии инфликсимабом, азатиоприном или их комбинации, была установлена более высокая эффективность комбинированной терапии в индукции бесстероидной ремиссии в сравнении с монотерапией [18]. Исследования, в которых бы сравнивалась эффективность применения комбинации других ТNF-α-антагонистов или ведолизумаба с иммуномодуляторами и биологической монотерапией, не проводились. Но ввиду положительного влияния такой комбинации на фармакокинетику биологического агента эксперты AГA экстраполировали это доказательство в пользу комбинированной терапии.
Рекомендация 6. У амбулаторных взрослых пациентов со среднетяжелым и тяжелым течением НЯК АГА рекомендует скорее раннее назначение биологической терапии с иммуномодуляторами или без них, чем пошаговое усиление терапии в случае неэффективности 5-АСК (условная рекомендация, низкое качество доказательств). Комментарий: пациенты, особенно с менее тяжелым течением болезни, для которых более значима безопасность терапии 5-АСК и менее значима эффективность биологической терапии, обоснованно могут выбрать пошаговое усиление терапии 5-АСК.
Исследований, в которых бы сравнивалась эффективность биологической терапии с иммуномодуляторами или без них и пошаговое усиление 5-АСК терапии, нет. Однако имеются результаты трех клинических исследований, в которых тиопурины продемонстрировали существенно лучшие показатели в достижении бесстероидной ремиссии в сравнении с 5-АСК [9, 12, 15]. С учетом 3-го и 4-го пункта этих рекомендаций биологическая терапия, вероятно, также будет более эффективна в сравнении с 5-АСК-терапией. Считаем важным отметить, что в указанных исследованиях речь идет о пациентах, которые также принимали глюкокортикостероиды. Таким образом, в данной рекомендации речь идет о назначении биологической терапии только после того, как все опции стандартной терапии показали свою неэффективность.
Рекомендация 7. АГA выступает против использования 5-АСК для индукции или поддержания ремиссии у амбулаторных взрослых пациентов со среднетяжелым и тяжелым течением НЯК, у которых на фоне биологической терапии с иммуномодуляторами или без них или терапии тофацитинибом удалось достичь ремиссии (условная рекомендация, очень низкое качество доказательств).
В ходе одного РКИ пациенты с клинической, эндоскопической, гистологической ремиссией на фоне терапии азатиоприном и 5-АСК (олсалазином) были рандомизированы на две группы: больные 1-й группы продолжали прием двух препаратов, больные 2-й принимали только азатиоприн. Через два года наблюдения не было выявлено достоверной разницы в риске возникновения рецидива НЯК между этими двумя группами. Аналогичных исследований с отменой приема 5-АСК на фоне биологической терапии или приема тофацитиниба пока нет. В качестве обоснования этой рекомендации использовались косвенные данные метаанализа нескольких РКИ, не показавшие достоверной разницы в частоте индукции ремиссии у пациентов с НЯК, которые получали TNF-α-антагонисты или тофацитиниб с 5-АСК или без 5-АСК. Следует отметить, однако, что в этих РКИ системно не оценивался отказ от 5-АСК у пациентов, находящихся на биологической терапии или лечении тофацитинибом.
Рекомендации по ведению госпитализированных пациентов с тяжелым НЯК в острой стадии
Рекомендация 8. Госпитализированным взрослым пациентам с тяжелым НЯК в острой стадии рекомендовано внутривенное введение метилпреднизолона преимущественно в дозе 40–60 мг/сут, чем применение более высоких доз (условная рекомендация, очень низкое качество доказательств).
Внутривенное введение кортикостероидов — это основное направление в лечении пациентов с острым тяжелым НЯК. На основании результатов многих РКИ по оценке риска проведения колэктомии у таких больных наиболее оптимальным считается курс гормональной терапии 3–5 дней [19–21].
Рекомендация 9. У госпитализированных взрослых пациентов с тяжелым НЯК в острой стадии, у которых не установлено наличие инфекции, рутинное применение антибиотиков не рекомендовано (условная рекомендация, очень низкое качество доказательств).
Метаанализ 4 РКИ продемонстрировал, что добавление антибиотика в схему лечения пациентов с острым тяжелым НЯК не уменьшает кратковременный риск проведения колэктомии [21–24].
Рекомендация 10. У госпитализированных взрослых пациентов с тяжелым НЯК в острой стадии при отсутствии ответа на внутривенное введение кортикостероидов рекомендовано применение инфликсимаба или циклоспорина (сильная рекомендация, низкое качество доказательств).
В ходе одного РКИ установлено, что у пациентов, резистентных к внутривенному введению кортикостероидов, инфликсимаб превосходил плацебо в снижении риска проведения колэктомии в течение 90 дней после госпитализации [25]. Результаты другого РКИ показали, что циклоспорин также был эффективен у пациентов, не отвечающих на гормональную терапию [26]. Эти данные подтверждены также и в других РКИ [27–29].
Рекомендация 11. АГA не дает рекомендаций по преимущественному рутинному применению увеличенных против стандартных доз инфликсимаба у госпитализированных взрослых пациентов с острым тяжелым течением НЯК, рефрактерного к внутривенному введению кортикостероидов (рекомендация отсутствует, недостаточно доказательств). Данная рекомендация основывается на результатах обсервационных исследований [30–32].
Таким образом, представленные клинические рекомендации по ведению пациентов со среднетяжелым и тяжелым НЯК разработаны на основе анализа современных научных исследований, подтверждающих высокую эффективность препаратов биологической терапии, таких как инфликсимаб, адалимумаб, голимумаб, ведолизумаб, и ингибиторов янус-киназ, таких как тофацитиниб, в качестве препаратов для индукции и поддержания ремиссии среднетяжелого и тяжелого НЯК.
На фармацевтическом рынке Украины нам известны 4 препарата для биологической терапии, которые предлагается использовать настоящими рекомендациями, — 3 антагониста TNF-α (инфликсимаб, адалимумаб, голимумаб) и один антиинтегриновый препарат (ведолизумаб). Ведолизумаб (Энтивио) является иммуносупрессивным биологическим препаратом с селективным воздействием на кишечник. Он представляет собой гуманизированные моноклональные антитела IgG1, которые специфически связываются с α4β7-интегрином и селективно блокируют взаимодействие α4β7-интегрина с молекулами клеточной адгезии слизистой оболочки адрессином 1 (MAdCAM-1), но не с молекулами клеточной адгезии сосудов 1 (VCAM-1). MAdCAM-1 экспрессируется главным образом на клетках эндотелия сосудов кишечника и играет ведущую роль в миграции Т-хелперных лимфоцитов, вызывающих хронический воспалительный процесс, характерный для язвенного колита и болезни Крона. Нарушение данного молекулярного взаимодействия препятствует трансмиграции кишечных Т-лимфоцитов через сосудистый эндотелий в паренхиматозную ткань. В клинических исследованиях пациентам вводили ведолизумаб в дозах от 2 до 10 мг/кг и наблюдали более чем 95% сатурацию рецепторов α4β7 на подтипах циркулирующих лимфоцитов, участвующих в иммунном надзоре в кишечнике. У здоровых добровольцев, пациентов с язвенным колитом или у пациентов с болезнью Крона ведолизумаб не вызывает повышение содержания нейтрофилов, базофилов, эозинофилов, В-клеток и цитотоксических Т-лимфоцитов, общего количества хелперных Т-лимфоцитов памяти, моноцитов или натуральных клеток-киллеров в периферической крови при отсутствии лейкоцитоза.
Противопоказаниями для применения ведолизумаба являются гиперчувствительность к препарату; активная форма тяжелых инфекционных заболеваний, таких как, например, туберкулез, сепсис, цитомегаловирусная инфекция, листериоз и оппортунистические инфекции; прогрессирующая мультифокальная лейкоэнцефалопатия; детский возраст до 18 лет (безопасность и эффективность применения у детей младше 18 лет не установлены). Исследований по применению ведолизумаба у беременных женщин не проводилось. Применение ведолизумаба в период беременности допустимо только в случае, если потенциальная польза явно превосходит предполагаемый риск как для матери, так и для плода.
Профиль безопасности ведолизумаба (Энтивио) изучали в трех плацебо-контролируемых клинических исследованиях с участием пациентов с язвенным колитом (I) или болезнью Крона (II и III). В двух контролируемых исследованиях (I и II) участвовало 1434 пациента, которые получали ведолизумаб в дозах 300 мг в 0 и 2 и 6-ю неделю, а затем каждую 8-ю или каждую 4-ю неделю в период до 52 недель, а также 297 пациентов, которым в течение 52 недель вводили плацебо. Нежелательные явления были отмечены у 84 % пациентов, получавших ведолизумаб, и у 78 % получавших плацебо, то есть разница была статистически недостоверной. Через 52 недели серьезные нежелательные явления наблюдали у 19 % пациентов, получавших ведолизумаб, и 13 % пациентов, получавших плацебо. Аналогичную частоту нежелательных явлений отмечали в каждой из групп, получавших ведолизумаб, с интервалом в 8 и 4 недели в клинических исследованиях III фазы. Доля пациентов, прекративших лечение по причине нежелательных явлений, составляла 9 % в группе, получавшей ведолизумаб, и 10 % в группе, получавшей плацебо. Кроме того, имеющиеся в настоящее время результаты клинических исследований не указывают на наличие повышенного риска злокачественных новообразований в результате лечения ведолизумабом. В объединенных исследованиях нежелательные реакции, которые наблюдали у ≥ 5 % пациентов, включали тошноту, назофарингит, инфекции верхних дыхательных путей, артралгию, пирексию, утомляемость, головную боль и кашель. Инфузионные реакции отмечали у 4 % пациентов, получавших ведолизумаб. Таким образом, профиль безопасности при применении ведолизумаба (Энтивио) в проведенных РКИ был сходен с плацебо.
Согласно данным рекомендациям, для индукции ремиссии НЯК монотерапия тиопуринами малоэффективна, но данный метод лечения можно рассматривать в аспекте поддержания ремиссии болезни. Монотерапия метотрексатом не должна использоваться ни для индукции, ни для поддержания ремиссии НЯК. У пациентов, которые ранее не получали биологическую терапию, в качестве первой линии терапии лучше использовать инфликсимаб и ведолизумаб (Энтивио), а не стандартные дозы адалимумаба. У пациентов, которые уже ранее получали инфликсимаб (особенно при отсутствии ответа на индукционную терапию) применение устекинумаба или тофацитиниба более предпочтительно, чем использование адалимумаба или ведолизумаба. Комбинированная терапия биологическими средствами и иммуномодуляторами более эффективна, чем монотерапия, хотя ввиду вероятности развития ряда побочных эффектов многие пациенты могут выбрать монотерапию биологическими препаратами.
Конфликт интересов. Не заявлен.
Список литературы
1. Fumery M., Singh S., Dulai P.S. et al. Natural History of Adult Ulcerative Colitis in Population-based Cohorts: A Systematic Review. Clin. Gastroenterol. Hepatol. 2018. 16. 343-356 e3.
2. Dassopoulos T., Cohen R.D., Scherl E.J. et al. Ulcerative Colitis Care Pathway. Gastroenterology. 2015. 149. 238-45.
3. Ungaro R., Mehandru S., Allen P.B. et al. Ulcerative colitis. Lancet. 2017. 389. 1756-1770.
4. Truelove S.C., Witts L.J. Cortisone in ulcerative colitis; final report on a therapeutic trial. Br. Med. J. 1955. 2. 1041-8.
5. Feuerstein J.D., Nguyen G.C., Kupfer S.S. et al. American Gastroenterological Association Institute Guideline on Therapeutic Drug Monitoring in Inflammatory Bowel Disease. Gastroenterology. 2017. 153. 827-834.
6. Singh S., George J., Boland B.S. et al. Primary non-response to tumor necrosis factor antagonists is associated with inferior response to second-line biologics in patients with inflammatory bowel diseases: a systematic review and meta-analysis. Journal of Crohn's and Colitis. 2018. 12. 635-643.
7. Caprilli R., Carratu R., Babbini M. Double-blind comparison of the effectiveness of azathioprine and sulfasalazine in idiopathic proctocolitis. Preliminary report. Am. J. Dig. Dis. 1975. 20. 115-20.
8. Jewell D.P., Truelove S.C. Azathioprine in ulcerative colitis: final report on controlled therapeutic trial. British Medical Journal. 1974. 4. 627-30.
9. Mate-Jimenez J., Hermida C., Cantero-Perona J. et al. 6-Mercaptopurine or methotrexate added to prednisone induces and maintains remission in steroid-dependent inflammatory bowel disease. European Journal of Gastroenterology and Hepatology. 2000. 12. 1227-1233.
10. Rosenberg J.L., Wall A.J., Levin B. et al. A controlled trial of azathioprine in the management of chronic ulcerative colitis. Gastroenterology. 1975. 69. 96-9.
11. Sood A., Midha V., Sood N. et al. Role of azathioprine in severe ulcerative colitis: one-year, placebo-controlled, randomized trial. Indian Journal of Gastroenterology. 2000. 19. 14-6.
12. Ardizzone S., Maconi G., Russo A. et al. Randomised controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis. Gut. 2006. 55. 47-53.
13. Hawthorne A.B., Logan R.F., Hawkey C.J. et al. Randomised controlled trial of azathioprine withdrawal in ulcerative colitis. BMJ. 1992. 305. 20-2.
14. Sood A., Kaushal V., Midha V. et al. The beneficial effect of azathioprine on maintenance of remission in severe ulcerative colitis. Journal of gastroenterology. 2002. Vol. 37. 270-274.
15. Sood A., Midha V., Sood N. et al. Azathioprine versus sulfasalazine in maintenance of remission in severe ulcerative colitis. Indian journal of gastroenterology. 2003. Vol. 22. 79-81.
16. Herfarth H., Barnes E.L., Valentine J.F. et al. Methotrexate is not superior to placebo in maintaining steroid-free response or remission in ulcerative colitis. Gastroenterology. 2018.
17. Oren R., Arber N., Odes S. et al. Methotrexate in chronic active ulcerative colitis: a double-blind, randomized, Israeli multicenter trial. Gastroenterology. 1996. 110. 1416-21.
18. Panaccione R., Ghosh S., Middleton S. et al. Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterology. 2014. Vol. 146. 392-400.e3.
19. Turner D., Walsh C.M., Steinhart A.H. et al. Response to Corticosteroids in Severe Ulcerative Colitis: A Systematic Review of the Literature and a Meta-Regression. Clinical Gastroenterology and Hepatology. 2007. 5. 103-110.
20. Seo M., Okada M., Yao T. et al. Evaluation of the clinical course of acute attacks in patients with ulcerative colitis through the use of an activity index. J. Gastroenterol. 2002. 37. 29-34.
21. Chapman R.W., Selby W.S., Jewell D.P. Controlled trial of intravenous metronidazole as an adjunct to corticosteroids in severe ulcerative colitis. Gut. 1986. 27. 1210-2.
22. Dickinson R.J., O'Connor H.J., Pinder I. Double blind controlled trial of oral vancomycin as adjunctive treatment in acute exacerbations of idiopathic colitis. Gut. 1985. 26. 1380-1384.
23. Mantzaris G.J., Hatzis A., Kontogiannis P. et al. Intravenous tobramycin and metronidazole as an adjunct to corticosteroids in acute, severe ulcerative colitis. American Journal of Gastroenterology. 1994. 89. 43-6.
24. Mantzaris G.J., Petraki K., Archavlis E. et al. A prospective randomized controlled trial of intravenous ciprofloxacin as an adjunct to corticosteroids in acute, severe ulcerative colitis. Scandinavian Journal of Gastroenterology. 2001. 36. 971-974.
25. Jarnerot G., Hertervig E., Friis-Liby I. et al. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study. Gastroenterology. 2005. 128. 1805-11.
26. Lichtiger S., Present D.H., Kornbluth A. et al. Cyclosporine in severe ulcerative colitis refractory to steroid therapy. New England Journal of Medicine. 1994. 330. 1841-5.
27. Van Assche G., D'Haens G., Noman M. et al. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis. Gastroenterology. 2003. 125. 1025-1031.
28. Laharie D., Bourreille A., Branche J. et al. Ciclosporin versus infliximab in patients with severe ulcerative colitis refractory to intravenous steroids: a parallel, open-label randomised controlled trial. Lancet. 2012. 380. 1909-15.
29. Williams J.G., Alam M.F., Alrubaiy L. et al. Infliximab versus ciclosporin for steroid-resistant acute severe ulcerative colitis (CONSTRUCT): a mixed methods, open-label, pragmatic randomised trial. The Lancet. Gastroenterology & Hepatology. 2016. 1. 15-24.
30. Choy M.C., Seah D., Gorelik A. et al. Predicting response after infliximab salvage in acute severe ulcerative colitis. J. Gastroenterol. Hepatol. 2018. 33. 1347-1352.
31. Gibson D.J., Heetun Z.S., Redmond C.E. et al. An accelerated infliximab induction regimen reduces the need for early colectomy in patients with acute severe ulcerative colitis. Clin. Gastroenterol. Hepatol. 2015. 13. 330-335 e1.
32. Govani S.M., Stidham R.W., Higgins P.D.R., Hardiman K. Accelerated Dosing of Infliximab Prevents Colectomy Within 90 Days in Only Half of Patients With Severe Ulcerative Colitis. Gastroenterology. 2016. 150. S106.

/76.jpg)