Журнал «Травма» Том 20, №6, 2019
Вернуться к номеру
Разработка и проверка достоверности метода оценки вентральной компрессии позвоночного канала при позвоночно-спинномозговой травме
Авторы: Слынько Е.И., Нехлопочин А.С., Вербов В.В.
Институт нейрохирургии им. акад. А.П. Ромоданова НАМН Украины, г. Киев, Украина
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Актуальність. Механічна компресія вмісту хребетного каналу, що виникає при травматичному пошкодженні хребта, має основоположне значення при визначенні тактики терапії і прогнозів регресу неврологічних розладів у постраждалих. Аналіз даних літератури демонструє відсутність критерію, який дозволяє характеризувати морфологічно гетерогенний субстрат, що викликає компресію спинного мозку. Мета: сформулювати визначення, розробити і виконати перевірку вірогідності рентгенограмметричного методу оцінки сагітального розміру різних за морфологічним типом вентрально-інтраканально розташованих травматичних субстратів. Матеріали та методи. Інформаційний пошук дозволив виявити існуючі індекси і методи вимірювання ступеня компресії хребетного каналу, а також клінічну значимість характеру і ступеня компресії спинного мозку травматичним субстратом. Для первинної перевірки вірогідності методу оцінювання вентрально розташованого травматичного субстрату був проведений ретроспективний аналіз даних нейровізуалізації 150 пацієнтів із травматичними змінами шийного відділу хребта. Були проаналізовані дані спондилограм, комп’ютерних та магнітно-резонансних томограм. Вимірювання проводились трьома незалежними експертами. Результати. Розроблений термін «компримуючий фактор», що становить собою збірне поняття і відображає загальну характеристику патологічних анатомічних субстратів, які виникають при ушкодженнях хребетного рухового сегмента, що призводять до деформації стінок хребетного каналу і, як наслідок, викликають здавлення структур хребетного каналу. Для кількісної характеристики виконувалось вимірювання сагітального розміру компримуючого фактора, що має абсолютну метричну величину і характеризує відносний ступінь зміщення субстрату в просвіт хребетного каналу. Отримані при статистичній обробці результати виявляють високу відтворюваність результатів вимірювань. Коефіцієнт конкордації становив 0,85 при р = 0,00025. Висновки. Наведену радіологічну ознаку доцільно використовувати для загальної характеристики клінічного випадку, а також при статистичній обробці даних із метою уніфікації уявлення про ступінь компресії вмісту хребетного каналу.
Актуальность. Механическая компрессия содержимого позвоночного канала, возникающая при травматическом повреждении позвоночника, имеет основополагающее значение при определении тактики терапии и прогнозов регресса неврологических расстройств у пострадавших. Анализ данных литературы демонстрирует отсутствие критерия, позволяющего характеризовать морфологически гетерогенный субстрат, вызывающий компрессию спинного мозга. Цель: сформулировать определение, разработать и выполнить проверку достоверности рентгенограмметрического метода оценки сагиттального размера различных по морфологическому типу вентрально-интраканально расположенных травматических субстратов. Материалы и методы. Информационный поиск позволил выявить существующие индексы и методы измерения степени компрессии позвоночного канала, а также клиническую значимость характера и степени компрессии спинного мозга травматическим субстратом. Для первичной проверки достоверности метода оценки вентрально расположенного травматического субстрата был проведен ретроспективный анализ данных нейровизуализаци 150 пациентов с травматическими изменениями шейного отдела позвоночника. Были пронализированы данные спондилограмм, компьютерных и магнитно-резонансных томограмм. Измерения проводились тремя независимыми экспертами. Результаты. Разработан термин «компримирующий фактор», который подразумевает собирательное понятие и отражает общую характеристику патологических анатомических субстратов, возникающих при повреждениях позвоночного двигательного сегмента, которые приводят к деформации стенок позвоночного канала и, как следствие, вызывают сдавление структур позвоночного канала. Для количественной характеристики выполнялось измерение сагиттального размера компримирующего фактора, имеющего абсолютную метрическую величину и характеризующего относительную степень смещения субстрата в просвет позвоночного канала. Полученные при статистической обработке данные показывают высокую воспроизводимость результатов измерений. Коэффициент конкордации составил 0,85 при р = 0,00025. Выводы. Представленный радиологический признак целесообразно использовать для общей характеристики клинического случая, а также при статистической обработке данных с целью унификации представления о степени компрессии содержимого позвоночного канала.
Background. Mechanical compression of spinal canal that occurs in spinal cord injury is the fundamental criteria in determining treatment approaches and prognosis of neurological disorders regression in the victims. Analysis of the literature data demonstrates the absence of a criterion that allows us to characterize a morphologically heterogeneous substrate that causes spinal cord compression. The purpose was to formulate definition, to develop and perform validation of radiologic criteria for assessing the sagittal size of the morphologically heterogenic, ventrally located intraspinal traumatic substrates. Materials and methods. Literature analysis revealed the existing indices and methods for measuring the value of spinal cord compression, as well as the clinical significance of the nature and degree of the spinal cord compression with a traumatic substrate. For the initial verification of the reliability of the method for assessing a ventrally located traumatic substrate, a retrospective analysis of neuroimaging data of 150 patients with traumatic changes in the cervical spine was performed. The data of X-ray films, computed tomography and magnetic resonance imaging were analyzed. The measurements were carried out by three independent experts. Results. The definition of compressing factor has been developed that implies a collective term and reflects the general characteristics of pathological anatomical substrates caused by a damage to the spinal motion segment, leading to the deformation of the walls of the spinal canal and, as a result, causing spinal cord compression. For quantitative characteristics, the sagittal size of the compressing factor was measured, having an absolute metric value and determining the relative degree of substrate displacement into the spinal canal. The results obtained by statistical processing reveal high reproducibility of the measurements. The concordance coefficient was 0.85 at p = 0.00025. Conclusions. The presented radiographic criteria should be used for the general characteristics of the clinical case, as well as for statistical data processing in order to unify the idea of the degree of spinal cord compression.
травма хребта; хребетний канал; компримуючий фактор; сагітальний розмір; нейровізуалізація
травма позвоночника; позвоночный канал; компримирующий фактор; сагиттальный размер; нейровизуализация
spinal injury; spinal canal; compression factor; sagittal size; neuroimaging
Введение
На этапе определения тактики лечения пострадавших с позвоночно-спинномозговой травмой необходимым является проведение целого комплекса диагностических мероприятий, позволяющих судить о характере повреждения позвоночника и степени компрессии содержимого позвоночного канала: спинного мозга, его корешков и оболочек [1, 2]. Предпочтение хирургическим методам лечения, как правило, отдается в случаях, когда у пострадавшего отмечаются компрессия невральных образований, нестабильные формы повреждений либо выраженная деформация позвоночника [3, 4].
При поступлении в лечебное учреждение одним из первоочередных, наиболее распространенных, доступных и часто выполняемых диагностических мероприятий является рентгенологическое обследование [5]. Анализу подлежат качественные спондилограммы с четким изображением тел и дуг позвонков обследуемого отдела позвоночника. При этом, по данным различных авторов, разрешающая способность рентгенографии при диагностике повреждений позвоночника колеблется в пределах 36–57 % [6, 7]. В некоторых случаях, особенно при травмах нижних шейных сегментов, рентгенография не позволяет получить исчерпывающую информацию о степени и характере повреждения, что препятствует выбору оптимальной тактики лечения [8]. Поэтому при патологии позвоночника к обязательным методам диагностики относят спиральную компьютерную томографию (СКТ) заинтересованного позвоночно-двигательного сегмента (ПДС), что в 83–98 % случаев позволяет установить правильный диагноз [9]. В сравнении с рентгенографией СКТ дает возможность на 25 % точнее диагностировать взрывные переломы тел позвонков [10]. Для объективизации состояния мягкотканных структур позвоночника наиболее эффективным и информативным нейровизуализирующим обследованием представляется магнитно-резонансная томография (МРТ). С ее помощью можно анализировать состояние мягких тканей позвоночного канала, спинного мозга, его оболочек, резервных пространств и спинномозговых корешков [11]. Метод эффективен при диагностике травматических экструзий дисков, экстра- и интрадуральных кровоизлияниях, ишемии и отеке спинного мозга, гематомиелии, а также в случае наличия радикулярной или миелорадикулярной симптоматики, несмотря на отсутствие костной патологии [12].
С целью измерения метрических и угловых показателей позвоночника, выявления патологических процессов, определения динамики развития нарушений ориентации структур позвоночных двигательных сегментов и оценки результатов лечения широко используются методы рентгенограмметрии [13–16].
Анализ данных литературы демонстрирует, что в настоящее время нет описания параметра, позволяющего характеризовать любую интраканальную структуру, вызывающую компрессию спинного мозга, — смещенные тела позвонков, фрагменты поврежденных тел и дуг позвонков, травматические грыжи межпозвонковых дисков, поврежденная задняя продольная связка, эпи- и субдуральные гематомы травматического генеза и т.д.
Цель исследования: сформулировать определение, разработать и выполнить проверку достоверности рентгенограмметрического метода оценки сагиттального размера различных по морфологическому типу вентрально-интраканально расположенных травматических субстратов.
Материалы и методы
Разработка метода
Информационный поиск выполнен с использованием базы MedLine по ключевым словам «spinal canal compression evaluation», «spinal canal compression diagnosis», «spinal canal compression index», «spinal cord compression evaluation», «spinal cord compression diagnosis», «spinal cord compression index». Использованы также базы Национальной библиотеки Украины имени В.И. Вернадского и Украинского института интеллектуальной собственности. Выявлены существующие индексы и методы измерения степени компрессии позвоночного канала, а также клиническая значимость характера и степени компрессии спинного мозга травматическим субстратом.
Проверка достоверности
Для первичной проверки достоверности метода оценки вентрально расположенного травматического субстрата был избран шейный отдел позвоночника. Проведен ретроспективный анализ данных нейровизуализаци 150 пациентов с травматическими изменениями шейного отдела позвоночника, находившихся на лечении в Институте нейрохирургии им. акад. А.П. Ромоданова НАМН Украины в период с 2010 по 2018 г. Анализировались данные спондилограмм, компьютерных и магнитно-резонансных томограмм, хранящиеся в архиве в формате DICOM. Обработка изображений выполнялась с применением программного продукта RadiAnt DICOM Viewer 4.2.1 demo version, позволяющего выполнять измерения с точностью до 0,1 мм. Расчеты выполнялись 3 независимыми специалистами. Оценка согласованности мнений экспертов производилась с использованием коэффициента конкордации рангов Кендалла (W). При этом считалось, что в случае, когда значение коэффициента конкордации превышает 0,40–0,50, качество оценки является удовлетворительным, если же W > 0,70–0,80 — высоким. Проверка значимости коэффициента основывалась на том, что если нулевая гипотеза об отсутствии корреляционной связи при n > 7 справедлива, то m(n–1)W имеет приближенное χ2-распределение с n–1 степенями свободы, где n — количество анализированных случаев, а m — количество экспертов.
Результаты и обсуждение
Анализ литературных данных позволил выявить достаточное количество рентгенограмметрических, СКТ- и МРТ-морфометрических референций, характеризующих топографоанатомические взаимоотношения костных и мягкотканных структур позвоночного канала на уровне как нормального с анатомической точки зрения, так и поврежденного позвоночного двигательного сегмента. Наиболее широко распространенные приведены ниже.
— Индекс Павлова — Торга — сопоставление сагиттального диаметра позвоночного канала и тела позвонка, за норму принимается показатель, равный 1,0 [17].
— Степень деформации — отношение разницы между сагиттальным размером позвоночного канала на уровне вышерасположенного позвонка и критическим расстоянием и сагиттальным размером позвоночного канала на уровне вышерасположенного позвонка, –умноженное на 100 (в %) [18].
— Среднесагиттальный размер позвоночного канала (метод Hinch) — наименьшее расстояние между задней поверхностью тела позвонка и внутренней поверхностью дуги у основания остистого отростка на уровне вышерасположенного от поврежденного позвонка [5, 14].
— Критическое расстояние (в см) — наименьший сагиттальный размер позвоночного канала на уровне поврежденного позвонка [5, 14].
— Сужения позвоночного канала от исходного уровня — определяются по формуле: A = (1 – x/y) ´ 100, где А — процент сужения, х — наименьший размер позвоночного канала на уровне повреждения, у — средняя величина среднесагиттального размера у данного пациента [19].
— Степень переднезадней компрессии спинного мозга — на МР-томограммах измеряется соотношение самого малого диаметра к самому большому диаметру спинного мозга [9, 11, 20].
При детальном анализе существующих рентгенограмметрических признаков обращает на себя внимание тот факт, что большинство описанных в литературе показателей является инструментом для оценки следствий травматических повреждений костных элементов позвонков и диско-связочного аппарата, а именно вторичный стеноз ПК, изменение площади ПК или степень сдавления СМ. Все приведенные характеристики косвенно интерпретируют причину компрессии спинного мозга, особенно при отсутствии интраканальных костных фрагментов.
В то же время мало исследований посвящено проблеме определения истинных размеров смещенных в результате повреждений элементов стенок ПК, вызывающих компрессию спинного мозга и его образований. Среди коэффициентов, позволяющих реализовать эту задачу, можно выделить измерение таких показателей, как величина сдвигового смещения и размер клина Урбана.
— Сдвиговое смещение — расстояние между линиями, проведенными вдоль задних замыкательных пластин смещенного и подлежащего позвонков. Измерение выполняется на уровне корня дуги подлежащего позвонка. Показатель используется для определения величины дислокации при подвывихах, вывихах и переломовывихах позвонков [21, 22].
— Клин Урбана — клиновидный отломок тела позвонка, смещающийся в сторону позвоночного канала. Возникает при компрессионном оскольчатом переломе позвоночника и его расплющивании. Может вызывать сдавление СМ. Описал врач J. Urban. Показатель используется для установления краниокаудального и вентродорсального сагиттальных размеров фрагментов тел поврежденных позвонков [7].
Безусловно, указанные диагностические методы довольно эффективны и позволяют получить достаточно полную информацию о деформации вентральной стенки позвоночного канала. Однако при этом имеются в виду смещения только костных элементов, в то время как сдавливание спинного мозга могут вызывать и иные патологические фрагменты.
Как показывает практика, сагиттальный размер смещенных элементов стенок ПК играет существенную роль при выборе метода лечения. Иногда они лишь незначительно пролабируют в позвоночный канал и не сдавливают спинной мозг. В этом случае при отсутствии других показаний большинство авторов рекомендуют воздержаться от хирургического вмешательства и назначить консервативное лечение, которое менее травматично для больного и исключает вероятность возникновения послеоперационных осложнений. И лишь в тех ситуациях, когда величина смещения имеет значительные размеры, эффективное лечение может быть достигнуто только хирургическим путем [2]. Используя только понятия «сдвиговое смещение» или «клин Урбана», не представляется возможным достоверно оценить все возможные варианты структурных изменений заинтересованного ПДС, тем более если речь идет не о костном фрагменте клиновидной формы или не о выстоящем крае смещенного позвонка. Данное обстоятельство может создавать определенные сложности при принятии правильного решения в отношении выбора оптимального варианта лечения больного.
В процессе генерирования определения показателя нами анализировалась рентгенологическая, СКТ- или МРТ-картина топографоанатомических взаимоотношений структур позвоночного канала заинтересованного ПДС. Полученная информация представляется нам той доказательной информационной базой, которая делает возможным исключение субъективизма при оценке состояния поврежденного ПДС и является одним из позитивных моментов в решении вопроса о выборе оптимальной тактики ведения больного с вертеброгенными миелокомпрессионными синдромами.
На этапе планирования операции важными являются сведения о параметрах фрагментов стенок позвоночного канала травмированного ПДС, оказывающих компрессионное воздействие на спинной мозг. Значимость этого показателя сложно переоценить, поскольку он является одним из базовых критериев, определяющих показания для выполнения декомпрессивно-реконструктивно-стабилизирующих, реконструктивно-стабилизирующих или стабилизирующих вмешательств.
В процессе формирования представления о показателе предусматривалось, что разрабатываемый термин не может иметь фиксированную величину в связи с отличными по характеру, механизму возникновения, степени выраженности, уровню повреждения индивидуальными особенностями позвоночника пациента. Тем не менее рекомендуемый индекс снижает целесообразность перечисления достаточного количества патологических ситуаций при статистической обработке данных, необходимых для общей характеристики результатов обследования, определенного объема клинических наблюдений.
Различные по характеру сужения ПК, вызванные смещением в его просвет костных отломков тел позвонков или фрагментов дискосвязочного аппарата, приводят к сдавлению спинного мозга. При этом не имеет принципиального значения, чем именно будет обусловлено компрессионное воздействие на невральные структуры. Актуален сам факт компрессии, то есть компримирующий фактор (КФ), являющийся частью поврежденной вентральной стенки позвоночного канала. В качестве примера приводим результаты нейровизуализирующих методов обследования при некоторых повреждениях шейного отдела позвоночника (рис. 1, 2).
Все приведенные клинические ситуации имеют один общий характерный признак — наличие травматического субстрата, выстоящего в просвет позвоночного канала и оказывающего компрессионное влияние на содержимое дурального мешка. При этом механизм воздействия на невральные структуры и результаты сдавления не зависит от морфологической структуры смещенных в результате повреждения позвоночника тканей.
Такая патология вызывает возникновение различных по степени выраженности и распространенности нарушений архитектоники СМ, обусловленных его повреждением в момент травмы, острой или хронической компрессией, нарушениями микроциркуляции спинномозговой жидкости или вторичными сосудистыми поражениями. В любом случае это инспирирует запуск серии реакций, приводящих к вторичной гибели изначально неповрежденных нейронов и глии [23]. При этом неврологические расстройства могут проявляться как в остром, так и в отдаленном периоде после перенесенной травмы позвоночника.
Термин «компримирующий фактор» подразумевает собирательное понятие и отражает общую характеристику патологических анатомических субстратов, возникающих при повреждениях позвоночного двигательного сегмента (сегментов), приводящих к деформации стенок позвоночного канала и, как следствие, вызывающих сдавление структур позвоночного канала. КФ не предусматривает детальное освещение патоморфологической характеристики каждой из нозологических форм, имеющих место в определенной клинической ситуации.
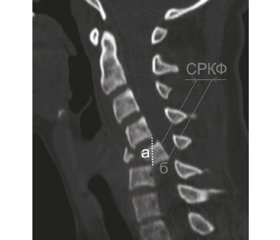
Для количественной характеристики КФ выполнялось измерение сагиттального размера компримирующего фактора (СРКФ), имеющего абсолютную метрическую величину и характеризующего относительную степень смещения КФ в просвет позвоночного канала.
Величина СРКФ — это длина перпендикуляра (б), опущенного от наиболее выступающего кзади участка деформированной вентральной стенки позвоночного канала заинтересованного ПДС (задневерхний или задненижний край смещенного тела позвонка, фрагмент тела позвонка, фрагмент дискосвязочного аппарата и т.д.) к линии (а), соединяющей задненижний край вышележащего по отношению к травмированному позвонка с зад-неверхним краем подлежащего позвонка (рис. 3) (Патент Украины на изобретение № 113119) [24].
Следует отметить, что при описании результатов СК- либо МР-томограмм ряд рентгенологов как используют термин СК, так и выполняют измерение СРКФ, не опираясь при этом на какую-либо унифицированную методику, что обусловливает определенные трудности в оценке результатов проведенного лечения. Оригинальность предложенного метода подтверждена проведенным анализом данных литературы и выполненным патентным поиском.
Для наглядности и упрощения анализа результатов проведенных исследований в статье приводятся материалы, полученные при обследовании больных с травмами шейного отдела позвоночника. Это обстоятельство обусловлено тем, что при правильном проведении рентгенологического обследования больных с позвоночно-спинномозговой травмой на этом уровне, за исключением нижних шейных сегментов, в связи с отсутствием проекционных наложений врач имеет возможность получить больше информации, чем при обследовании пострадавших с повреждениями других отделов позвоночника. Результаты рентгенографии в сочетании с неврологической симптоматикой имеют решающее значение, упрощают и позволяют дифференцированно подходить к выбору показаний для проведения таких высокотехнологичных методов обследования, как СКТ и МРТ. В процессе реализации поставленной задачи нами использовались оба указанных диагностических метода.
В результате анализа данных нейровизуализации 150 пациентов для анализа отобрано 208 исследований надлежащего качества, включающих 34 цервикальные спондилограммы, 65 СК-томограмм и 109 МР-томограмм. Патологический субстрат КФ был представлен следующими образованиями:
— неповрежденный участок тела позвонка, вызывающий компрессию в результате кифотической деформации;
— неповрежденный участок тела позвонка, вызывающий компрессию в результате смещения деформации;
— отломки тела позвонка;
— травматические экструзии межпозвоночных дисков;
— эпи- и субдуральные гематомы.
Указанные элементы встречались изолированно либо в комбинации. С учетом различных диагностических возможностей указанные элементы выявлялись с помощью различных методов (табл. 1).
Следует отметить, что целью настоящей работы не являлось определение диагностической ценности результатов различных методов диагностики при оценке КФ. Определены только общие диагностические возможности. Так, например, очевидно, что отломки тел позвонков, пролабирующие в позвоночный канал, гораздо лучше визуализируются на СК-томограммах, чем на спондилограммах. Сравнение СРКФ, полученных у одного пациента при использовании различных методов диагностики, не проводилось.
При обработке данных нейровизуализации выявлены определенные закономерности, определяющие морфологический субстрат КФ при различных типах повреждений (табл. 2).
Обращает на себя внимание то, что 54 % случаев КФ представлены морфологически полиморфным субстратом. При этом в литературе данному факту уделяется недостаточно внимания; как правило, оцениваются размеры либо костных фрагментов, либо травматической экструзии межпозвоночного диска.
Анализ данных статистической обработки по оценке согласованности мнений экспертов выявил следующие закономерности (табл. 3).
Полученные результаты выявляют высокую воспроизводимость результатов измерений. Закономерно, что наиболее близкие значения размеров КФ получены в тех случаях, когда в роли КФ выступает костная ткань, что в значительной степени облегчает определение границ компримирующего фрагмента. Наименьшие значения коэффициента конкордации зарегистрированы в тех ситуациях, когда компримирующий фактор образован разнородными морфологическими элементами (костная ткань + ткань диска, костная ткань + гематома и др.). Во всех случаях значимость коэффициента — p < 0,05, что свидетельствует о высокой статистической достоверности полученных результатов.
Подводя итог приведенным результатам, можно сделать следующие выводы:
— определение сагиттального размера КФ не имеет значительных технических трудностей и характеризуется высокой воспроизводимостью результатов;
— предложенное определение компримирующего фактора в настоящее время является единственной характеристикой морфологически полиморфного субстрата, оказывающего компримирующий эффект на структуры позвоночного канала;
— предложенный метод измерения КФ в отличие от существующих позволяет оценивать компримирующий эффект задних отделов тела позвонка на структуры позвоночного канала при кифотической деформации;
— метод не имеет строгой привязки к определенному способу нейровизуализации, что делает его достаточно универсальным для широкого спектра диагностических исследований.
Все вышеперечисленное позволяет рекомендовать предложенный способ измерения КФ к широкому применению в клинической практике. Дальнейшие исследования необходимы для повышения диагностической ценности описанного метода.
Выводы
Представленный рентгенометрический признак целесообразно использовать для общей характеристики клинического случая, а также при статистической обработке данных, например рентгенометрических показателей, полученных при изучении эффективности тех или иных методов лечения у определенной группы больных, либо для освещения общей характеристики КФ, вызвавшего деформацию передней стенки позвоночного канала в конкретной клинической ситуации.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов в отношении любых препаратов, материалов, устройств, методов, использованных в этом исследовании, или результатов, указанных в этой статье.

/30-1.jpg)
/30-2.jpg)
/31-1.jpg)
/32-1.jpg)
/32-2.jpg)
/32-3.jpg)