Вступ
Сьогодні розвиток медичної науки в цілому і зокрема травматології та ортопедії характеризується інтеграцією, технічними інноваціями з метою підвищення точності, ефективності лікувально-діагностичного процесу, а також оптимізації роботи системи охорони здоров’я [3]. Одним із досягнень сучасної науки в галузі програмного забезпечення є автоматизовані комп’ютерні системи, що досить успішно впроваджуються в аерокосмічній галузі та багатьох інших видах надточного виробництва. Система автоматизованого проектування у наш час активно застосовується в різних сферах економічної діяльності [1, 2].
3D-друк в охороні здоров’я — поки відносно невеликий ринок: у 2014 році його обсяг становив, за оцінкою компанії Visiongain, $825 млн. Але до 2019 року він зросте майже вчетверо — до $2,9 млрд [7]. Інша аналітична компанія, Industy ARC, вважає, що в 2014-му обсяг ринку дорівнював $487 млн, і ця цифра була рекордною, а до 2020-го вона буде збільшуватися на 18,3 % щорічно з одночасним зниженням ціни технології і матеріалів. Найактивніше розвиватимуться технології 3D-друку для виготовлення ортопедичних, черепних і щелепно-лицьових імплантів, як очікують аналітики Visiongain [7].
Натепер адитивні (3D) технології активно впроваджуються у повсякденну медичну практику. 3D-моделювання та прототипування застосовуються в різних галузях хірургії при плануванні та виконанні оперативних втручань. В ортопедії ця технологія з’явилася в 1990 році, коли при ендопротезуванні колінного суглоба був використаний виготовлений методом 3D-друку індивідуальний шаблон з орієнтирами для проведення гвинтів [5, 10, 11]. Відтоді у зарубіжній літературі все частіше згадується про застосування індивідуальних шаблонів для навігації при хірургічних втручаннях на різних кістках скелета. У наш час в ортопедії та травматології перспективними є такі напрямки адитивних технологій [4]:
— 3D-моделювання з виготовленням пластикового прототипу;
— індивідуальне ортезування та протезування на основі 3D-сканування частин тіла;
— виготовлення індивідуальних металофіксаторів і кастомних ендопротезів (3D-друк титаном);
— біопринтинг — вирощування тканин та органів із застосуванням стовбурових клітин.
Отже, розробка нових і впровадження відомих методик 3D-моделювання та прототипування в комплексі діагностичних заходів при травматологічній та ортопедичній патології — перспективний напрямок, що є цікавим як з наукової, так і з практичної точки зору. В лабораторії 3D-друку ДУ «Інститут травматології та ортопедії НАМН України» широко використовують технологію виготовлення пластикових прототипів при різній ортопедичній і травматологічній патології. Викликав інтерес аналіз досвіду роботи даної лабораторії з визначенням діагностичної цінності використання адитивних технологій у доопераційній підготовці хворих ортопедично-травматологічного профілю.
Мета роботи — визначити діагностичну цінність використання адитивних технологій при доопераційній підготовці хворих із ортопедо-травматологічною патологією.
Матеріали та методи
Протягом 2018 року в лабораторії медичного 3D-друку ДУ «Інститут травматології та ортопедії НАМН України» виконано 3D-моделювання та виготовлення пластикових прототипів у 45 пацієнтів. Спектр ортопедо-травматологічної патології, де були застосовані адитивні технології, поданий на рис. 1. Найчастіше 3D-моделювання використовували у випадках складного ревізійного ендопротезування кульшового суглоба (57,8 %). 3D-моделювання знайшло своє місце в комплексній доопераційній підготовці хворих при складному ендопротезуванні колінного суглоба (13,3 %), складних переломах таза та довгих кісток (11,1 %), диспластичному коксартрозі, онкологічних захворюваннях кісток — по 6,7 %, гетеротопічній осифікації кульшового суглоба — 4,4 %.
Усім категоріям хворих у доопераційному періоді було виконано стандартні рентгенограми та комп’ютерну томографію уражених сегментів з метою побудови тривимірної моделі та пластикового прототипу ураженого сегмента.
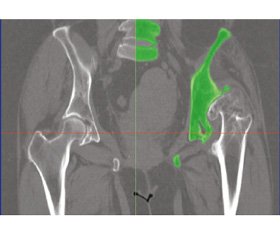
Першим етапом створення фізичної 3D-моделі є обробка двовимірних зображень КТ- та МРТ-сканування (рис. 2). Аналіз, очищення артефактів відбувається на кожному зрізі та в трьох площинах конкретного дослідження, отриманого за допомогою променевої діагностики, що зумовлює додатковий аналіз кожного зрізу спеціалістом ортопедом-травматологом та високу точність у побудові тривимірного зображення. Для забезпечення високої точності кінцевого прототипу необхідно мати якісні вхідні дані КТ- та МРТ-зображень.
Для обробки двовимірних зображень використовується спеціалізоване програмне забезпечення. Найбільш поширеним форматом введення даних для цих програм є DICOM, але також підтримуються інші формати зображень, такі як TIFF, JPEG, BMP і RAW. Оброблене зображення зберігається в будь-якому з форматів вихідних файлів залежно від подальшого застосування: STL, VRML, PLY і DXF. Основний формат файлів для тривимірного друку (далі 3D-друк) — STL (рис. 3).
Другим етапом є експорт збереженого файлу в форматі STL у програму Autodesk NetFabb (рис. 4), в якій проводиться автоматичне й ручне виправлення та редагування 3D-моделі. Поверхня об’єктів у цьому форматі являє собою сукупність полігонів (Polygon mesh). Інтелектуальні скрипти можуть автоматично аналізувати поверхні, виправляти помилки сіток, покращувати точність моделей шляхом повторної тріангуляції, усувати просторові колізії та інші помилки. Програма дає можливість спрогнозувати можливі спотворення, що виникають у виробі під час 3D-друку, безпосередньо до запуску у виробництво. На підставі цього інженер може скорегувати вихідний дизайн таким чином, щоб уникнути помилок під час 3D-друку.
/90-2.jpg)
Третім етапом є переведення готової 3D-моделі у програму «слайсер», яка безпосередньо підходить до самого 3D-принтера, в нашому випадку Flash Print. Flash Print — це програма для перетворення тривимірної моделі в зрозумілий принтеру набір команд, званий g-code. На цьому етапі встановлюються кінцеві дані для 3D-друку, а саме: задають положення деталі під час друку, розраховується тип та кількість підтримок, задають щільність заповнення моделі, обирають оптимальну швидкість та температуру для друку.
Принтер друкує пластиковий прототип кістки в натуральну величину. Процес триває від кількох годин до однієї доби. Даний вид пластику легко обробляється фрезами та іншими хірургічними інструментами, що дає змогу примірити вибрану імплантаційну систему.
Друк прототипу виконувався на 3D-принтері Flash Forge Guider II з ABS-пластику (рис. 5).
У 3 хворих (онкологічні захворювання кісток), за вимогою оперуючих хірургів, виконано друк ураженого сегмента кістки разом із судинами, після їх попереднього контрастування при виконанні КТ.
З метою визначення ефективності виконання оперативних втручань хворі з нестабільністю компонентів ендопротезу кульшового суглоба, диспластичними коксартрозами, гетеротопічною осифікацією кульшового суглоба, яким у доопераційному періоді виконувалось 3D-моделювання та друк пластикового прототипу, були обстежені в доопераційному та ранньому післяопераційному періоді клінічно за класифікацією W.H. Harris [6]. У всіх пацієнтів цієї категорії відзначали негативний результат цієї оцінки (діапазон 46–56 балів) у доопераційному періоді. Ознаками ефективності хірургічного лікування у хворих із складними переломами таза та довгих кісток були наявність консолідації переломів, відновлення опороздатності та функції уражених кінцівок. У хворих, яким виконувалось складне ендопротезування колінного суглоба, для оцінки ефективності використовували альгофункційний індекс стану колінного суглоба за M.G. Lequesne [8]. У всіх пацієнтів цієї групи відмічали негативний результат цієї оцінки (діапазон 8–11 балів) у доопераційному періоді. У хворих із онкологічними захворюваннями кісток критеріями ефективності оперативного лікування вважали відсутність інтраопераційних (порушення іннервації й ушкодження судин) і ранніх післяопераційних ускладнень, відновлення опороздатності та функції уражених кінцівок.
Результати та обговорення
Найчастіше пластикові моделі застосовувались у процесі передопераційної підготовки до складного та ревізійного ендопротезування кульшового суглоба (рис. 6). Ця технологія дає можливість оцінити розміри дефектів, точно підібрати ревізійну систему, визначити доцільність використання аугментів або кісткової пластики.
Пластик моделі можна обробляти фрезами. У разі необхідності його можна простерилізувати та взяти в операційну. На рис. 7 подано рентгенографію хворої до оперативного втручання (А), підготовку макета кульшової западини при диспластичному коксартрозі (Б) та результат ендопротезування кульшового суглоба (В).
Використання з метою визначення характеристик (локалізація, величина) дефектів кульшової западини чи проксимального відділу стегнової кістки та можливість примірки імплантаційної системи в передопераційному періоді хворих із нестабільністю компонентів ендопротезу кульшового суглоба, диспластичними коксартрозами, гетеротопічною осифікацією кульшового суглоба пластикового прототипу дозволило зменшити час оперативного втручання, інтраопераційну крововтрату та добитися добрих функціональних результатів. У післяопераційному періоді показники бальної оцінки за W.H. Harris [6] у 20 пацієнтів відмінні, в 11 — добрі. Строк спостереження становив 1 рік.
Приклад складного ендопротезування колінного суглоба подано на рис. 8. У доопераційному періоді визначено рівень потрібної резекції тібіального плато та необхідність застосування аугменту медіального виростка великогомілкової кістки.
Проведення в доопераційному періоді ретельного обстеження суглоба з використанням адитивних технологій у хворих, які готувалися до складного ендопротезування колінного суглоба, дозволило досягти добрих функціональних результатів у ранньому післяопераційному періоді. Показники альгофункціонального індексу за M.G. Lequesne [8] у цієї категорії хворих були в діапазоні 2–3 балів. Строк спостереження — 1 рік.
Ще одним важливим сегментом застосування 3D-моделювання та прототипування є його використання при складних внутрішньосуглобових переломах кісток (рис. 9, 10). Пластиковий прототип дозволяє максимально точно оцінити характер перелому та спланувати оперативне втручання. Пластик добре обробляється інструментами. Ми можемо ідеально підібрати фіксатори, вигнути їх, ніби виконати операцію до операції. Це значно скорочує час оперативного втручання та зменшує кількість можливих ускладнень. Прикладом цього може бути рис. 9: у хворого із застарілим переломом бокової маси крижової кістки, переломом лонної та сідничної кісток (А) ми виготовили з термопластика та застосували в операційній індивідуальну навігаційну систему для остеосинтезу крижової кістки гвинтами (Б). Із звичайним інтраопераційним ЕОПом досягти коректного введення гвинтів в умовах спотвореної анатомії було б досить складним завданням.
/93-2.jpg)
/94-1.jpg)
Використання сучасних адитивних технологій дозволило в 100 % (3 випадки — переломи кісток таза та 2 випадки — внутрішньосуглобові переломи довгих кісток) досягти консолідації переломів із відновленням опороздатності та функції ураженого сегмента.
Існує можливість друкувати кістки разом із судинами, після їх попереднього контрастування при виконанні КТ.
В онкології 3D-друк дозволяє визначити рівень резекції пухлини та оцінити можливість ушкодження судин під час операції. На рис. 11 подано прототип плечової кістки, ураженої метастазом раку нирки. На прохання хірургів візуалізовано плечову артерію.
Використання адитивних технологій з методикою друку судин після їх попереднього контрастування у хворих з онкологічними захворюваннями кісток (3 випадки) дозволило запобігти судинним і неврологічним ускладненням під час оперативного втручання, відновити опороздатність та функцію ураженої кінцівки всіх прооперованих хворих. Строк спостереження — 6 місяців.
Отже, наше дослідження доводить високу діагностичну цінність 3D-моделювання та прототипування в доопераційній підготовці хворих із різною ортопедо-травматологічної патологією. Використання адитивних технологій дозволило досягти добрих і відмінних функціональних результатів у всіх 45 обстежених хворих у ранньому післяопераційному періоді, що доводить його високу ефективність та може бути рекомендовано як незамінний метод при підготовці до складних реконструктивних ортопедо-травматологічних втручань.
Щодо перспектив відносно розширення спектра ортопедичної патології, де застосовуються адитивні технології, вже сьогодні нагальною потребою вважаємо виготовлення пластикових прототипів при ранніх стадіях асептичного некрозу головки стегнової кістки та підготовці до її тунелізації, багатоплощинних деформаціях кінцівок, при підготовці до остеотомій тощо.
Висновки
1. Проведене дослідження визначило високу діагностичну цінність використання адитивних технологій при доопераційній підготовці хворих із різною ортопедо-травматологічною патологією.
2. 3D-моделювання та виготовлення пластикового прототипу дозволяє підібрати оптимальну конструкцію імплантів та визначити їх правильне просторове розташування під час підготовки до оперативного втручання, скоротити час оперативного втручання, зменшити кількість інтраопераційних ускладнень.
3. Ця технологія може бути рекомендована до впровадження в центри, які займаються ревізійним і складним ендопротезуванням, остеосинтезом та онкоортопедією.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Боев В.Д. Компьютерное моделирование / В.Д. Боев, Р.П. Сыпченко. — М.: ИНТУИТ. РУ, 2010. — 349 с.
2. Королев А.Л. Компьютерное моделирование / А.Л. Королев. — М.: Бином. Лаборатория знаний, 2010. — 232 с.
3. 3D-Printed Biopolymers for Tissue Engineering Application / Xiaoming LI., Rongrong C., Lianwen S. et al. // International Journal of Polymer Science. — 2014. — Article: ID 829145.
4. Application of the polystyrene model made by 3D-printing rapid prototyping technology for operation planning in revision lumbar discectomy / Li C., Yang M., Xie Y. et al. // J. Orthop. Sci. — 2015. — № 20. — P. 475-480.
5. Docquier P.L. Surgical navigation in paediatric orthopaedics / P.L. Docquier, L. Paul, V. Tran Duy // EFORT Open Rev. — 2016. — № 1. — P. 152-159.
6. Harris W.H. Traumatic artthritis of the hip after dislocation and acetabular fractures treatment by mold artroplasty. An end result study using a new method of ressult evalution / W.H. Harris // J. Bone Jt. Surg. — 1969. — Vol. 51-A. — P. 737-743.
7. https://www.rbc.ru/own_business/24/12/2015/567a88529a794778d2f8bae4
8. Indexes of severity for osteoarthritis of the hip and knee. Validation-value in comparison with other assessment tests / Lequesne M.G., Mery C., Samson M., Gerard P. // Scand. J. Rheumatol. Suppl. — 1987. — Vol. 65. — P. 85-89.
9. Paprosky W. Acetabular defect classification and surgical reconstruction in revision arthroplasty: a 6-year follow-up evaluation / W. Paprosky, P. Perona, J. Lawrence // J. Arthroplasty. — 1994. — Vol. 9. — P. 33-44.
10. The current status and future prospects of computer-assisted hip surgery / Inaba Y., Kobayashi N., Ike H. et al. // Journal of Orthopaedic Science. — 2016. — Vol. 21, № 2. — P. 107-115.
11. Userguided 3D-active contour segmentation of anatomical structures: significantly improved efficiency and reliability / Yushkevich P.A., Piven J., Hazlett H.C. et al. // Neuroimage. — 2006. — Vol. 31, № 31. — P. 116-1117.

/90-1.jpg)
/90-2.jpg)
/91-1.jpg)
/92-1.jpg)
/92-2.jpg)
/93-1.jpg)
/93-2.jpg)
/94-1.jpg)
/95-1.jpg)