Резюме
Актуальність. В ортопедії та травматології як гвинти та фіксаційні штифти, пластини, анкери, кейджі значне місце посідають полімерні матеріали, що резорбуються й розчиняються в біологічних рідинах. Перевагою таких імплантатів є їх повне розсмоктування, що позбавляє від необхідності операції з видаленням імплантату. Підвищити якість біоматеріалів на основі полілактидів можливо шляхом введення в їх склад керамічних матеріалів, зокрема гідроксіапатиту. Однак імплантати з різним відсотковим співвідношенням і складом керамічного матеріалу розрізняються властивостями міцності та поведінки в кістці. Мета. В експерименті на тваринах дослідити тривалість збереження стабільності фіксації кісткових уламків за допомогою накісткових пластин, виготовлених з біодеградуючих матеріалів на основі полілактиду. Матеріали та методи. Експеримент проводили на 20 кроликах-самцях віком 6 місяців. Усім тваринам моделювали перелом діафіза правої стегнової кістки в середній третині шляхом розпилу та виконували остеосинтез накістковою пластиною, виготовленою за допомогою 3D-друку з матеріалу на основі полілактиду з домішкою 20% трикальційфосфату та 10% гідроксіапатиту. Кроликів виводили з експерименту групами по 5 тварин через 1, 3, 6 та 12 місяців після початку експерименту. Після виведення з експерименту у тварин виділяли оперовану та контралатеральну стегнові кістки. Контралатеральні (неоперовані) кістки тварин вважали за групу конт-ролю. Всі препарати стегнових кісток кроликів випробували на міцність під впливом навантаження на згин. Згинаюче навантаження збільшували від 50 до 100 Н із кроком у 10 Н. При кожній величині навантаження вимірювали величину прогину препарату. Результати. В результаті проведених досліджень нами було отримано величини прогину препаратів стегнових кісток кроликів на різних термінах проведення експерименту під впливом згинаючих навантажень різної величини. Обробка даних за методами описової статистики дала можливість отримати середні значення та стандартне відхилення величини прогину в різних експериментальних групах, а також порівняти величини деформації препаратів між різними групами. Висновки. Накісткові пластини на основі полілактиду з домішкою 20% трикальційфосфату та 10% гідроксіапатиту забезпечують збереження своїх початкових механічних властивостей протягом усього терміну зрощення переломів стегнової кістки кроликів, що сприяло досягненню повного зрощення уламків кісток.
Актуальность. В ортопедии и травматологии в качестве винтов и фиксационных штифтов, пластин и анкеров, кейджей значительное место занимают полимерные материалы, которые резорбируются и растворяются в биологических жидкостях. Преимуществом таких имплантатов является их полное рассасывание, что избавляет от необходимости операции с удалением имплантата. Повысить качество биоматериалов на основе полилактида возможно путем введения в их состав керамических материалов, в частности гидроксиапатита. Однако имплантаты с различным процентным соотношением и составом керамического материала различаются свойствами прочности и поведения в кости. Цель. В эксперименте на животных исследовать длительность сохранения стабильности фиксации костных отломков с помощью накостных пластин, изготовленных из биодеградируемых материалов на основе полилактида. Материалы и методы. Эксперимент проводили на 20 кроликах-самцах в возрасте 6 месяцев. Всем животным моделировали перелом диафиза правой бедренной кости в средней трети путем распила и выполняли остеосинтез накостной пластиной, изготовленной с помощью 3D-печати из материала на основе полилактида с примесью 20% трикальцийфосфата и 10% гидроксиапатита. Кроликов выводили из эксперимента группами по 5 животных через 1, 3, 6 и 12 месяцев после начала эксперимента. После вывода из эксперимента у животных выделяли оперированную и контралатерально бедренные кости. Контралатеральные (неоперированные) кости животных выполняли роль группы контроля. Все препараты бедренных костей кроликов испытали на прочность под воздействием нагрузки на изгиб. Сгибая, нагрузки увеличивали от 50 до 100 Н с шагом в 10 Н. При каждой величине нагрузки измеряли величину прогиба препарата. Результаты. В результате проведенных исследований нами были получены величины прогиба препаратов бедренных костей кроликов на разных сроках проведения эксперимента под влиянием изгибающих нагрузок различной величины. Обработка данных методами описательной статистики позволила получить средние значения и стандартное отклонение величины прогиба в различных экспериментальных группах, а также сравнить величины деформации препаратов между различными группами. Выводы. Накостные пластины на основе полилактида с примесью 20% трикальцийфосфата и 10% гидроксиапатита обеспечивают сохранение своих первоначальных механических свойств в течение всего срока срастания переломов бедренной кости кроликов, что позволило достичь полного сращения отломков костей.
Background. In orthopedics and traumatology, polymeric materials that resorb and dissolve in biological fluids occupy a significant place as screws and fixing pins, plates and anchors, cages. The advantage of these implants is their complete resorption, which eliminates the need for surgery to remove the implant. Increasing the quality of polylactide biomaterials is possible by inclusion of ceramic materials into their composition, in particular, hydroxyapatite. However, implants with different percentage ratios and composition of ceramic materials differ in strength and behavior in the bone. Objective: in animal experiment, to study the duration of maintaining the stability of bone fragments with the help of plates made from biodegradable polylactide materials. Materials and methods. The experiment was performed on 20 male rabbits aged 6 months. In all animals, diaphyseal fractures in the middle third of the right femur were modeled by cutting, and osteosynthesis was performed with an external plate made of polylactide material with an admixture of 20% tricalcium phosphate and 10% hydroxyapatite using 3D-printing. Rabbits were sacrificed in groups of 5 animals each after 1, 3, 6 and 12 months from the start of the experiment. Following sacrificing, operated and contralateral femoral bones were separated. Contralateral (intact) bones served as a control group. All samples of femoral bones of rabbits were tested for strength under the influence of bending loads. Bending load was increased from 50 to 100 N in increments of 10 N. For each load, the value of sample bending was measured. Results. As a result of our research, we obtained the values of sample (femoral bones of rabbits) bending in different terms of the experiment, under the influence of different bending loads. Data processing by means of descriptive statistics allowed obtaining average parameters and standard deviation of bending value in various experimental groups, as well as comparing the deformation of samples between different groups. Conclusions. Polylactide external plates with an admixture of 20% tricalcium phosphate and 10% hydroxyapatite ensure the preservation of initial mechanical properties during the entire period of healing of femoral fractures in rabbits, allowed achieving complete adhesion of bone fragments.
Вступ
В ортопедії та травматології як гвинти та фіксаційні штифти, пластини, анкери, кейджі значне місце посідають полімерні матеріали, що резорбуються та розчиняються в біологічних рідинах [1, 2].
Серед таких матеріалів частіше використовують імплантати з L-полімолочної кислоти (L-полілактид), особливістю яких є біодеградація, остеоінтеграція, здатність індукувати процеси утворення кісткової тканини та висока біосумісність з організмом [1, 3]. Перевагою таких імплантатів є їх повне розсмоктування, що позбавляє від необхідності операції з видаленням імплантату або фіксуючого пристрою, відповідно, запобігає ушкодженню тканин. Підвищити якість біоматеріалів на основі полілактидів можливо шляхом введення в їх склад керамічних матеріалів, зокрема гідроксіапатиту [4, 5]. Однак імплантати з різним відсотковим співвідношенням і складом керамічного матеріалу розрізняються властивостями міцності та поведінки в кістці.
Мета: в експерименті на тваринах дослідити тривалість збереження стабільності фіксації кісткових уламків за допомогою накісткових пластин, виготовлених із біодеградуючих матеріалів на основі полілактиду.
Матеріали та методи
В лабораторії біомеханіки ДУ «ІПХС ім. проф. М.І. Ситенка НАМН» було проведено експериментальні дослідження міцності стегнових кісток кроликів після остеосинтезу модельованих переломів накістковими пластинами, виготовленими за допомогою 3D-друку з матеріалу на основі полілактиду (PLA) з домішкою 20% трикальційфосфату (ТКФ) та 10% гідроксіапатиту (ГА).
Експеримент проводили на 20 кроликах-самцях віком 6 місяців. На основі ISO10993-6:2004 (Національні стандарти України. Біологічне оцінювання медичних виробів, 2006) [6, 7] усім тваринам моделювали перелом діафіза правої стегнової кістки в середній третині шляхом розпилу та виконували остеосинтез накістковою пластиною. Склад матеріалу пластини: PLA — 70%, ТКФ — 20%, ГА — 10%. Кроликів виводили з експерименту групами по 5 тварин через 1, 3, 6 та 12 місяців після початку експерименту. Після виведення з експерименту у тварин виділяли оперовану та контра-латеральну стегнові кістки. Контралатеральні (неоперовані) кістки тварин вважали за групу контролю.
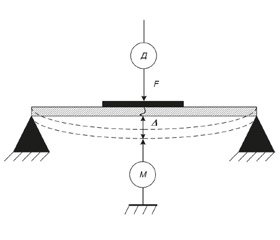
Всі препарати стегнових кісток кроликів випробували на міцність під впливом навантаження на згин. Схему проведення випробувань препаратів стегнових кісток кроликів на згин наведено на рис. 1.
Препарати стегнових кісток кроликів жорстко закріплювали за проксимальний і дистальний кінці. Згинаюче навантаження прикладали в зоні перелому з боку накісткової пластини. Згинаюче навантаження збільшували від 50 до 100 Н із кроком у 10 Н. При кожній величині навантаження вимірювали величину прогину препарату.
Величину деформації вимірювали мікрометром годинникового типу. Величину навантаження вимірювали за допомогою тензометричного датчика SBA-100L, результати контролювали пристроєм реєстрації CAS типу CI-2001A.
Отримані дані експерименту були оброблені за статистичними методами [8]. В результаті статистичного аналізу визначали середнє значення (М) величини деформації моделей для кожного значення навантаження та її стандартне відхилення (SD). Порівняння величин деформації препаратів між різними групами проводили за допомогою дисперсійного аналізу (ANOVA) з апостеріорним тестом Дункана.
Обробку даних для статистичних розрахунків проводили за допомогою електронних таблиць MS Excel. Статистичний аналіз виконували за допомогою пакета прикладних програм для статистичної обробки даних SPSS 20.0.
Результати та обговорення
Під час досліджень нами було отримано величини прогину препаратів стегнових кісток кроликів на різних термінах проведення експерименту під впливом згинаючих навантажень різної величини. Обробка даних методами описової статистики дала можливість отримати середні значення та стандартне відхилення величини прогину в різних експериментальних групах (табл. 1).
Результати дисперсійного аналізу ANOVA показали, що при всіх значеннях навантаження є значущі відмінності між різними групами препаратів стегнової кістки. Це стало підставою для пошуку визначення питання про те, між якими групами існують ці відмінності при кожній з величин навантаження. Відповідь на це питання було отримано за допомогою апостеріорного тесту Дункана. В табл. 2 наведені результати апостеріорного тесту Дункана для величин прогину препаратів стегнової кістки кроликів під впливом згинаючого навантаження величиною 50 Н.
/100-1.jpg)
Дослідження величини прогину препаратів стегнової кістки кроликів під впливом згинаючого навантаження величиною 50 Н показало, що найменша величина прогину (106 ± 4 мкм) спостерігалась через 3 місяці після моделювання перелому. Це статистично значущо відрізняється від інших груп досліджених препаратів, про що свідчить їх потрапляння у першу підгрупу за результатами апостеріорного тесту Дункана. Найбільшу величину прогину (802 ± 4 мкм) визначали на препаратах із терміном спостереження 1 місяць, що також має статистично значущу відмінність від препаратів інших груп. Величини прогину препаратів, які було взято в термін 6 та 12 місяців, статистично значущо не відрізнялись від показників препаратів контрольної групи (р = 0,105), на що вказує і розміщення їх в окремій підгрупі за результатами тесту Дункана.
Наочно порівняти величини прогину препаратів стегнової кістки кроликів під впливом згинаючого навантаження величиною 50 Н можна за допомогою діаграми (рис. 2).
При збільшенні величини згинаючого навантаження до 60 Н картина розбіжностей показників прогину препаратів стегнової кістки кроликів декілька змінюється. Про це свідчать результати апостеріорного тесту Дункана, що подані у вигляді табл. 3.
/100-3.jpg)
Як показано в табл. 3, при згинаючих навантаженнях величиною 60 Н група препаратів стегнових кісток кроликів, отриманих у термін 3 місяці після моделювання перелому, демонструє найкращі результати за величиною прогину (128 ± 5 мкм), що статистично значущо відрізняє їх від інших груп досліджених препаратів, тому за результатами тесту Дункана віднесено в окрему першу підгрупу. Аналогічно, найгірші результати величини прогину (958 ± 2 мкм) отримано в групі препаратів стегнових кісток тварин, яких виведено з експерименту в термін 1 місяць після моделювання перелому. Наявність статистичної значущості відмін дозволило віднести їх в окрему четверту підгрупу. На відміну від попереднього дослідження в окрему другу підгрупу за величиною прогину (244 ± 4 мкм) за допомогою апостеріорного тесту Дункана виділено групу препаратів із терміном спостереження 6 місяців з початку експерименту. Це свідчить про наявність статистично значущих відмінностей між препаратами цієї групи та контрольними контралатеральними кістками. Препарати, які отримано в термін 12 місяців після моделювання переломів, за величиною прогину (322 ± 18 мкм) статистично значущо не відрізнялись (р = 0,151) від контрольних препаратів контралатеральніх кісток піддослідних тварин (304 ± 2 мкм).
Для більш зручного порівняння величин прогину препаратів стегнових кісток кроликів під впливом згинаючого навантаження величиною 60 Н результати випробувань наведені у вигляді діаграми на рис. 3.
Підвищення величини навантаження до 70 Н не внесло суттєвих змін у характер відмінностей між групами препаратів стегнових кісток кроликів на різних етапах зрощення переломів. Це підтверджується результатами апостеріорного тесту Дункана, які наведені в табл. 4.
/101-2.jpg)
Згідно з табл 4, із підвищенням величини навантаження до 70 Н характер відмінностей між групами досліджених препаратів стегнових кісток кроликів не змінився. Найкращий (162 ± 6 мкм) і найгірший (1116 ± 12 мкм) результати величини прогину показали, відповідно, препарати після 3 місяців моделювання переломів та після 1 місяця тривалості експерименту. Розміщення їх в окремих підгрупах свідчить про наявність статистично значущих відмінностей. Також в окрему групу за результатами величини прогину (264 ± 5 мкм) потрапили препарати стегнових кісток після 6 місяців зрощення переломів. Кістки тварин, які було досліджено після 12 місяців з моменту моделювання переломів, за величиною прогину (326 ± 12 мкм) не мали статистично значущих відмінностей від групи контрольних контралатеральних кісток (314 ± 11 мкм).
Детальніше порівняти величини прогину препаратів стегнових кісток піддослідних тварин під впливом навантаження на згин величиною 70 Н на різних етапах тривалості експерименту можна за допомогою діаграми, що наведена на рис. 4.
При подальшому збільшенні величини згинаючого навантаження до 80 Н спостерігається картина розбіжності відмінностей величин прогину препаратів стегнових кісток кроликів між групами на різних етапах перебігу експерименту (табл. 5).
/102-1.jpg)
Як видно, підвищення величини навантаження до 80 Н привело до того, що всі групи препаратів стегнових кісток кроликів мають значущі відмінності одна від одної за показниками величини прогину. Це підтверджується результатами тесту Дункана, за яким їх розташовано по окремих підгрупах. Традиційно, найгірший результат величини прогину (1268 ± 9 мкм) показали препарати, що були отримані місяць тому після моделювання перелому. Найбільший спротив згинаючим навантаженням здійснювали препарати після тримісячного зрощення перелому. Величина прогину в цій групі становила 202 ± 20 мкм. Препарати стегнових кісток кроликів, які було випробувано в терміни 6 та 12 місяців після початку експерименту, були трохи міцніші за контрольну групу (402 ± 14 мкм), показавши величину прогину 302 ± 12 мкм та 358 ± 12 мкм відповідно.
Наочно оцінити різницю величин прогину препаратів стегнової кістки кроликів під впливом згинаючого навантаження величиною 80 Н у різні терміни зрощення переломів можна за допомогою діаграми, яка наведена на рис. 5.
У табл. 6 наведені результати апостеріорного тесту Дункана для величин прогину препаратів стегнової кістки кроликів з модельованим переломом у середній третині на різних термінах їх зрощення під впливом згинаючого навантаження величиною 90 Н.
Наведена табл. 6 наглядно демонструє, що збільшення величини навантаження до 90 Н не призводить до кардинальних змін у розбіжностях показників величини прогину препаратів стегнової кістки кроликів між різними групами. Найкращі результати (184 ± 13 мкм), як і раніше, демонструють препарати, що були підлеглі випробуванням після трьох місяців з початку експерименту. Найгірші (1460 ± 15 мкм) належать групі препаратів, які було випробувано в термін місяць після моделювання перелому. Препарати, що було отримано після 12 місяців тривалості експерименту, за величиною прогину (422 ± 2 мкм) не мали статистично значущих відмінностей від препаратів контрольної групи (438 ± 15 мкм), тому за результатами апостеріорного тесту Дункана потрапили до однієї підгрупи.
Для більш зручного порівняння величин прогину препаратів стегнових кісток кроликів під впливом згинаючого навантаження величиною 90 Н результати випробувань представлені у вигляді діаграми, що наведена на рис. 6.
Підвищення величини навантаження до 100 Н не внесло суттєвих змін в характер відмінностей між групами препаратів стегнових кісток кроликів на різних етапах зрощення переломів. Це підтверджується результатами апостеріорного тесту Дункана (табл. 7).
/103-2.jpg)
Отже, картина відмінностей результатів випробувань на згин препаратів стегнових кісток кроликів на різних термінах зрощення переломів при збільшенні величини навантаження до 100 Н практично не змінилась. Знову виявилась статистична значущість розбіжностей за величиною прогину між препаратами контрольної групи (492 ± 23 мкм) та препаратами з терміном зрощення 12 місяців (442 ± 7 мкм). Кращі результати (214 ± 12 мкм), як і раніше, належать препаратам групи після 3 місяців моделювання переломів порівняно з найгіршіми (1618 ± 19 мкм). Розміщення всіх груп досліджених препаратів до окремих підгруп, за результатами апостеріорного тесту Дункана, свідчить про наявність статистично значущих відмінностей між усіма групами. Порівняння величини прогину препаратів стегнових кісток під впливом навантаження величиною 100 Н — на діаграмі (рис. 7).
Проведений біомеханічний експеримент щодо визначення міцності з’єднання уламків стегнових кісток кроликів за допомогою накісткових пластин із матеріалу на основі полілактиду з домішкою 30 % трикальційфосфату показав, що найгірший результат спостерігався на препаратах після одного місяця моделювання перелому. Це можна пояснити тим, що в цей термін кістковий регенерат у зоні перелому не набрав достатньої міцності для створення значної протидії згинаючим навантаженням, тому механічний спротив здійснювався тільки накістковою пластиною. Після трьох місяців з початку експерименту кістки кроликів досягають повного зрощення, а міцність кісткового регенерату дорівнює міцності здорової кісткової тканини, але величини прогину препаратів на цьому етапі статистично значущо кращі за препарати контрольної (неоперованої) кінцівки. Цей факт може свідчити про те, що процес біодеградації матеріалу, з якого були зроблені накісткові пластини, ще не почався, і пластини зберігають початкові міцнісні властивості, тому спротив згинаючим навантаженням надають як кісткова тканина, так і накісткова пластина, завдяки чому маємо найкращій результат саме в цій групі препаратів.
Група препаратів із терміном зрощення 6 місяців, починаючи з навантаження величиною 60 Н, за величиною прогину статистично значущо відрізняється від препаратів контрольної групи в позитивному напрямку, але також статистично значущо поступається препаратам з терміном зрощення 3 місяці. Це може бути вказівкою на те, що процес біодеградації матеріалу почався, але його міцність поки ще достатня для надання дійсного спротиву згинаючим навантаженням. Про що не можна сказати про препарати з терміном зрощення 12 місяців, які практично не мають статистично значущих відмінностей від препаратів контрольної групи. Набування ними статистично значущої різниці в показниках прогину при деяких високих значеннях згинаючих навантажень може бути пояснене нерівномірністю процесу біодеградації між окремими пластинами.
Висновки
Накісткові пластини на основі полілактиду з домішкою 20% трикальційфосфату та 10% гідроксіапатиту забезпечують збереження своїх початкових механічних властивостей протягом усього терміну зрощення переломів стегнової кістки кроликів, що дало можливість досягти повного зрощення уламків кісток.
Список литературы
1. Биорезорбируемые полимеры в ортопедии и травматологии / Радченко В.А., Дедух Н.В., Малышкина С., Бенгус Л.М // Ортопедия, травматология и протезирование. — 2006. — № 3. — С. 116-124.
2. Bioabsorbable materials in orthopaedics / G.M. Kontakis, J.E. Pagkalos, T.I. Tosounidis, J. Melissas, P. Katonis // Acta Orthop. Belg. — 2007. — Vol. 73. — P. 159-169.
3. Терещенко В.П. Матрицы-носители в тканевой инженерии костной ткани / В.П. Терещенко, И.А. Кирилова, П.М. Ларионов // Успехи современного естествознания. — 2015. — № 8. — С. 66-70.
4. Имплантационные материалы и остеогенез. Роль индукции и кондукции в остеогенезе / Н.А. Корж, В.А. Радченко, Л.А. Кладченко, C.В. Малышкина // Ортопед., травматол. и протезир. — 2003. — № 2. — С. 150-15.
5. Семикозов О.В. Экспериментальное обоснование применения для костной пластики пористого минералонаполненного композита полилактида, подвергнутого воздействию сверхкритической среды СО2: Автореф. дис... канд. мед. наук 14.00.16 / Семикозов О.В. — ГОУВПО «Российский университет дружбы народов». — Москва, 2008. — 25 с.: 29 ил.
6. Європейська конвенція про захист хребетних тварин, що використовуються для дослідних та інших наукових цілей. Страсбург, 18 березня 1986 року: офіційний переклад [Електронний ресурс] / Верховна Рада України. — Офіц. веб-сайт. — (Міжнародний документ Ради Європи). — Режим доступу до документа: http: zakon.rada.gov.ua/cgi-bin/laws/main.cgi?nreg = 994_137.
7. Закон України № 3447-IV від 21.02.2006 р. «Про захист тварин від жорстокого поводження» (стаття 26).
8. Бююль Ахим. SPSS: искусство обработки информации. Анализ статистических данных и восстановление скрытых закономерностей: пер. с нем. / Ахим Бююль, Петер Цефлер. — СПб.: ООО «ДиаСофтЮП», 2005. — 608 с.

/99-1.jpg)
/99-2.jpg)
/100-1.jpg)
/100-2.jpg)
/100-3.jpg)
/101-1.jpg)
/101-2.jpg)
/102-1.jpg)
/102-2.jpg)
/102-3.jpg)
/103-1.jpg)
/103-2.jpg)