Введение
Нейротравматизм в конце XX и начале XXI века стал актуальнейшей проблемой здравоохранения всех стран. Многочисленные эпидемиологические исследования черепно-мозговой травмы (ЧМТ) свидетельствуют о ее значительной распространенности. В общей структуре травматизма на долю ЧМТ приходится от 30 до 50 %. Частота ее колеблется от 180 до 540 случаев на 100 тыс. населения в год. Возрастает доля ЧМТ легкой степени, которые при недостаточном внимании со стороны медицинских учреждений и недооценке пострадавшими своего состояния в дальнейшем проявляются последствиями в виде различных нарушений, приводящих к ограничению жизнедеятельности пострадавших. В Украине ежегодно получают ЧМТ около 100 тыс. человек (2 на 1 тыс. жителей) [1]. Показатель уровня травматизма среди взрослого населения Харьковской области в 2015 г. составил 274,1 на 10 тыс. В структуре смертности травмы занимали третье место — 5,6 %, уступая лишь показателям смертности от заболеваний системы кровообращения (70,6 %) и новообразований (14,4 %) [2]. В силу морфофункциональных особенностей репаративные возможности головного мозга крайне ограниченны, что приводит к высокой частоте инвалидизации при ЧМТ. Больные с последствиями ЧМТ длительное время, а зачастую и пожизненно социально не адаптированы. Именно поэтому ученые всего мира продолжают изучать патогенез и усовершенствовать диагностические и лечебно-реабилитационные мероприятия при ЧМТ во все ее периоды.
Современная теория патогенеза ЧМТ основана на действии первичных и вторичных повреждающих факторов [3, 4]. Важными факторами повреждения после ЧМТ являются: активация иммунного воспаления, дефицит нейротрофических факторов. Наряду с процессами вторичного повреждения тканей мозга при ЧМТ запускаются процессы нейрорегенерации и нейропротекции. В частности, астроциты и микроглия экспрессируют фактор роста, выделенный из головного мозга (BDNF), и другие нейропротективные факторы, а именно фактор роста нервов (NGF), ней-ротрофин-3; вырабатывают противовоспалительные цитокины и хемокины (CD206, CD163, FcyR, аргиназа 1, TGFβ) [5, 6]. NGF участвует в росте, пластических перестройках нейронов при дифференцировке, а также в поддержании их жизнедеятельности в центральной и периферической нервной системе как в норме, так и при патологии. Сегодня уже широко известно, что эффективная нейропротекторная терапия ЧМТ, мозгового инсульта и глобальной ишемии мозга состоит в первую очередь из первичной нейропротекции, которая должна быть направлена прежде всего на восстановление свойств нейроглии [7–9]. Вторичная нейропротекция, влияющая преимущественно на нейроциты, осуществляется только после начала проведения первичной нейропротективной терапии. Считается, что в основе клинического проявления даже самой легкой формы ЧМТ (сотрясение мозга) лежит асинапсия, преимущественно функциональная. Возникающая при этом дегенерация холинергических нейронов и снижение уровня ацетилхолина в корковых и подкорковых структурах головного мозга ответственны за развитие облигатных клинических проявлений заболевания — очаговых расстройств, нарушений памяти и высших корковых функций. Нарушения когнитивных функций в молодом и среднем возрасте как последствия ЧМТ многообразны и являются отражением патологии острого периода либо выявляются впервые. Показано, что более чем у 35 % больных, перенесших ЧМТ легкой степени тяжести, в последующем наблюдаются когнитивные нарушения (КН) различной степени выраженности, а после тяжелой травмы это число значительно выше [10].
Одним из направлений в разработке стратегии лечения ЧМТ считается компенсация холинергической недостаточности. Наиболее эффективным методом такой компенсаторной терапии признается применение ингибиторов ацетилхолинэстеразы, предотвращающих разрушение ацетилхолина в синаптической щели [11]. Включение их в схему реабилитации позволяет за счет дополнительной активации нейропластичности значительно ускорить и сделать более эффективным процесс восстановления.
Наше внимание привлек препарат Нейромидин®, который уже много лет присутствует в медицинской практике в Украине и обладает всеми необходимыми свойствами стимулятора нейротрофической функции при повреждениях нервной системы. Среди ключевых механизмов Нейромидина® отмечено его положительное влияние на адаптивную нейропластичность, что создает предпосылки для интенсификации разветвления нейронов. Препарат обладает хорошей терапевтической эффективностью: стимулирует проведение импульса по нервному волокну и улучшает нервно-мышечную передачу, нарушенную вследствие воздействия различных факторов, в том числе при травматическом повреждении; улучшает процессы памяти, тем самым затормаживая прогредиентное развитие деменции; специфически умеренно стимулирует центральную нервную систему с отдельными проявлениями седативного эффекта; проявляет анальгезирующие свойства.
Цель исследования — оценить клиническую эффективность препарата Нейромидин® в восстановлении нарушенной когнитивной сферы при ЧМТ.
Материалы и методы
Нами было обследовано 80 пациентов с ЧМТ (79 % из них с сотрясением головного мозга, 21 % — с ушибом головного мозга легкой степени). Все пациенты находились на стационарном лечении в КУЗ «Центр экстренной медицинской помощи и медицины катастроф» г. Харькова. ЧМТ была подтверждена клинико-неврологическим статусом и лабораторно-инструментальными методами исследования. Критериями включения в исследование были: возраст больных 25–60 лет; наличие полученной впервые ЧМТ легкой или средней степени тяжести в остром и раннем восстановительном периоде; информированное согласие больных на исследование. Пациент исключался из исследования, если у него имелись тяжелые соматические и неврологические заболевания, 2 и более ЧМТ в анамнезе, функциональная недостаточность печени и почек, лекарственная и наркотическая зависимость, беременность, получение травмы в состоянии алкогольного опьянения, а также при его отказе от участия. Критериями исключения также были противопоказания к использованию препарата Нейромидин®: эпилепсия, экстрапирамидные расстройства, стенокардия, выраженная брадикардия, бронхиальная астма, гиперфункция щитовидной железы, язвенная болезнь, мочекаменная болезнь, повышенная чувствительность к препарату.
Исследование проводили в 2 этапа: 1-й этап — 1–2-е сутки после поступления в стационар; 2-й этап — окончание курса терапии, который составил 2 месяца. На первом этапе было отобрано по 40 пациентов в остром и раннем восстановительном периоде ЧМТ. Все больные были распределены на две равноценные группы: І группа — основная и ІІ группа — контрольная. Каждая группа состояла из 40 пациентов (20 — острый период (ОП) ЧМТ, 20 — с ЧМТ в раннем восстановительном периоде (РВП)). Пациентам І группы в схему стандартной терапии включали препарат Нейромидин®, пациенты ІІ группы получали только стандартную терапию. Терапия Нейромидином® осуществлялась по такой схеме: внутримышечные инъекции 15 мг 2 раза в день курсом 10 дней, затем по 1 таблетке (20 мг) 3 раза в день курсом 1,5 мес. для пациентов в остром периоде ЧМТ и по 1 таблетке (20 мг) три раза в день курсом 2 мес. для пациентов с ЧМТ в раннем восстановительном периоде.
Степень неврологического дефицита и иных нарушений оценивали при клинико-неврологическом осмотре и с использованием психодиагностических шкал для выявления когнитивных нарушений (КН). Когнитивные функции оценивали по Монреальской шкале когнитивных функций (МоСА). Результаты исследования памяти, утомляемости, активности внимания и работоспособности у больных оценивали с помощью методики заучивания 10 слов (по А.П. Лурия) и с использованием таблиц Шульте. Самооценку своего психоэмоционального состояния пациенты давали при помощи опросника САН (самочувствие, активность, настроение). Исследование основных сфер жизнедеятельности пациентов проводили методом оценки качества жизни (КЖ), используя опросник MOS SF-36 (MOS 36-Item Short-Form Health Survey). Оценка репаративных возможностей головного мозга после травматического повреждения проводилась с помощью определения нейротрофического фактора роста нервов в сыворотке крови (бета-NGF) иммуноферментным методом на анализаторе с использованием набора для лабораторного анализа. Все полученные данные обрабатывались с использованием методов математической статистики.
Результаты и обсуждение
Стандартное клинико-неврологическое обследование больных с ЧМТ позволило выявить полисиндромную неврологическую симптоматику. В остром периоде ЧМТ на фоне стресса жалобы больных были немногочисленны, в основном на общую слабость (96 %), головную боль (94 %), головокружение и шаткость при ходьбе (92 %), ухудшение памяти, внимания (80 %), подавленность настроения (74 %). При активном опросе больные отмечали апатию и сонливость (76 %), чувство тревоги за состояние собственного здоровья (63 %), раздражительность (54 %), слабость в конечностях (34 %), чувствительные нарушения (23 %), речевые нарушения (15 %), снижение зрения, слуха, тошноту. В раннем восстановительном периоде ЧМТ выявлено значительно меньшее количество жалоб у больных даже при активном опросе: головная боль с метеозависимостью (65 %), головная боль с общей слабостью (35 %), нарушение памяти и внимания (54 %), сонливость (23 %), неустойчивость настроения, нарушение общения. В неврологическом статусе полиморфность симптоматики также была более выражена в остром периоде ЧМТ: эмоционально-личностные расстройства с преобладанием тревожного компонента (98 %), горизонтальный нистагм (80 %), глазодвигательные нарушения (83 %), вегетативная дисфункция (80 %), цефалгический синдром (80 %), координаторные нарушения (77 %), симптомы пирамидной недостаточности (32 %) и др. В раннем восстановительном периоде ЧМТ диагностировали: эмоционально-личностные расстройства с преобладанием тревожного компонента (84 %), вегетативную дисфункцию (80 %), астенический синдром (79 %), цефалгический синдром (65 %), координаторные нарушения (47 %) и др.
Выявленные нами неспецифические нарушения формируют симптомокомплекс дезадаптации, который составляет основу социальной дезадаптации, ведущей к длительной потере трудоспособности и снижению КЖ. Формирование такого симптомокомплекса свидетельствует о дисфункции неспецифических систем головного мозга, что создает благоприятный фон для срыва неустойчивой и легко нарушаемой компенсации в разные периоды ЧМТ и лежит в основе когнитивных нарушений.
Широко известно, что ЧМТ в любом периоде оказывает прямое влияние на особенности психического напряжения, эмоционального состояния и общего самочувствия травмированного. Для исследования состояния психоэмоциональной и когнитивной сфер проводился целенаправленный опрос пациентов о состоянии памяти, умственной работоспособности. При этом учитывалось, что самооценка больными этих функций часто не отражала истинного положения вещей, поскольку при наличии тревожных или депрессивных расстройств часто отмечается субъективное ухудшение памяти, сниженная переносимость умственных нагрузок. Нарушение психоэмоционального состояния по данным теста САН было выявлено у 88 % обследованных, о чем свидетельствовало достоверное снижение всех функциональных показателей во всех периодах ЧМТ. Также была выявлена их диспропорция — превалировало снижение самочувствия и особенно активности. Это подтверждает то, что люди, перенесшие ЧМТ, характеризуются, как правило, более низкой активностью и, следовательно, работоспособностью.
Несмотря на отсутствие иногда субъективных жалоб когнитивного характера, особенно в острый период ЧМТ (за исключением амнестических расстройств) у больных и отсутствие выявленных КН при стандартном неврологическом обследовании, уже при проведении короткого психодиагностического тестирования результаты не соответствовали возрастной норме более чем у 90 % пациентов. Так, в остром периоде ЧМТ результаты тестов не соответствовали возрастной норме у 93 % больных. Доля легких КН составляла 62 %, а умеренных КН — 38 %; в раннем восстановительном периоде — 71 и 29 % соответственно без статистически достоверной разницы в группах. Тяжелую степень когнитивных нарушений (деменции) ни у кого из пациентов не обнаружили.
Показатели шкалы МоСА указывали на снижение когнитивных функций у 82,7 % пациентов. Так, в остром периоде ЧМТ результат теста составлял 22,7 ± 4,3 балла, в раннем восстановительном — 24,7 ± 2,3 балла. Наибольшее количество ошибок пациенты совершали при определении категориального сходства между предметами, отсроченном воспроизведении, в субтесте на внимание.
Изменения когнитивных функций подтверждали и результаты тестирования по таблицам Шульте, которые свидетельствовали об истощении внимания в виде снижения уровня активного внимания и об ухудшении способности к его переключению. Такие изменения наблюдали у всех пациентов с острой ЧМТ, при этом больше всего снижались темп выполнения задания (у 60 % больных) и способность к концентрации внимания (33 %). По-видимому, больным мешало сконцентрироваться и значительное снижение как субъективной, так и объективной работоспособности. В раннем восстановительном периоде ЧМТ низкие показатели темпа выполнения задания продемонстрировали 28 % больных, а расстройства концентрации внимания — 21 %. Среднее время выполнения задания (эффективность работы) составляло 146,52 ± 21,42 с. Увеличивалось и общее время выполнения задания: у больных с острой ЧМТ — до 230,9 ± 22,1 с; у больных в ранний восстановительный период — до 178,9 ± 20,3 с; контрольные показатели — 139,6 ± 9,8 с (рис. 1).
/29-1.jpg)
Темп выполнения задач по таблицам был неравномерным: кривая трудоспособности отличалась невысоким исходным уровнем у всех больных (41,43 ± 19,87 с — время, затраченное на первую таблицу) с постепенным и неуклонным ухудшением показателей (48,14 ± 20,73 с — время, затраченное на пятую таблицу). 46 % обследованных пациентов допускали в работе с таблицами различные ошибки. Такой неравномерный темп работы и увеличение количества ошибок с каждой последующей таблицей свидетельствуют о повышенной истощаемости внимания у больных в любой период ЧМТ.
О снижении работоспособности свидетельствуют результаты теста «10 слов», которые продемонстрировали увеличение количества ошибок к концу его выполнения. При исследовании памяти выявлено значительное ухудшение показателей зрительной и слуховой памяти, особенно в воспроизведении заученного материала, при отсутствии нарушения в механизмах запоминания. Также отмечали высокую степень отвлекаемости и низкий уровень внимания, снижение продуктивности непроизвольного и отсроченного запоминания вербального материала по сравнению с контрольными показателями. Несмотря на то, что результаты теста не выявили достоверных различий при непосредственном воспроизведении слов с подсказкой, результаты непосредственного воспроизведения без подсказки и отсроченного воспроизведения оказались достоверно сниженными (p < 0,01), что свидетельствует о нарушении всех показателей вербальной памяти. Полученные результаты говорят о расстройствах как кратковременной, так и долговременной памяти, что коррелировало с жалобами больных. Так, в остром периоде ЧМТ среднее значение непосредственной вербальной памяти (после первого зачитывания) составило 5,1 ± 0,3 слова, объем долговременной памяти — 6,8 ± 0,1 слова. В раннем восстановительном периоде ЧМТ объем непосредственной вербальной памяти составил 5,5 ± 0,3 слова, объем долговременной памяти — 7,0 ± 0,3 слова. Объем кратковременной и отсроченной памяти в контрольной группе составил соответственно 6,5 ± 0,7 и 9,3 ± 0,8 слова. 45 % больных с острой ЧМТ и 30 % больных в раннем восстановительном периоде не смогли полностью воспроизвести 10 слов даже после 5-кратного зачитывания. Только 18 % пациентов могли запомнить весь ряд уже после 4–5 зачитываний.
Таким образом, у обследованных нами больных преобладала легкая форма когнитивных нарушений (ЛКН), которые носили преимущественно нейродинамический характер. При этом страдают такие характеристики когнитивных процессов, как скорость обработки информации, способность быстро переключаться с одного вида деятельности на другой, оперативная память. Больные отмечали затруднения при осуществлении наиболее сложных и непривычных для них видов деятельности. Сегодня неоспорим тот факт, что отсутствие должной коррекции даже ЛКН, а также умеренных когнитивных нарушений (УКН) в дальнейшем может быстро привести к бытовой, социальной и профессиональной дезадаптации.
Положительные результаты проведенной терапии подтверждались субъективной оценкой пациентами своего состояния, что прежде всего выразилось в снижении жалоб на двигательную и координаторную функцию, появлении интереса и инициативы, мотор-ной активности. Наиболее заметными эти изменения были у больных І группы. Уменьшение выраженности головных болей и эмоционально-волевых нарушений позволило больным значительно улучшить взаимоотношения с окружающими и повысить повседневную активность. Это привело к более быстрой социализации (как в остром, так и в раннем восстановительном периоде) пациентов, принимавших Нейромидин®. Большинство больных (73 %) І группы уже ко второй неделе приема Нейромидина® отмечали улучшение настроения, ощущение восстановления сил, повышение внутренней энергии и работоспособности, а также уменьшение тревожности и чувства страха, нормализацию сна. Только 47 % больных ІІ группы назвали подобные улучшения на втором этапе исследования. У больных ІІ группы жалобы астенического характера регрессировали не полностью даже к концу 2-го этапа: оставалось чувство усталости, небольшая слабость, двигательная неуверенность, плаксивость, тревожность, иногда мешающие обычной жизнедеятельности.
Менее значительные изменения претерпевали церебрально-очаговые проявления (в частности пирамидная симптоматика, мозжечково-вестибулярная дисфункция, ликворная дистензия) и выраженность синдрома внутричерепной гипертензии на втором этапе в обеих группах, хотя положительная динамика была наиболее выражена у больных І группы. Несмотря на стойкость вегетативных нарушений, на фоне приема Нейромидина® отмечена положительная динамика в стабилизации деятельности вегетативной нервной системы (согласно субъективным ощущениям и объективным данным) у 50 % больных І группы в конце курса лечения, тогда как во ІІ группе эти изменения произошли лишь у 32 % больных.
После проведенной терапии результаты опросника САН показали субъективное улучшение самочувствия, повышение активности и фонового настроения во всех группах больных во все периоды ЧМТ (рис. 2). Особенно эффективным в этом направлении оказался препарат Нейромидин®. Так, пациенты І группы давали более высокие тестовые оценки (p < 0,05). В остром и раннем восстановительном периодах ЧМТ практически все показатели увеличились в 2–3 раза на фоне приема этого препарата и приближались к благоприятным и нормальным значениям (> 40 баллов) у 81 % пациентов. Тогда как на фоне стандартной терапии свое состояние как благоприятное и нормальное оценили 63 % пациентов.
/30-1.jpg)
Повышение оценки своего самочувствия, активности и фонового настроения во всех группах больных во все периоды ЧМТ не могло не отразиться на когнитивной сфере. У пациентов І группы в остром периоде ЧМТ в динамике лечения отмечали уменьшение количества УКН практически в 2 раза с увеличением доли ЛКН. В ранний восстановительный период в этой же группе больных фиксировали также уменьшение количества пациентов с УКН (рис. 3). Это позволяет говорить о регрессирующем характере КН на фоне терапии Нейромидином®. У больных ІІ группы такой выраженной динамики в остром периоде ЧМТ не наблюдали, а в раннем восстановительном периоде даже возрастала доля пациентов с УКН.
Подтверждением этого служили результаты психодиагностических шкал. Положительная динамика результатов шкалы МоСА во всех группах и во все периоды ЧМТ указывала на улучшение когнитивных функций на фоне проведенной терапии независимо от ее вида (рис. 4).
Однако на втором этапе исследования показатели во ІІ группе пациентов составили 24,5 ± 1,2 балла в острый период и 25,3 ± 2,2 балла (р < 0,01) в ранний восстановительный период ЧМТ. Тогда как больные І группы, которые принимали Нейромидин®, показали более выраженную динамику результатов теста — 27,5 ± 1,2 и 28,3 ± 1,2 балла в аналогичные периоды ЧМТ. Следует добавить, что этим пациентам понадобилось значительно меньше времени для выполнения теста. Таким образом, наиболее выраженная динамика результатов наблюдалась в остром периоде ЧМТ на фоне терапии Нейромидином®, что свидетельствует о важности вида терапии в этом периоде.
На фоне проводимой терапии были отмечены достоверные изменения показателей непосредственной вербальной памяти (тест «10 слов») у больных, которые принимали Нейромидин®, как в остром, так и в раннем восстановительном периоде ЧМТ (рис. 5). Кроме того, у этих пациентов достоверно уменьшилось количество ошибок с 2,5 ± 0,4 до 1,65 ± 0,20. У пациентов ІІ группы положительную динамику результатов теста наблюдали на уровне статистической тенденции.
Таким образом, использование в схеме терапии ЧМТ препарата Нейромидин®, особенно в остром периоде ЧМТ, позволит избежать прогрессирующего нарушения когнитивных функций в дальнейшем.
Улучшение психоэмоционального состояния и когнитивной сферы не могло не сказаться на оценке КЖ пациентами. На первом этапе исследования интегральная оценка КЖ по шкалам опросника SF-36 показала снижение физического, психического, эмоционального и социального функционирования у больных в остром и раннем восстановительном периоде ЧМТ. При этом наиболее существенное снижение наблюдали в группе больных в остром периоде ЧМТ.
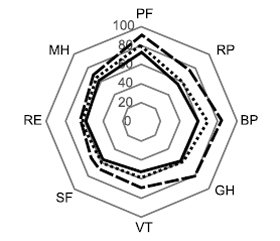
Анализ показателей шкал опросника SF-36, которые отражают физический (шкалы PF, RP, ВР, GH) и психологический компоненты здоровья (шкалы МН, RE, SF, VT), по завершении терапии показал, что у пациентов І группы имело место более значимое улучшение всех показателей качества жизни, чем у пациентов ІІ группы (рис. 6). Особенно это отразилось на таких показателях КЖ, как физическое и социальное функционирование, самооценка состояния своего здоровья, уменьшение интенсивности болевых ощущений.
/32-1.jpg)
Выявленная положительная динамика клинической картины заболевания на фоне проведенной терапии свидетельствует об активации процессов посттравматической адаптивной нейропластичности. Подтверждением этого может служить изменение нейропротективных факторов. Определение уровня бета-NGF (биологически активная часть молекулы NGF) в сыворотке крови у больных с ЧМТ на первом этапе исследования выявило его достоверное снижение (p < 0,05) без существенной разницы в обеих группах больных. Это указывает на активное участие бета-NGF в процессах нейропластичности.
О положительном влиянии Нейромидина® на адаптивную пластичность, которая создает предпосылки для роста отростков нейрона, свидетельствует изменение уровня бета-NGF в сыворотке крови у пациентов, перенесших ЧМТ, после проведенного курса терапии. На фоне достоверного снижения уровня бета-NGF до терапии во все периоды ЧМТ после проведенного лечения отмечено значительное повышение среднего значения этого маркера (в 2,3 раза) у больных І группы, в терапию которым добавлен препарат Нейромидин®. В то же время у больных ІІ группы этот показатель вырос в 1,2 раза. Причем наиболее выраженная положительная динамика была отмечена у больных в острый период ЧМТ (рис. 7).
Выводы
По результатам проведенного исследования установлено, что включение препарата Нейромидин® в стандартное лечение больных с легкой и средней ЧМТ в острый и ранний восстановительный периоды имеет более выраженный терапевтический эффект в сравнении с традиционной терапией. Назначение Нейромидина® уже в остром периоде ЧМТ способствовало более качественному и быстрому регрессу неврологических и когнитивных расстройств. Более высокий уровень мозгового глиального нейротрофического фактора бета-NGF в сыворотке крови больных, получавших Нейромидин®, свидетельствовал об активном влиянии препарата на стимуляцию процессов нейропластичности при травматическом повреждении головного мозга. Таким образом, клиническая эффективность Нейромидина® позволяет рекомендовать его включение в схемы стандартной терапии ЧМТ. А назначение препарата в остром периоде ЧМТ позволит избежать прогрессирующего нарушения когнитивных функций в дальнейшем.
Конфликт интересов. Не заявлен.
Список литературы
1. Лехан В.М. Особливості епідеміології черепно-мозкової травми в Україні / В.М. Лехан, А.П. Гук // Україна. Здоров’я нації. — 2010. — T. 2, № 14. — C. 7-14.
2. Григорова И.А., Тесленко О.А. Астеновегетативный синдром при черепно-мозговой травме и методы его коррекции // Український вісник психоневрології. Тези доповідей Національного конгресу неврологів, психіатрів та наркологів України. — Харків, 2017. — Т. 25, вип. 1 (90). — С. 76.
3. Крылов В.В., Талыпов А.Э., Пурас Ю.В. и др. Вторичные факторы повреждений головного мозга при черепно-мозговой травме // Российский медицинский журнал. — 2009. — № 3. — С. 23-28.
4. Reed A.R., Welsh D.G. Secondary injury in traumatic brain injury patients — a prospective study // S. Afr. Med. J. — 2012. — 92. — 221-224.
5. Wurzelmann M. Therapeutic potential of brain-derived neurotrophic factor (BDNF) and a small molecular mimics of BDNF for traumatic brain injury / M. Wurzelmann, J. Romeika, D. Sun // Neural. Regen. Res. — 2017. — Vol. 12, № 1. — P. 7-12.
6. Loane D.J. Microglia in the TBI brain: The good, the bad, and the dysregulated / D.J. Loane, A. Kumar // Exp. Neurol. — 2016. — Vol. 275, Pt. 3. — P. 316-27.
7. Румянцева С.А., Афанасьев В.В., Кузьмина Ю.В., Силина Е.В. Рациональная фармакокоррекция поражений мозга при острой и хронической ишемии // Consilium Medicum. — 2010. — Т. 12, № 9. — С. 21-29.
8. Черний Т.В. Концепция патогенетической нейропротекции пораженного мозга // Питання експериментальної та клінічної медицини: Зб. статей. — Донецьк, 2011. — Т. 1, вип. 15. — С. 137-143.
9. Румянцева С.А., Федин А.И., Афанасьев В.В., Елисеев Е.В., Мартынов М.Ю., Силина Е.В., Голузова Ю.Н. Алгоритмы терапии острого инсульта // Неврология. — М.: РГМУ им. Н.И. Пирогова, 2010. — 328 (тематический номер).
10. Стародубцев А.А. Клиническая картина травматической энцефалопатии и ее динамика у людей молодого возраста, перенесших СГМ / А.А. Стародубцев, А.И. Стародубцев // Неврологический журнал. — 2008. — Т. 13, № 4. — С. 15-19.
11. Нейромидин в клинической практике / Дамулин И.В., Живолупов С.А., Зайцев О.С., Максимова М.Ю., Маркин С.П., Самарцев И.Н., Санадзе А.Г., Строков И.А. — 2-е изд., перераб. и доп. — М.: Медицинское информационное агентство, 2016. — 60 с.

/29-1.jpg)
/30-1.jpg)
/30-2.jpg)
/31-1.jpg)
/31-2.jpg)
/32-1.jpg)
/32-2.jpg)