Статтю опубліковано на с. 72-79
Распространенность острого тонзиллофарингита (ОТФ) среди детей и взрослых (данный термин заменил применяемые ранее «тонзиллит», «ангина»), сложность быстрой диагностики его этиологии и, как следствие, лечения сделали данное заболевание одной из наиболее обсуждаемых проблем в отоларингологии. В странах Европы и Северной Америки, а также в Украине заболеваемость тонзиллофарингитом достигает 5 % во взрослой популяции и 10 % — в детской. При этом число больных хронической формой тонзиллита в 1,5 раза больше. В США ежегодно регистрируется до 15 млн детей, больных ОТФ [1, 2]. При ОТФ имеет место острое воспаление преимущественно небных миндалин, а также окружающих их тканей, протекающее с о–теком, гиперемией, наличием экссудата на миндалинах (тонзиллит) при участии слизистой оболочки глотки (фарингит). Заболевание часто сопровождается повышением температуры тела, интоксикацией, резкими болями при глотании и реакцией регионарных лимфатических узлов.
В проведенных в последние годы многочисленных исследованиях, как в нашей стране, так и за рубежом, получены достоверные данные, что основной и наиболее значимой причиной возникновения ОТФ является вирусная инфекция. Бактериальный возбудитель — β-гемолитический стрептококк группы А, ранее считающийся ведущим в этиологии заболевания, по частоте в разы уступает вирусным возбудителям. Ведущую позицию среди вирусов занимают аденовирус, вирус Эпштейна — Барр и энтеровирус, однако к воспалению лимфоидного глоточного кольца могут приводить и другие возбудители респираторных вирусных инфекций [3].
Системная антибактериальная терапия неэффективна в отношении вирусных тонзиллитов: не предотвращая бактериальную суперинфекцию, она потенцирует размножение бактериальной флоры, нечувствительной к данному противомикробному препарату, а также грибов, не говоря о развитии дисбиотических изменений в полости рта, носоглотке и желудочно-кишечном тракте (ЖКТ). Поэтому в настоящее время в мировой литературе данный вопрос практически не дискутируется, и нередко предлагается вести основную массу больных ОТФ без антибиотиков. Применение антибиотиков рекомендуется ограничить доказанными случаями стрептококковых тонзиллитов, несмотря на высокую вероятность их самопроизвольного разрешения. Это обусловлено тем, что пропущенный или неадекватно леченный стрептококковый тонзиллит чреват как (пусть и очень редко) гнойными (лимфаденит, абсцессы глотки), так и системными (острая ревматическая лихорадка, гломерулонефрит, PANDAS-синдром) осложнениями [4].
/72-79/72-1.jpg)
Однако до сегодняшнего дня большая часть больных детей с ОТФ подвергается необоснованному антибактериальному лечению. Причины этого — общность клинической картины всех форм заболевания и трудности этиологической диагностики при первичном осмотре пациента.
Необходимость этиологической дифференциации тонзиллитов уже в 1975 г. привела к созданию клинической оценочной шкалы Walsh. Позднее были попытки использования шкал Breese, Centor, и, наконец, в 1998 г. для детей (от 3 до 15 лет) была предложена шкала оценки клинических симптомов — шкала McIsaac, широко используемая сего–дня в мире и в Украине [5].
Вне зависимости от этиологии заболевания для ОТФ характерны:
— острое начало с температурой до 39–40 °С, –озноб, боли в горле;
— гиперемия слизистых миндалин, язычка и глотки;
— отечность миндалин, язычка и глотки;
— часто фолликулярный или лакунарный выпот;
— рыхлые налеты на миндалинах.
Шкала этиологической дифференциации тонзиллофарингитов McIsaac W:
— температура тела выше 38 °С — +1 балл;
— наличие экссудата на миндалинах — +1 балл;
— болезненные переднешейные лимфоузлы — +1 балл;
— отсутствие кашля — +1 балл;
— возраст до 15 лет — +1 балл;
— возраст больше 45 лет — –1 балл.
Оценка результатов:
— 0–1 балл — вероятность инфекции БГСА 1–10 %;
— 2–3 балла — вероятность инфекции БГСА 17–35 %;
— больше 4 баллов — вероятность инфекции БГСА 50 % и выше.
Таким образом, согласно оценке по шкале McIsaac при 0–1 балле антибиотики не применяются, используется местное и симптоматическое лечение. Если оценка по шкале McIsaac составляет 2 и более балла, необходимо провести бакпосев из зева или экспресс-тест на стрептококк. При их положительных результатах необходимо использование антибиотикотерапии, при отрицательных — антибиотикотерапия не назначается. В случаях наличия опасных симптомов, признаков скарлатины, осложнений, документированного контакта с больным, инфицированным бета-гемолитическим стрептококком группы А, ревматизма в анамнезе антибиотикотерапию следует начать до получения результатов посевов.
/72-79/73-1.jpg)
/72-79/73-2.jpg)
/72-79/73-3.jpg)
Вместе с тем следует учитывать, что использование шкалы ограничено: шкала не учитывает случаи ОТФ у детей младше 3 лет, а это более половины детей, госпитализированных по поводу изменений фарингоскопической картины. В этих случаях необходимо учитывать наличие катаральных явлений (гиперемия конъюнктив, затрудненное носовое дыхание), с большой вероятностью свидетельствующих в пользу вирусной этиологии заболевания.
Дополнительным дифференциально-диагностическим критерием могут служить данные, что на детей до 3 лет приходится лишь 2 % случаев бактериального тонзиллита. Напротив, у детей старше 12 лет бактериальный тонзиллит диагностировался почти в половине случаев. В дополнение у пациентов младшего возраста фарингоскопические изменения нередко сопровождаются появлением микровезикул на передних небных дужках при энтеровирусной и герпетической инфекции (герпангина), что также не предполагает антибактериальное лечение [6].
/72-79/74-1.jpg)
/72-79/74-2.jpg)
/72-79/74-3.jpg)
Сегодня на обязательное, как считалось ранее, назначение антибиотиков при ангине смотрят не так однозначно. Об осторожности применения системных антибиотиков при ОТФ свидетельствуют результаты проведенного в 2014 г. многоцентрового исследования, включившего 12 677 амбулаторных пациентов с острой болью в горле, из которых 4805 (38 %) получали только симптоматическую терапию. Лишь у 1,4 % из них возникли гнойные осложнения — в 62 % случаев это были острый средний отит и острый риносинусит, которые в большинстве случаев развиваются при затруднении носового дыхания на фоне течения ОРВИ. 6088 пациентов (48 %) получили антибиотик сразу, однако, как выяснилось после проведенного исследования, необходим он был лишь в 3 % случаев. 14 % пациентов начали получать антибиотики отсроченно, что реально требовалось только в 9,7 % случаев. Ретроспективно было подсчитано, что из всех пациентов антибактериальная терапия была показана только 3 % [7].
По данным Центра по контролю и профилактике заболеваний [8], подавляющее большинство (85 %) случаев острого тонзиллофарингита имеет вирусное происхождение (респираторные и энтеровирусы, вирус Эпштейна — Барр) и поэтому не требует назначения антибактериальной терапии. Вместе с тем, согласно многочисленным исследованиям в мире, а также данным ВОЗ, в более чем 70 % случаев антибактериальная терапия назначается при отсутствии показаний. То есть данный вид терапии не только не оказывает положительного влияния на течение заболевания (экспертная оценка ВОЗ), а наоборот, нередко приводит к неблагоприятным побочным явлениям [9]. Кроме того, формируются новые кланы антибиотикорезистентной микробной флоры, что в конце концов приведет к снижению возможностей этого, вне сомнения, важного для всего человечества метода терапии [10]. Более того, концепция моноэтиологичности заболеваний микробного происхождения в свете современных исследований о делении микробов на патогенные и непатогенные должна быть пересмотрена. Все микробы, обитающие в организме человека, одновременно пребывают в этих двух состояниях. Каждый из них при нарушении их баланса может быть причиной воспалительных процессов. Должна быть пересмотрена и концепция антибиотикотерапии. Ее фундамент — микробная моноэтиологичность и резистентность штаммов к антибиотикам в монокультуре in vitro — не адекватен форме существования микробного сообщества человека в норме и патологии.
Таким образом, подход к антибактериальному лечению детей с болями в горле должен быть ра–зумным и тщательно взвешенным: при исключении бактериальной инфекции ведущим методом в лечении ОТФ становится местная противовоспалительная терапия. Именно на рациональное и строго дифференцированное использование антибиотиков при ОТФ, подчеркивая при этом необходимость использования местной патогенетической и симптоматической терапии, указывают последние национальные и континентальные руководства по отоларингологии [11–15].
/72-79/75-1.jpg)
Местное лечение ОТФ имеет цель максимально быстро облегчить течение заболевания: снять воспалительные явления, боль, неприятные ощущения в горле, часто являющиеся причиной отказа пациентов от еды и питья, что у детей, особенно при наличии лихорадки, достаточно быстро может привес–ти к эксикозу. Выраженный болевой синдром при остром тонзиллофарингите является одной из ведущих жалоб и объясняется богатством иннервации глотки, что объясняет возможность иррадиации боли при заболевании глотки в ухо, нижнюю челюсть и т.д. Следует подчеркнуть, что именно воспалительный процесс при ОТФ вне зависимости от этиологии заболевания — бактериальной, вирусной, грибковой — обусловливает развивающуюся симптоматику. Поэтому и купирование механизмов воспалительных реакций является одним из важнейших методов местной терапии. В связи с этим сегодня при ОТФ небактериальной этиологии некоторыми клиницистами предлагаются нестероидные противовоспалительные препараты (НПВП). При этом нередко не учитывается, что НПВП относятся к средствам с частыми побочными эффектами, в том числе серьезными. Препараты данной группы, особенно для системного применения, нередко вызывают нежелательные побочные явления: гастропатию и нефропатию, гепатотоксичность и гематотоксичность, вплоть до развития при применении ацетилсалициловой кислоты синдрома Рея. В отдельных случаях прием НПВП вызывает бессимптомную энтеропатию, сопровож–дающуюся кровопотерей [16]. Нестероидные препараты уменьшают скорость почечного кровотока, способствуют задержке воды и натрия в организме, что может влиять на сосудистый тонус и состояние гемодинамики. Нередки на фоне терапии НПВП изменения в системах кроветворения и свертывания крови.
Ранее широко используемые местные антисептические и противовоспалительные средства в лечении ОТФ (препараты йода, перекись водорода, средства, содержащие фенол, альдегид, хлор) не рекомендованы в педиатрии вследствие неблагоприятных побочных воздействий и, кроме того, отсутствия эффекта при вирусной природе заболевания. Препараты данных групп подавляют нормальную микрофлору, повреждают слизистую оболочку ротоглотки и желудочно-кишечного тракта, нарушают местный иммунный ответ. Использование средств растительного происхождения (отвары и настойки эвкалипта, календулы, ромашки, каланхоэ) ограничено в связи с ростом числа аллергических реакций на данный вид терапии.
Поскольку механическое удаление налетов с миндалин или втирание лекарственных препаратов в слизистую оболочку недопустимо из-за опасности травмирования слизистой оболочки и риска развития гнойных осложнений, топический лекарственный препарат при ОТФ рекомендуется назначать в виде спрея, раствора для полоскания или таблеток для рассасывания.
Таким образом, с учетом разнообразия механизмов развития патогенетических сдвигов при ОТФ у детей и взрослых наиболее рациональным является использование топического препарата, обладающего комбинированным действием, по крайней мере антисептическим (противомикробным и противовирусным), анальгетическим и противовоспалительным, и в то же время безопасного. Более того, в педиатрической практике при лечении острого тонзиллофарингита независимо от этиологии заболевания имеет смысл дополнять терапию топическими средствами, обладающими данными свойствами. При бактериальной этиологии заболевания препараты этой группы являются дополнением к антибактериальной терапии, а при небактериальной — ведущим и направленным методом лечения.
К средствам, активно влияющим на различные патогенетические звенья воспалительного процесса в глотке, относится препарат, широко используемый за рубежом, а в последние годы и в Украине, — бензидамина гидрохлорид (Тантум Верде®). Этот НПВП относится к группе индазолов комбинированного действия для местного применения. Но, в отличие от остальных НПВП, не содержит карбоксильной группы, что придает ему ряд особенностей: он является слабым основанием, тогда как большинство НПВП — слабые кислоты; обладает высокой липофильностью; по градиенту рН хорошо проникает в очаг воспаления, где рН ниже, и накап–ливается в терапевтических концентрациях.
Бензидамина гидрохлорид обладает выраженным противовоспалительным, местноанестезирующим и противоотечным действием. Механизм действия препарата связан с угнетением продукции и блокированием активности провоспалительных цитокинов, в частности фактора некроза опухоли α и интерлейкина-1β, ингибированием синтеза простагландинов. В связи с этим бензидамина гидро–хлорид классифицирован как цитокинподавляющий противовоспалительный препарат [18]. Тантум Верде® способствует уменьшению проницаемости капилляров, стабилизации мембран лизосом, торможению процесса окислительного фосфорилирования за счет угнетения выработки АТФ и других макроэргических соединений, а также синтеза или инактивации простагландинов, гистамина, брадикинина и провоспалительных факторов.
В отличие от большинства НПВП, противовоспалительное действие бензидамина связано не только с блокадой циклооксигеназного пути метаболизма арахидоновой кислоты, но и со снижением ее высвобождения из фосфолипидов на уровне фосфолипазы А2. Бензидамина гидрохлориду присуще стабилизирующее действие на клеточные мембраны нейтрофилов, тучных клеток, эритроцитов и тромбоцитов. Кроме того, Тантум Верде® способствует улучшению микроциркуляции в очаге воспаления, вследствие этого оказывает противозастойное действие и уменьшает экссудацию. Препарат также улучшает процессы эпителизации слизистых ротоглотки [19].
/72-79/76-1.jpg)
/72-79/76-2.jpg)
Бензидамина гидрохлорид блокирует взаимодействие брадикинина с тканевыми рецепторами, вследствие чего способствует снижению болевой чувствительности в очаге воспаления. Местное анестезирующее действие препарата связано со структурным сходством молекулы бензидамина и местных анестетиков, что и обусловливает стабилизацию сенсорных рецепторов, снижение концентрации биогенных аминов, имеющих алгогенные свойства [20, 21]. Недавно получены данные и о воздействии бензидамина гидрохлорида на таламические центры болевой чувствительности (локальная блокада синтеза простагландинов E1, E2 и F2a).
Кроме того, препарат не раздражает слизистые полости рта и желудочно-кишечного тракта и практически не абсорбируется в кровь и в здоровые ткани, т.е. токсический эффект даже при его передозировке отсутствует. Тантум Верде® неаллергенен — по крайней мере мы не обнаружили в литературе никаких сведений об аллергических реакциях.
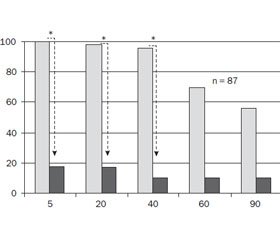
Эффективность Тантум Верде® изучалась во многих лабораториях мира (Blackwell и соавторы, 1975; Centini и соавторы, 1983; Cioli и соавторы, 1985; Cushman и Cheung, 1976; Moncada и соавторы, 1976; Serge и Hammarstrom, 1985). 0,15% водный раствор бензидамина при лечении различных воспалительных процессов ротовой полости и горла широко используется с начала шестидесятых годов прошлого столетия. Его высокая эффективность, противовоспалительный и анальгезирующий эффект подтверждены при лечении тонзиллофарингита у детей еще 40 лет назад [25]. По сравнению с плацебо бензидамин способствует более значимому уменьшению боли с более быстрым снижением ее интенсивности уже на 2-й день терапии [26]. Пациенты с острым фарингитом и тонзиллитом при использовании раствора Тантум Верде® (15 мл каждые 1,5–3 часа в течение 7 дней) ощущают быстрое, начиная со 2-го дня терапии, уменьшение болевых ощущений, чувства жжения и улучшение общего самочувствия. В ходе клинических испытаний, проведенных на 87 здоровых добровольцах, при местном применении Тантум Верде® было установлено, что уже в течение 60 секунд после обработки препаратом слизистых определяется значимый обезболивающий эффект, намного превосходящий результаты в группе контроля (цетилпиридиния гидрохлорид 0,025%) и группе плацебо и длящийся более 90 минут. Авторы приходят к выводу об эффективности Тантум Верде® в купировании болевых ощущений со стороны полости рта и горла [27].
/72-79/77-1.jpg)
/72-79/77-2.jpg)
Быстрое местное болеутоляющее действие Тантум Верде®, наступающее в течение 15 секунд и длящееся до 30–40 минут, выявлено в крупном многоцентровом двойном слепом рандомизированном исследовании, результаты которого также показали, что при лечении 0,15% раствором бензидамина (раствор для полоскания рта Тантум Верде®) ускоряется заживление язв и уменьшается их количество. Положительная динамика симптомов наблюдалась у 84 пациентов, больных мукозитом (язвенное поражение слизистых полости рта у больных со злокачественными новообразованиями и получающих химио- и радиотерапию), получавших бензидамин, в отличие от состояния 88 больных, у которых использовали плацебо. Слизистую оболочку рта обрабатывали в течение 2 минут 4–8 раз в день до лучевой терапии, во время ее проведения и в течение 2 недель после ее завершения. Исследование также показало снижение потребности в анальгетиках у пациентов, которые лечились бензидамином, по сравнению с пациентами, принимавшими плацебо [28]. Начиная с 1-го дня лечения поражений слизистых полости рта на фоне лучевой терапии с использованием Тантум Верде® наблюдается уменьшение гиперемии и отека глотки, а также гипертрофии лимфатических узлов [29].
V. Chudoba (1983) представил данные о безопасности и эффективности Тантум Верде® в лечении пациентов с хроническим тонзиллитом, перенесших тонзиллэктомию, объясняя это ингибированием синтеза ФНО-α и ИЛ-1β. Подобным образом в работе Cingi и соавторов (2011) изучали влияние спреев для горла, содержащих бензидамина гидро–хлорид и хлоргексидина глюконат, в сочетании с антибиотикотерапией у 147 пациентов с тонзиллофарингитом, вызванным стрептококком группы А. Отмечено значимое и статистически достоверное снижение выраженности клинических симптомов в исследуемой группе больных по сравнению с пациентами, не получавшими бензидамина гидрохлорид. Авторы пришли к выводу, что добавление к терапии антибиотиками спрея, содержащего бензидамина гидрохлорид, позволяет существенно снизить выраженность клинических симптомов у пациентов со стрептококковым фарингитом. Идентичные данные получены и у детей [30].
Высокий противовоспалительный и анальгезирующий эффект при лечении воспалительных заболеваний ротовой полости и горла Тантум Верде® получен в работе R.S. Turnbul как у детей, так и у взрослых пациентов [31]. Применение Тантум Верде® при афтозных стоматитах и язвах, наблюдаемых почти у 20 % человеческой популяции, особенно герпетической этиологии, способствует двукратному ускорению стихания болевого синдрома [32]. Никаких серьезных побочных эффектов при применении бензидамина у 7618 пациентов с заболеваниями орофарингеальной зоны не наблюдалось [33].
Тантум Верде® в виде спрея или раствора для полоскания полости рта широко применяется для снижения тяжести и интенсивности боли после интубации как до, так и после оперативного вмешательства [34].
Тантум Верде® представлен несколькими лекарственными формами: таблетки для рассасывания, раствор для местного применения, аэрозоль для местного применения. Тантум Верде® в виде спрея — 1 доза (одно распыление) — 0,255 мкг бензидамина гидрохлорида.
Дозирование. Детям в возрасте 4–6 лет: 1 распыление на каждые 4 кг массы тела, до максимальной дозы, эквивалентной 4 распылениям 2–6 раз в сутки; детям в возрасте 6–12 лет — 4 распыления 2–6 раз в сутки. Взрослым: 4–8 распылений 2–6 раз в сутки.
Тантум Верде® в виде раствора для местного применения: взрослым и детям старше 12 лет назначают по 15 мл для полоскания рта и горла каждые 2–3 часа.
Показаниями к применению препарата Тантум Верде® являются: инфекционно-воспалительные заболевания полости рта и глотки — фарингит, тонзиллит, фаринготонзиллит, ангина, глоссит, гингивит, стоматит различной этиологии, постлучевой эпителиит, кандидоз полости рта (в составе комплексной терапии); в послеоперационном периоде на полости рта и глотки — тонзиллэктомии, аденотомии, крио- и лазерной хирургии новообразований ротоглотки; после травм и оперативных вмешательств на небе, полости рта, нижней челюсти.
Таким образом, Тантум Верде®, являясь нестероидным противовоспалительным средством из группы индазолов, при местном применении в лор-практике и в стоматологии, с одной стороны, уменьшает воспалительные процессы, отечность пораженных тканей, с другой — способствует купированию болевого синдрома. Высокий противовоспалительный, анальгезирующий, антибактериальный и противовирусный эффект получен при лечении воспалительных заболеваний ротовой полости и горла: фарингита, гингивита, глоссита, стоматита, ларингита, тонзиллита, афтозных язв как у детей, так и у взрослых пациентов. Более того, раннее назначение противовоспалительного препарата бензидамина гидрохлорида обеспечивает рациональный контроль над симптомами воспаления, способствует быстрому уменьшению клинических проявлений респираторной инфекции, снижает вероятность развития осложнений.
Список литературы
1. Delayed antibiotic prescribing strategies for respiratory tract infections in primary care pragmatic, factorial, randomized controlled trial // BMJ. — 2014. — 348.
2. Shulman S.T., Bisno A.L., Clegg H.W., Gerber M.A., Kaplan E.L., Lee G., Martin J.M., van Beneden C. Clinical Practice Guideline for the Diagnosis and Management of Group A Streptococcal Pharyngitis: 2012 Update by the Infectious Diseases Society of America // Clin. Infect. Dis. Adv. — 2012.
3. Hsieh T.H., Chen P.Y., Huang F.L., Wang J.D., Wang L.C., Lin H.K., Lin H.C., Hsieh H.Y., Yu M.K., Chang C.F., Chuang T.Y., Lee C.Y. Are empiric antibiotics for acute exudative tonsillitis needed in children? // J. Microbiol. Immunol. Infect. — 2011. — Vol. 44 (5). — Р. 328-332.
4. Shulman et al. IDSA Guideline for GAS Pharyngitis, Clinical Practice Guideline for the Diagnosis and Management of Group A Streptococcal Pharyngitis: 2012 Update by the Infectious Diseases Society of America // Clinical Infectious Diseases. — 2012. — Vol. 3. — Р. 1-17.
5. McIsaac W.J., Kellner J.D., Aufricht P., Vanjaka A., Low D.E. Empirical validation of guidelines for the management of pha–ryngitis in children and adults // JAMA. — 2004. — 291. — 1587-1595.
6. Regoli M., Chiappini E., Bonsignori F., Galli L., de Martino M. Update on the management of acute pharyngitis in children Regoli et al. // Italian Journal of Pediatrics. — 2011. — Vol. 37. — Р. 10.
7. Little P., Stuart B., Hobbs F.D., Butler C.C., Hay A.D., De–laney B., Campbell J., Broomfield S., Barratt P., Hood K., Everitt H., Mullee M., Williamson I., Mant D., Moore M. Antibiotic prescription strategies for acute sore throat: a prospective observational cohort study // Lancet Infect Dis. — 2014. — Vol. 14, № 3. — P. 213-219.
8. Centers for Disease Control and Prevention. CDC twenty four seven. Saving Lives, Protecting People, 2016.
9. WHO Global Strategy for Containment of Antimicrobial Resistance, 2001.
10. Spurling G.K.P., Del Mar C.B., Dooley l. et al. Delayed antibiotics for respiratory infections // Cochrane Database of Systematic Reviews. — 2013. — Issue 4: CD004417. DOI: 10.1002/14651858. CD004417.pub4
11. Guideline for the Diagnosis and Management of Acute Pha–ryngitis. Toward Optimized Practice. Guideline Alberta Clinical Practice. Administered by the Alberta Medical Association. Toward Optimized Practice, Guidelines Alberta clinical practice, Canada, 2008.
12. Chiappini E., Principi N., Mansi N., Serra A., de Masi S., Camaioni A., Esposito S., Felisati G., Galli L., Landi M., Speciale A.M., Bonsignori F., Marchisio P., de Martimo M. Management of acute pharyngitis in children: summary of the Italian Institute of Health guidelines // Clin. Ther. — 2012. — 34 (6). — 1442-1458.
13. Pelluchi C., Grigoryan L., Galeone C., Esposito S., Huovi–nen P., Little P. and Verheij T. Guideline for the Management of Acute Sore Throat. ESMID Sore Throat Guideline Group // Clinical Microbiology and Infection. — 2012. — Vol. 18, Suppl. 1.
14. Stanford T. Shulman, Alan L. Bisno, Herbert W. Clegg, Michael A. Gerber, Edward L. Kaplan, Grace Lee, Judith M. Martin and Chris Van Beneden. Clinical Practice Guideline for Diagnosis and Management of Group A Streptococcal Pharyngitis: 2012 Update by the Infectious Diseases Society of America // Clinical Infectious Di–seases Advance Access. — Published 2012.
15. Little P., Stuart B., Hobbs R. Antibiotic strategies for acute sore throat: a prospective observational cohort study // The Lancet Infectious Diseases, Early Online Publication. — 2014; doi: 10.1016/S1473-3099 (13)70294-9.
16. Bjarnason I., Hayllar J., Macpherson A.J., Russele A.S. // Gastroenterology. — 1993. — V. L04. — Р. l832-1847.
17. Sironi M. Inhibition of inflammatory cytokine production and protection against endotoxin toxicity by benzydamine / M. Sironi, P. Pozzi, N. Polentarutti [et al.] // Cytokine. — 1996. — Vol. 8 (9). — P. 710-716.
18. Schachtel B.P., Padjarino D.A. A Randomized, Double-Blind, Placebo-Controlled Model Demonstrating the Topical Effect of Benzydamine in Children with Sore Throat // Clin. Pharmacol. Ther. — 1996. — 59. — 145.
19. Тарасова Г.Д. Тантум Верде в комплексном лечении хронического тонзиллита / Г.Д. Тарасова // Мат-лы юбилейной Всероссийской науч.-практ. конф. «Современные аспекты и перспективы развития оториноларингологии». — М., 2005. — С. 26.
20. Nash D.R., Harman J., Wald E.R., Kelleher K.J. Antibiotic prescribing by primary care physicians for children with upper respiratory tract infections // Arch. Pediatr. Adolesc. Med. — 2002. — Vol. 156, № 11. — P. 1114-1119.
21. Mangano G. et al. Benzydamine Local Anestetic Activity And [3h]-Batrachotoxin Binding Sites. — Italian Society of Pharmacology, 2003.
22. Морозова С.В., Митюк А.М. Принципы дифференциальной диагностики и топической терапии острых воспалительных заболеваний глотки // РМЖ. — 2011. — № 8. — С. 525-530.
23. Prats G. Study of Benzydaminein-vitro Activity against diffe–rent bacterial strains of clinical interest — Servicio de Microbiologia, Hospital de Sant Pau, Barcelona, Spain, 2001.
24. Старостина С.В. Боль в горле: эффективность топической терапии // РМЖ. — 2014. — № 9. — С. 666-670.
25. Froom J. et al. Benzydamine oral rinse for sore throat // Curr. Ther. Res. — 1979. — 26. — 856-61.
26. Kazdan N. Benzydamine HCL oral rinse and gargle in the treatment of acute pharyngitis // Inter. Canada Pharmaceuticals. — 1977.
27. Matthews R. et al. Clinical evaluation of benzydamine, chlorhexidine, and placebo mouthwashes in the management of recurrent aphthous stomatitis // Oral. Surg. Oral. Med. Oral. Pathol. — 1987. — 63 (2). — 189-91.
28. Kim J. BenzydamineHCl, a new agent for the treatment of radiation mucositis of the oropharynx // Am. J. Clin. Oncol. — 1986. — 9 (2). — 132-4.
29. Rubenstein E.B., Peterson D.E., Schubert M., Keefe D., –McGuire D., Epstein J. et al. Clinical practice guidelines for the prevention and treatment of cancer therapy-induced oral and gastrointestinal mucositis // Cancer. — 2004. — 100 (Suppl. 9). — 2026-46.
30. Крюков А.И., Туровский А.Б. Симптоматическая терапия при некоторых заболеваниях лор-органов // Справочник поликлинического врача. — 2005. — Т. 4, № 4. — С. 24-28.
31. Turnbul R.S. Benzydamine Hydrochloride (Tantum) in the management of oral inflammatory conditions // Journal Can Den Assoc. — 1995. — 61 (2). — 127-34.
32. Yankell S. Evaluation of Benzydamine HCL in patients with aphthous Ulcers // Compend Contin. Educ. Dent. — 1981. — 2 (1). — 14-6.
33. Engles I. Vertraglichkeits studiemit Tantum Verde gurrgellosung // Med. Welt. — 1980.
34. Kati I., Tekin M., Silay E., Huseyinoglu U.A., Yildiz H. Does benzydamine hydrochloride applied preemptively reduce sore throat due to laryngeal mask airway? // Anesth. Analg. — 2004. — 99 (3). — 710-21.

/72-79/72-1.jpg)
/72-79/73-1.jpg)
/72-79/73-2.jpg)
/72-79/73-3.jpg)
/72-79/74-1.jpg)
/72-79/74-2.jpg)
/72-79/74-3.jpg)
/72-79/75-1.jpg)
/72-79/76-1.jpg)
/72-79/76-2.jpg)
/72-79/77-1.jpg)
/72-79/77-2.jpg)
/72-79/78-1.jpg)