Статья опубликована на с. 59-66
Болезнь Лайма представляет собой инфекционное заболевание, распространенное на определенных территориях, где обитает микроорганизм, являющийся его возбудителем. Заболевание имеет множество названий: системный клещевой боррелиоз, клещевой боррелиоз, Лайм-боррелиоз, иксодовый боррелиоз, эритемный спирохетоз, клещевой менингополиневрит и т.д. Однако согласно Международной статистической классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра, принятой 43-й Всемирной ассамблеей здравоохранения, заболевание кодируется шифром А69.2 с названием «болезнь Лайма» (Lyme disease).
Заболевание получило название «болезнь Лайма» по наименованию города Лайма в штате Коннектикут, в котором в 1975 году была впервые зарегистрирована вспышка инфекции и описаны ее основные симптомы. Все остальные названия данной инфекции являются производными либо от названия возбудителя (боррелиозы), либо от ведущих клинических признаков (клещевой менингополиневрит, мигрирующая эритема), либо от наименования клещей-переносчиков спирохет (иксодовый или клещевой боррелиоз и др.).
Болезнь Лайма была открыта после обследования подростков штата Коннектикут, у которых ювенильный артрит встречался в 100 раз чаще, чем у их сверстников из других местностей США. Врачи и ученые заинтересовались подобной аномалией, взяли пробы синовиальной жидкости из суставов больных и смогли высеять спирохету Borrelia burgdorferi, которая оказалась возбудителем заболевания.
Боррелиоз распространен повсеместно, кроме Антарктиды, но преобладает в странах Северного полушария, особенно в США, Канаде, Китае, Японии, России, Литве, Латвии, Эстонии и странах Западной Европы [1, 2]. Инфекция распространена на тех территориях, где находится ее природный резервуар, который постоянен и не перемещается с течением времени. В эндемичных зонах Америки и Европы заболеваемость достигает 300–500 случаев на 100 тыс. населения, в Германии, Австрии, Словакии — 100 случаев на 100 тыс. населения. С момента начала официальной регистрации болезни Лайма в Украине отмечается ежегодное увеличение заболеваемости на 5–30 %. Но в 2015 году этот показатель увеличился в 2,02 раза и составил 3413 случаев (7,96 на 100 тыс. населения) против 1686 случаев (3,72 на 100 тыс. населения) в 2014 году. Уровень заболеваемости в Киеве традиционно наивысший по Украине и в 2015 году составил 27,1 на 100 тыс. населения (рис. 1).
/60.jpg)
В настоящее время известно около 20 геновидов боррелий, относящихся к комплексу B.burgdorferi sensu lato. Доказана патогенность для человека 4 геновидов: B.burgdorferi sensu stricto, B.garinii, B.afzelii и B.miyamatoi. В Европе болезнь Лайма вызывают B.afzelii (до 80 % случаев заболевания) и B.garinii (до 15 % случаев заболевания) [2–7]. В Северной Америке боррелиоз вызывается только В.burgdorferi sensu stricto. У отдельных представителей боррелий геном различается примерно на 10 %, что обусловливает то, какие органы (нервная система, суставы, кожа или сердце) будут поражаться у больного. Мигрирующая эритема наблюдается наиболее часто при инфицировании В.аfzelii, B.garinii обусловливает преимущественно поражение нервной системы, а В.burgdorferi sensu stricto — поражение опорно-двигательного аппарата [2].
Инфекция трансмиссивная, поскольку заражение происходит только при укусе иксодовых клещей, которые являются переносчиками боррелий. Переносчиками боррелиоза в европейских странах являются иксодовые клещи видов Ixodes ricinus и Ixodes persulcatus, на территории североамериканского континента (США и Канада) — вида Ixodes dammini. В Украине переносчиками боррелий являются лесной клещ (Ixodes ricinus) и луговой клещ (D.reticulatus). Сами клещи заражаются боррелиями после укусов ими домашних или диких животных, которые являются хозяевами данных микроорганизмов (около 130 видов мелких млекопитающих и 100 видов птиц) [1, 2]. Когда клещ укусит такое животное, в его организм попадают боррелии, и насекомое становится их пожизненным носителем. Более того, самки клещей передают боррелии своим личинкам, из которых формируются взрослые клещи и которые буквально с момента рождения являются переносчиками инфекции. В природных очагах зараженность клещей может варьировать от 5–10 до 70–90 % [1–3]. В некоторых странах с природными очагами боррелиоза, где зараженность клещей может достигать 90 %, практически каждый укус клеща может вызвать заражение боррелиозом. В Украине, по данным санитарно-эпидемиологической службы, инфицированность клещей колеблется от 12,5 до 18,6 %. Период активности клещей, в течение которого они могут кусать человека, длится с мая по сентябрь, пока на деревьях и кустарниках имеется листва, а на земле — трава. Именно в этот период клещи становятся активными, могут запрыгивать с травы и листвы кустарников на одежду человека, с которой перебираются на кожу и присасываются. В зонах обитания клещей I.ricinus случаи заболеваний могут регистрироваться и осенью (в сентябре-октябре), что связано с наличием дополнительного периода активности этих клещей в конце лета. Прикрепление и присасывание клеща к телу человека в большинстве случаев остаются незамеченными, так как в состав его слюны входят анестезирующие, сосудорасширяющие и антикоагулирующие вещества. После присасывания клещ впрыскивает в кровоток слюну вместе с боррелиями, в результате чего человек заражается инфекцией.
Описаны случаи механической передачи возбудителей при случайном раздавливании клещей во время их снятия с животных (например, собак) и попадания содержимого кишечника клеща в микротравмы кожи или на конъюнктиву глаз. Другим возможным путем передачи боррелий от животных к человеку может быть алиментарный путь, реализующийся при употреблении в пищу сырого козьего молока или молочных продуктов без термической обработки [2].
От человека к человеку боррелиоз не передается, поэтому больной совершенно безопасен для окружающих. Боррелиозом могут заболевать люди любого пола и возраста, в том числе и маленькие дети.
Из места укуса боррелии попадают в лимфу и кровь, с током которых разносятся в различные внутренние органы, нервные волокна, лимфатические узлы и суставы. После попадания в нервные волокна боррелии могут передвигаться по ним и попадать в спинной и головной мозг, вызывая в них воспалительные процессы. В процессе распространения по организму часть боррелий погибает, выделяя эндотоксин, который вызывает активацию целого каскада реакций иммунной системы. В результате этих реакций происходит образование циркулирующих иммунных комплексов, которые повреждают ткани суставов, почек, кожи, подкожного жирового слоя, селезенки, головного мозга и нервных ганглиев, формируя в них воспалительные инфильтраты. Живые боррелии выделяют липополисахариды, стимулирующие выработку интерлейкина‑1, который активизирует воспалительный процесс в суставах, что, соответственно, приводит к артриту, разрушению костей и хрящей, а также паннусу (воспаление роговицы глаза).
Поскольку боррелии могут жить внутри клеток, то даже после выздоровления человека бактерии могут сохраняться в его организме в течение длительного времени — до 10 лет [1]. Наиболее вероятно, что боррелии сохраняются в лимфатической системе.
Инкубационный период болезни Лайма обычно длится от 2 до 50 дней, но в редких случаях может продолжаться в течение нескольких месяцев или даже лет. Боррелиоз протекает стадийно, с поражением суставов, нервной системы и сердца и подвергается полному излечению, если начать терапию антибиотиками в течение короткого срока после начала заболевания.
На первой стадии (острой) у человека появляются симптомы интоксикации (повышенная температура тела, головные и мышечные боли, слабость, сонливость и т.д.) и мигрирующая эритема. Примерно в 7–30 % случаев первая стадия боррелиоза протекает бессимптомно, и в этом случае выявить заболевание можно только при помощи лабораторных анализов крови. Эритема образуется в месте укуса клеща и представляет собой постоянно увеличивающееся в диаметре пятно с ярко-красным наружным ободком и светлой внутренней частью. Помимо эритемы, на коже может быть сыпь в виде крапивницы, а также точечные и кольцевидные высыпания. У 5–8 % людей на первой стадии боррелиоза появляются признаки поражения головного мозга: головная боль, тошнота, рвота, светобоязнь, гиперестезия, менингеальные знаки. В очень редких случаях первый этап боррелиоза проявляется безжелтушным гепатитом со следующими симптомами: потеря аппетита, тошнота, рвота, боли в правом подреберье, повышение активности аспартатаминотрансферазы, аланинаминотрансферазы (АЛТ) и лактатдегидрогеназы в крови. Первая стадия боррелиоза развивается через несколько дней или недель после укуса клеща и заражения спирохетами и длится до 1 месяца. После завершения первой, острой стадии боррелиоза либо наступает выздоровление, либо инфекция переходит в хроническое течение и развиваются 2-я и 3-я стадии. Вероятность полного выздоровления при начале адекватной антибиотикотерапии на первой стадии составляет 80 %.
Вторая стадия болезни Лайма развивается через несколько недель или месяцев после инфицирования человека или в конце 1–3-го месяца после появления первых клинических симптомов инфекции (эритемы и интоксикации). Чаще наблюдается поражение нервной системы и/или сердца. В результате поражения нервной системы развиваются серозный менингит, периферические нейропатии (онемение конечностей, потеря чувствительности на отдельных участках рук и ног и т.д.), радикулиты и др. Отличительной чертой болезни Лайма является сочетание менингита с парезами черепных нервов и радикулопатией. Этот наиболее часто встречающийся симптомокомплекс неврологических нарушений называется лимфоцитарным менингорадикулоневритом Банноварта. Если в этой стадии не начать лечение антибиотиками, то боррелиозный менингорадикулоневрит может продолжаться до нескольких месяцев. В очень редких случаях боррелиоз проявляется менингоэнцефалитом с преобладанием воспаления оболочек мозга.
Поражение сердца проявляется по типу преходящих нарушений проводимости (преимущественно в виде атриовентрикулярной блокады), перикардита или миокардита. При этом отмечаются сердцебиение, одышка, боли в груди сжимающего характера, на электрокардиограмме фиксируется удлинение интервала PQ. Кардиальные (сердечные) симптомы обычно продолжаются 2–3 недели.
Реже на второй стадии боррелиоза может развиваться поражение кожи, протекающее по типу капилляритов, сыпей или одиночной доброкачественной лимфоцитомы. Эритема и доброкачественная лимфоцитома кожи являются наиболее специфическими симптомами боррелиоза. Внешне такая лимфоцитома выглядит как единичный выпуклый узелок на коже, окрашенный в ярко-малиновый цвет и слегка болезненный при ощупывании. Лимфоцитомы могут локализоваться на лице, половых органах и в паховой области.
Также на второй стадии могут встречаться поражения опорно-двигательного аппарата в виде артритов крупных суставов. Вторая стадия инфекции может длиться до полугода.
Третья стадия боррелиоза начинается через 0,5–2 года после появления первых клинических симптомов инфекции (или через 3–6 месяцев после завершения 1-й и 2-й стадий) и продолжается в течение многих лет. Переход инфекции в третью стадию означает хронизацию патологического процесса в органах и развитие хронического боррелиоза. Для третьей стадии характерно развитие хронических артритов, атрофического акродерматита и хронических неврологических синдромов.
Поражение суставов на третьей стадии боррелиоза может протекать в трех формах: мигрирующие артралгии, доброкачественный рецидивирующий артрит, хронический прогрессирующий артрит.
Мигрирующие артралгии фиксируются в 20–50 % случаев и практически всегда сочетаются с болями в мышцах. Наиболее сильные боли часто развиваются в мышцах шеи. Боли в суставах продолжаются несколько дней подряд, сочетаются со слабостью, утомляемостью и головной болью, после чего внезапно и самостоятельно проходят.
При развитии доброкачественного рецидивирующего артрита, как правило, поражаются коленные или другие крупные суставы. В патологический процесс вовлекаются один или максимум 3 сустава. Артрит протекает с чередованием рецидивов и ремиссий. Рецидивы длятся 1–2 недели, ремиссии продолжаются от нескольких недель до месяцев. Причем с течением заболевания частота рецидивов уменьшается, а длительность ремиссий увеличивается. В течение 4–5 лет рецидивы полностью сходят на нет, и артрит перестает беспокоить человека, благодаря чему его считают доброкачественным.
Хронический прогрессирующий артрит поражает сразу несколько суставов (больше трех) и протекает в виде постоянного воспалительного процесса. При таком артрите человека беспокоят боли, отечность, плохая подвижность и ограниченность движений в пораженных суставах, а также эрозия хрящей и костей. Очень часто в патологический процесс вовлекаются ткани, окружающие сустав, в результате чего артрит осложняется бурситами, лигаментитами, энтезопатиями, остеопорозом, истончением хряща, а также остеофитозом (наслоение на кость рыхлой воспалительной массы). Иногда хронический боррелиозный артрит сочетается с паннусом (воспалением роговицы глаза).
Помимо поражения суставов, в третьем периоде болезни Лайма развивается патологический процесс в коже, протекающий по типу атрофического акродерматита или очаговой склеродермии. Атрофический акродерматит начинается с появления красно-синих пятен на разгибательных поверхностях, таких как колени, локти, тыльная часть кистей и подошвы. В области пятен может образовываться плотный воспалительный инфильтрат, отек и нарушение оттока лимфы на пораженном участке. Данная воспалительная фаза продолжается годами и медленно переходит в склеротическую, при которой кожа атрофируется и становится похожей на мятую тонкую бумагу. В третьей стадии болезни Лайма атрофический акродерматит в 30 % случаев сочетается с поражением суставов, а в 45–50 % — с поздними неврологическими осложнениями.
Наиболее характерными поздними неврологическими осложнениями этой стадии являются хронический энцефаломиелит, спастический парапарез, хроническая аксональная полирадикулопатия, потеря памяти, слабоумие. Хронический энцефаломиелит характеризуется постоянными головными болями, усталостью, головокружением, тошнотой, периодически возникающей рвотой, судорогами, галлюцинациями, а также нарушением памяти, внимания, речи, координации движений, чувствительности и т.д. Спастический парапарез характеризуется повышением мышечного тонуса различных частей тела с развитием неконтролируемых патологических рефлексов и движений. При хронической аксональной полирадикулопатии отмечается слабость мышц в нижних частях конечностей (кисти, стопы). При выраженной слабости мышц ног развивается степпаж — «петушиная» походка. Наблюдается снижение или полное выпадение сухожильных рефлексов, нарушение чувствительности в дистальных отделах рук и ног по типу «носков» и «перчаток». Нарушение чувствительности проявляется в ощущении бегания мурашек, жжении, покалывании, потери способности чувствовать температуру, вибрацию, прикосновения и т.д. Характерна сухость кожных покровов, нарушение работы кровеносных сосудов, вследствие чего у человека появляются приступы сердцебиения, гипотензии и т.д. Хронический боррелиоз развивается, если инфекция не лечилась или прибегали к неэффективной терапии.
Болезнь Лайма у детей чаще наблюдается в возрасте старше 7 лет. Малыши дошкольного возраста очень редко заболевают боррелиозом, даже если их укусил инфицированный клещ-переносчик. Течение заболевания и клинические признаки у детей точно такие же, как и у взрослых. Однако для детей в основном характерно развитие менингита как проявления поражения нервной системы, в то время как у взрослых чаще формируются периферические нейропатии (парезы нервов, радикулиты и т.д.). После выздоровления у детей могут оставаться астеновегетативные реакции, такие как неустойчивость настроения, повышенная возбудимость и расстройства сна. Данные реакции через некоторое время полностью проходят.
Для подтверждения диагноза боррелиоза исследуют кровь на наличие боррелий и антител к ним при помощи следующих анализов: реакция непрямой иммунофлуоресценции (РНИФ), иммуноферментный анализ (ИФА), полимеразная цепная реакция (ПЦР), иммуноблоттинг. Метод микроскопии используют для установления инфицированности клещей. Однако этот метод не позволяет установить патогенность боррелий. Перспективность использования метода ПЦР заключается в возможности определять наличие ДНК боррелий в различных биологических материалах: клещ, кожный биоптат, кровь, моча, цереброспинальная и суставная жидкости и др. Однако метод ПЦР для диагностики боррелиоза в настоящее время не унифицирован и не стандартизирован [2]. Относительно низкая чувствительность этого метода при боррелиозной инфекции не позволяет определять инфицированность пациента на ранних сроках (7–10 дней) от момента присасывания клеща и подтвердить диагноз. Кроме этого, генетическая разнородность патогенных боррелий в Европейском регионе также ограничивает диагностические возможности этого метода.
Наиболее простыми, доступными и достаточно эффективными анализами для подтверждения болезни Лайма являются ИФА и РНИФ. Сейчас в Украине используются тест-системы для одномоментного выявления антител к 3 видам патогенных боррелий: B.burgdorferi sensu stricto, B.garinii, B.аfzelii. Антитела к боррелиям класса IgM появляются в крови через 2–6 недель после инфицирования и сохраняются до нескольких лет. Соответственно, анализы, проведенные сразу после укуса клеща, неинформативны. Следует учитывать данные литературы, согласно которым до 60 % больных с клиническими проявлениями болезни Лайма в первом периоде заболевания имеют титры антител ниже референтных [5]. Антитела класса IgG появляются через 4–6 недель после инфицирования и определяются в крови в течение нескольких лет даже после полного излечения инфекции на первой стадии. Поэтому определение концентрации специфических IgG один раз неинформативно. Для выявления динамики заболевания необходимо определить концентрацию антител класса IgG к боррелиям дважды с интервалом в 4–6 недель. Снижение титра антител указывает на выздоровление пациента.
В настоящее время золотым стандартом диагностики Лайм-боррелиоза в мире является двухэтапная серодиагностика: 1-й этап — выявление антител методом ИФА или РНИФ; 2-й этап — иммуноблотт с определением антител к конкретным антигенам боррелий [2–5]. При получении отрицательных результатов на 1-м этапе исследование с использованием метода ИФА повторяют через 2–4 недели. При проведении иммуноблотта диагностическим является обнаружение по меньшей мере 3 специфических белков для IgM или 5 специфических белков для IgG [6, 7].
Лечение боррелиоза заключается в приеме антибиотиков, к которым чувствительны боррелии. При этом длительность и схема их применения различны для лечения болезни Лайма на разных стадиях и для разных клинических проявлений. Для лечения боррелиоза на первой стадии применяют антибиотики тетрациклинового ряда, цефалоспорины II–III поколений и полусинтетические пенициллины в течение 10–21 дня. Однако следует учитывать, что у детей диссеминация возбудителя из места первичного аффекта во внутренние органы и нервную систему наблюдается значительно быстрее, чем у взрослых, и может происходить уже на 7–10-й день болезни [2]. В связи с этим в качестве стартовой терапии у детей отдают предпочтение инъекционным формам антибиотиков, обеспечивающим быструю и достаточную концентрацию препарата во всех органах и системах. Наши наблюдения подтверждают эти данные.
При оценке профиля риска/пользы группа экспертов Международного общества болезни Лайма и ассоциированных заболеваний (ILADS) установила недопустимо высокую частоту неэффективности лечения мигрирующей эритемы при проведении антибактериальной терапии в течение 20 и менее дней и чрезмерно высокий показатель потенциального вреда. Поэтому следует рекомендовать пациентам выдерживать трехнедельный курс терапии даже при быстром исчезновении клинических проявлений [8].
При тяжелых форма боррелиоза, а также при наличии признаков поражения нервной системы, сердца и суставов у пациентов всех возрастных групп препаратом выбора является цефтриаксон, который назначается на 14–21-й день.
В случае аллергической реакции на пенициллины и цефалоспорины могут быть использованы хлорамфеникол, тетрациклины или макролиды.
При артритах, а также хроническом атрофическом акродерматите вышеперечисленные антибиотики применяют в течение 30 дней.
В течение первых 24 часов лечения антибиотиками у 5–25 % больных может наблюдаться реакция Яриша — Герксгеймера, которая проявляется усилением интоксикации, появлением новых высыпаний или усугублением кожных проявлений в области эритемы. Появление этой реакции свидетельствует об успешности проводимого лечения и не требует отмены антибактериальной терапии.
В некоторых случаях бывает недостаточным проведение одного курса антибиотикотерапии. При назначении повторного курса этиотропной терапии смена антибиотика не является обоснованной, так как боррелии не приобретают устойчивости к использованному ранее антибиотику и неудача лечения в большинстве случаев обусловлена либо коротким предыдущим курсом, либо невозможностью создания действенных концентраций антибиотиков в местах персистенции возбудителей [2].
Если боррелиоз был выявлен у беременной женщины, то ей следует принимать амоксициллин по 500 мг 3 раза в сутки в течение 21 дня. Данного курса антибиотикотерапии достаточно для того, чтобы профилактировать передачу инфекции плоду [1].
Специфической профилактики боррелиоза не существует. Поэтому единственно возможной профилактикой инфекции является неспецифическая, заключающаяся в минимизации риска попадания клеща на тело человека. Если человек собирается на природу, то следует одеваться в светлую одежду, максимально закрывающую тело. Кроме того, открытые участки тела следует обрабатывать репеллентами, отпугивающими клещей. Во время нахождения в лесу или парке следует через каждые два часа осматривать тело на наличие клещей.
В случае обнаружения боррелий в клеще и не позднее 5 суток после присасывания клеща всем пациентам проводится химиопрофилактика доксициклином, аминопенициллинами, цефтриаксоном. Согласно рекомендациям ILADS, предпочтительной схемой профилактики болезни Лайма является назначение всем пациентам при установленных случаях укуса иксодовыми клещами с признаками кровососания доксициклина в дозе 100–200 мг 2 раза в день в течение 20 дней [8].
Антибиотикотерапия в ранние сроки инкубационного периода (до 5 суток после присасывания клеща) позволяет практически у всех пациентов оборвать инфекционный процесс, причем эффективность использования разных антибиотиков примерно одинакова и составляет 80–98 % [1–3].
Мы ретроспективно проанализировали истории болезни пациентов, которые проходили лечение по поводу болезни Лайма в Киевской городской детской клинической инфекционной больнице (КГДКИБ) в 2014–2015 гг. С диагнозом «болезнь Лайма» было госпитализировано 12 детей в 2014 году и 22 ребенка в 2015 году, что составляет 31,4 % от общего числа зарегистрированных случаев заболевания в Киеве. От госпитализации отказались 8 пациентов в 2014 году и 11 пациентов в 2015 году. Им была назначена антибактериальная терапия, и повторно в связи с неэффективностью терапии обратился только 1 пациент.
В 2014 году 5 (41,7 %) пациентов поступили в стационар по направлению педиатра: 4 детей — с диагнозом «болезнь Лайма?», 1 ребенок — с диагнозом «острая респираторная инфекция». Остальные 7 (58,3 %) пациентов обратились в стационар самостоятельно после появления эритемы. В 2015 году без направления было госпитализировано 4 (18,2 %) детей, остальные пациенты были направлены в стационар врачами разных специальностей (педиатр, дерматолог, невролог) с диагнозом «болезнь Лайма». Хотелось обратить внимание, что из 5 детей, которые первично после появления эритемы обратились к дерматологам, только в одном случае была заподозрена болезнь Лайма, остальным детям поставили диагноз «аллергический дерматит» и назначено соответствующее лечение. И только после неэффективности такой терапии в течение 1–12 недель эти пациенты попали к нам в стационар.
/63.jpg)
В течение первых 3 дней после появления эритемы к врачам обратились 67,8 % пациентов: в 2014 году — 55,5 % пациентов, в 2015 — 81,0 % пациентов (рис. 2). Но 10,7 % больных обращались к специалистам после 10-го дня с момента появления эритемы (рис. 2). Максимальный период от появления эритемы до обращения к врачу в 2014 году длился 3 месяца, а в 2015 году — 16 дней.
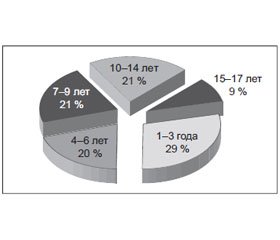
Среди госпитализированных было 6 (17,4 %) мальчиков и 28 (82,6 %) девочек. Половину госпитализированных составили детей первых 6 лет жизни (рис. 3).
Больные поступали в стационар с апреля по октябрь, при этом с апреля по июнь поступило 73,5 % пациентов. Клещей на теле детей выявляли после прогулок в парках Святошинского, Голосеевского, Дарницкого районов г. Киева и в лесах Киевской и Житомирской областей. Данные об укусе клеща отсутствовали у 5 (14,7 %) детей. Профилактическую химиотерапию после укуса клеща никто из детей не получал даже после обращения к специалистам.
Эритема появлялась с 3-го по 30-й день после укуса клеща у 28 (82,4 %) детей, у 2 (5,9 %) пациентов была безэритемная форма и они поступали во второй стадии болезни Лайма, еще у 2 (5,9 %) пациентов была диагностирована латентная форма. При появлении эритемы у 6 (17,6 %) больных отмечались субфебрильная температура и катаральные симптомы, у 2 (5,8 %) детей — артралгии и миалгии. У 30,0 % детей эритема локализовалась на ногах, у 26,7 % — в области головы, у 16,7 % — на груди и у 23,3 % пациентов была мигрирующая сыпь.
На фоне антибактериальной терапии цефтриаксоном эритема исчезала через 5–12 дней (в среднем 6,9 ± 3,5). Один ребенок после появления эритемы в амбулаторных условиях получал доксициклин, но на 16-й день лечения появились боли в коленных суставах, эритема не исчезала, и ребенок был направлен на госпитализацию в ГДКИБ. В стационаре при введении цефтриаксона артралгии исчезли на 2-й день, эритема — на 7-й день.
У 3 (8,8 %) больных на 8–20-й день лечения цефтриаксоном отмечалось повышение уровня АЛТ в 3–10 раз (табл. 1). Показатели АЛТ нормализовались в течение 1–2 недель. Маркеры вирусных гепатитов у этих больных были отрицательными.
Мелкая пятнисто-папулезная сыпь на конечностях и туловище выявлялась у 3 (8,8 %) больных. Сыпь у 1 ребенка появилась сразу после появления эритемы, еще у 2 детей — на 8–11-й день лечения в стационаре. Высыпания исчезли бесследно через 1–3 дня у всех детей.
У двоих членов семьи больного с эритематозной формой болезни Лайма выявили высокие титры IgM к Borrelia burgdorferi в крови при отрицательных IgG к Borrelia burgdorferi. При этом клинические проявления заболевания у них отсутствовали, но были данные об укусах клещами. На основании этих данных был выставлен диагноз «болезнь Лайма, латентное течение». При наблюдении за этими пациентами в течение 1,5 года клинические проявления, характерные для болезни Лайма, не выявлялись.
У одного ребенка с безэритемной формой болезни на 49-й день после укуса клеща развилось сходящееся левостороннее косоглазие, которое уменьшилось на 3-й день и полностью исчезло на 13-й день лечения цефтриаксоном. Еще у одного пациента, который получил только 5-дневный курс азитромицина при появлении эритемы, через 1 месяц после исчезновения эритемы появились диплопия, горизонтальный нистагм, расходящееся косоглазие левого глаза. На фоне приема цефтриаксона перечисленные симптомы исчезли через 6 дней, однако на 10-й день терапии появился легкий тремор рук и языка, который сохранялся 3 дня, повысился уровень АЛТ, который нормализовался через 15 дней. После 4-недельного курса цефтриаксоном клинических проявлений заболевания в течение 1 года наблюдения не выявляли.
Антитела к боррелиям определяли у 26 больных, из них IgM к Borrelia burgdorferi, В.afzelli, В.garinii присутстовали у 19 (73,1 %) пациентов и отсутствовали у 7 (26,9 %) (табл. 2).
У всех больных с безэритемной формой болезни Лайма выявлялись IgM к Borrelia burgdorferi. Среди пациентов с эритемной формой болезни Лайма IgM к боррелиям выявлялись у 15 (68,2 %) детей на 5–20-й день с момента появления эритемы и отсутствовали у 7 (31,8 %) детей на 2–12-й день после появления эритемы. У 3 детей с эритемой одномоментно выявлялись IgМ и IgG к Borrelia burgdorferi, В.afzelli, В.garinii. Из них у ребенка с данными о перенесенной болезни Лайма 4 года назад на 12-й день от момента появления эритемы уровень IgM превышал в 3 раза референтные значения, а уровень IgG — в 11 раз. У одного пациента на 15-й день эритемы уровень IgM к боррелиям превышал референтные значения в 9 раз, а уровень IgG — в 2 раза, еще у одного ребенка на 17-й день эритемы показатели IgM и IgG были одинаково положительными.
При госпитализации в стационар всем больным с болезнью Лайма назначался цефтриаксон. Длительность антибактериальной терапии составляла 21–28 дней. У части больных после исчезновения клинических проявлений цефтриаксон заменяли на пероральные цефалоспорины III поколения или доксициклин (детям старше 8 лет).
Все пациенты были выписаны с полным выздоровлением, повторных обращений в течение 1 года наблюдения не было.
В качестве примера поздней диагностики болезни Лайма приводим следующий клинический случай. Больная О., 11 лет, поступила в стационар 29.01.2014 с диагнозом «болезнь Лайма». В начале ноября девочку стала беспокоить боль в области левого подреберья, затем на этом месте появилась эритема. Осмотрена дерматологом, выставлен диагноз «аллергический дерматит», назначена противоаллергическая мазь. Так как терапия оказалась неэффективной, родители решили самостоятельно обратиться в КГДКИБ. При госпитализации в КГДКИБ 29.01.2014 выявлена кольцевидная эритема размером 45 × 30 см. Данных про укус клеща не было. В крови методом ИФА выявлены IgM к Borrelia burgdorferi — 5,6 ЕД/мл (отрицательные при ≤ 0,8 ЕД/мл), IgG к Borrelia burgdorferi — 0,43 ЕД/мл (отрицательные при ≤ 0,8 ЕД/мл). На фоне приема цефтриаксона эритема исчезла в течение 5 дней. Курс антибактериальной терапии был продлен до 14 дней (цефтриаксон) и 7 дней (доксициклин). Девочка в удовлетворительном состоянии выписана домой. Была проконсультирована неврологом, кардиологом — патологии не выявлено.
Следующий пример клинического случая второй стадии болезни Лайма. Ребенок Г., 13 лет, поступил в КГДКИБ 23.07.2011 с диагнозом «болезнь Лайма». Из данных эпиданамнеза: проживал в США, где 25.06.2011 был укушен клещом в области подколенной ямки. Антибиотикопрофилактика не проводилась. 17.07.2011 приехал в Чехию (г. Прага), где 18.07.2011 почувствовал себя больным. Заболевание началось с повышения температуры тела до 38 °C, ломоты в теле, боли по ходу позвоночника, головной боли. Мать заметила асимметрию лица и кольцевидную эритему диаметром 20–30 см в месте укуса клеща. Был госпитализирован. Проведена люмбальная пункция. В ликворе: белок — 0,52 г/л, реакция Панди +, плеоцитоз — 440 клеток в 1 мкл (55 % — лимфоциты, 38 % — моноциты, 7 % — нейтрофилы). Установлен диагноз «асептический менингоэнцефалит с периферическим парезом VII пары черепных нервов». Проводилась терапия цефтриаксоном, нестероидными противовоспалительными препаратами. 23.07.2011 мальчик с родителями самолетом прилетел в Украину и в этот же день был госпитализирован в КГДКИБ. На основании наличия у ребенка серозного менингита, пареза лицевого нерва и радикулярного синдрома был установлен диагноз лимфоцитарного менингорадикулоневрита Баннварта. В крови методом ИФА выявлены антитела IgM к Borrelia burgdorferi — 43,4 ЕД/мл (отрицательные при ≤ 9,0 ЕД/мл), антитела IgG к Borrelia burgdorferi — 3,39 ЕД/мл (отрицательные при ≤ 0,4 ЕД/мл). Заключительный клинический диагноз: болезнь Лайма, 2-я стадия — лимфоцитарный менингорадикулоневрит Баннварта. Проводимая терапия: цефтриаксон внутривенно (в/в) — 21 день, глюкокортикостероиды (дексазон + преднизолон) в/в начиная с 5 мг/кг/сутки в убывающей дозировке — 21 день, в/в инфузии солевых растворов с целью дезинтоксикации — 3 дня, эриус, милдронат.
Общее состояние мальчика нормализовалось через 3 дня после госпитализации. Радикулярный синдром исчез спустя неделю. Санация ликвора отмечалась через 3 недели от начала лечения. Дольше удерживались проявления неврита лицевого нерва. Выписан из стационара 16.08.2011 с незначительными остаточными проявлениями пареза лицевого нерва под наблюдение невролога.
Таким образом, литературные данные и результаты собственных наблюдений подтверждают тот факт, что в настоящее время болезнь Лайма имеет значительный вес в структуре инфекционной патологии. Большинство наблюдавшихся больных (82,3 %) поступают в стационар с ранними специфическими проявлениями болезни в виде мигрирующей эритемы, что позволяет поставить диагноз клинически. Однократная серологическая диагностика болезни Лайма методом ИФА, в связи с поздним появлением антител, обладает недостаточной информативностью, и при наличии специфической эритемы нет необходимости в проведении этого исследования. В связи с отсутствием мер специфической профилактики болезни Лайма необходимо как можно раньше диагностировать болезнь, а своевременная адекватная терапия полными курсами антибактериальных препаратов позволяет предупредить хронизацию болезни, развитие рецидивов и избежать поздних осложнений. Личная профилактика заключается в предупреждении присасывания клещей, а в случае укуса клеща необходимо своевременное обращение за медицинской помощью. Учитывая постоянный рост заболеваемости, особенно в 2015 году, необходимо активизировать санитарно-просветительную работу среди населения и врачей различных специальностей (педиатры, дерматологи, хирурги), разработать оптимальные схемы химиопрофилактики заболевания.
/60.jpg)
/63.jpg)
/64_2.jpg)
/64.jpg)

/65.jpg)