Статтю опубліковано на с. 53-58
Герпетичні інфекції (ГІ) належать до числа одних із найпоширеніших у світі. Якщо розглядати етіологічну структуру інфекційної захворюваності, то на початку ХХ століття провідну роль відігравали інфекції бактеріальної природи (дифтерія, коклюш, скарлатина, дизентерія). На початку ХХI століття вже домінують інфекційні захворювання вірусної етіології (грип, гострі респіраторні вірусні інфекції (ГРВІ), ентеровірусні, ротавірусна, ГІ, ВІЛ-інфекція, гепатит та ін.). Серед персистуючих внутрішньоклітинних агентів провідне місце за поширеністю посідає група герпесвірусів. Сьогодні інфікованість вірусами герпесу і пов’язана з ними захворюваність у загальній популяції випереджає швидкість приросту населення Землі. За даними ВООЗ, у майбутньому серед інфекційної патології визначальне місце займатиме саме ГІ.
Всесвітня організація охорони здоров’я (ВООЗ) застерігає світове співтовариство про небезпеку прихованої пандемії ГІ. За даними ВООЗ, від 70 до 90 % населення світу інфіковано одним або декількома типами вірусу герпесу і у 50 % з них через відсутність стійкого імунітету щорічно спостерігаються рецидиви захворювання. Герпесвіруси як причина смерті стоять на 2-му місці після грипу — понад 15 % випадків [1, 2, 11, 12]. У США щорічно у 1 600 000 молодих жінок розвивається генітальний герпес, викликаний вірусом простого герпесу (ВПГ) 2-го типу, і у більше ніж 2 % вагітних відзначається сероконверсія до нього протягом вагітності. На Національній конференції з профілактики інфекцій, що передаються статевим шляхом, яка відбулась у березні 2012 р. у Міннеаполісі (США), опубліковані тривожні дані: летальність при ГІ у новонароджених досягає 30 %, а у 20 % дітей, які вижили, відзначаються ураження нервової системи. Частота даного захворювання в США становить 8–60 випадків на 100 000 пологів. Саме майбутня мати є основним джерелом інфекції для плода та новонародженого [5, 13]. Є дані, що до 5-річного віку близько 60 % дітей вже інфіковано вірусами герпесу, а до 15 років їх частка становить 90 %. Більшість людей є довічними вірусоносіями. Причому у 85–100 % випадків первинна інфекція у них має безсимптомний перебіг і тільки в 1–15 % — у вигляді системної інфекції [3, 4, 9]. При цьому практично всі відомі зараз герпесвіруси людини здатні спричиняти ураження нервової системи [4, 6]. У зв’язку з цим герпесвірусні інфекції стали однією з провідних медико-соціальних проблем і набувають загальнодержавного значення.
Термін «герпетична інфекція» вживається стосовно захворювань, що викликаються ВПГ (HSV) 1 і 2. У розвинених країнах Європи на ГІ хворіє третина населення. За даними ВООЗ, захворювання, викликані герпесвірусами, посідають 2-ге місце після грипу та інших ГРВІ у структурі захворюваності та смертності при вірусних інфекціях [7, 8, 10].
Деякі науковці вважають, що саме герпесвіруси несуть відповідальність за значну частину інфекційної патології людини і характеризуються великим розмаїттям шляхів передачі збудника, які здатні уражати практично всі органи і системи людського організму, реплікуватися в усіх клітинах організму: лейкоцитах, тканинних макрофагах, моноцитах, фібробластах, епітеліальних і нервових клітинах, мають тропність до Т-лімфоцитів, спричиняючи їх ураження, поступаючись лише вірусу імунодефіциту за руйнівним ефектом. Зазначені дані дають підстави розглядати герпесвірусну інфекцію як системне захворювання з переважним ураженням того чи іншого органа. Інфікованість населення земної кулі ВПГ‑1 становить 90–97 %, ВПГ‑2 — близько 40 %. Інфікування відбувається в перші 5 років життя.
ВПГ були відкриті V. Gruter 1912 р. Вони належать до родини Herpesviridae, підродини Alphaherpesvirinae. Свою назву родина герпесвірусів отримала від грецького «herpes» — повзучий. До родини герпесвірусів, що виявлені у людини, належать ВПГ 1-го і 2-го типів, вірус герпесу Zoster, цитомегаловірус (ЦМВ), вірус Епштейна — Барр (ВЕБ), вірус герпесу людини 6-го типу (ВГЛ‑6), герпесу людини 7-го типу (ВГЛ‑7), герпесу людини 8-го типу (ВГЛ‑8).
На підставі біологічних властивостей та особливостей реплікації, патогенезу захворювань, клінічної картини, спричинених зазначеними збудниками, всі герпесвіруси, відповідно до рекомендацій Міжнародного комітету з таксономії вірусів, були розділені на 3 субродини (α, β, γ).
Представниками альфа-герпесвірусів є ВПГ 1-го і 2-го типів, вірус вітряної віспи та оперізуючого герпесу. До бета-герпесвірусів належать ЦМВ, два варіанти А і В 6-го і 7-го типу.
До гамма-герпесвірусів належать віруси 4-го та 8-го типів (саркома Капоші — асоційований герпесвірус). Найбільш вивченими є герпесвіруси 1–5-го типів. У більшості випадків інфікування відбувається повітряно-крапельним шляхом при прямому контакті або через предмети побуту (наприклад, через рушник), пероральним (через поцілунки), статевим, трансфузійним (при переливанні крові), трансплацентарним (від матері до плода), трансплантаційним (при пересадці органів) шляхом. У кожної людини захворювання може мати різний перебіг. На цей процес впливають вік, стать, стан імунної системи та супутні захворювання.
/54.jpg)
Джерелом ВПГ-інфекції є особи з різними формами захворювання (у тому числі латентними), а також вірусоносії. ВПГ‑1 передається повітряно-крапельним і контактним шляхом, вражає шкіру, слизові оболонки, центральну нервову систему (ЦНС). Так, під час кашлю або чхання вірус, що знаходиться у крапельках слини, потрапляє на шкіру та інші поверхні й зберігається на них упродовж однієї години. На вологих поверхнях він виживає протягом 3–4 годин, що може бути причиною епідемічного спалаху в дитячих дошкільних установах. Зараження може здійснюватися також через предмети вжитку, інфіковані слиною хворого чи вірусоносія.
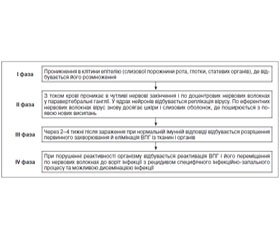
Порушення імунної відповіді — найважливіша ланка у розвитку простого герпесу. У патогенезі ГІ (ВПГ 1-го і 2-го типів) виділяють чотири основні фази: проникнення в клітини епітелію → проникнення в нервові закінчення і паравертебральні ганглії → елімінація вірусу з тканин і органів → реактивація ВПГ і його переміщення до воріт інфекції (рис. 1).
У більшості випадків альфа-герпесвіруси характеризуються значним поліморфізмом. При типовій формі герпесу шкіри виникають згруповані везикульозні висипання на інфільтрованій шкірі, навколо рота, носа, слизових оболонках губ, рідше — на щоках, повіках і вушних раковинах, інших місцях. Появі висипань передують свербіння, печія або біль у відповідній ділянці тіла.
Ураження герпесом слизової оболонки рота супроводжується гарячкою, печією в місці ураження, що посилюється під час їди. На слизовій оболонці щік, піднебіння, язика, ясен з’являються пухирці з прозорим вмістом, які через 2–3 дні перетворюються на ерозії.
Однією з найчастіших форм первинної ГІ, особливо у дітей молодшого віку, є гострий герпетичний стоматит. Етіологія афтозного стоматиту невідома, хоча на герпетичну природу цього захворювання вказував Н.Ф. Філатов. Тепер доведено, що 80 % стоматитів мають герпетичну етіологію.
ВПГ 2-го типу передається статевим або вертикальним шляхом. В останньому випадку зараження може відбуватися під час пологів, трансплацентарно або висхідним шляхом, коли інфекція проникає через цервікальний канал до порожнини матки. ВПГ 2-го типу спричиняє в основному генітальний та неонатальний герпес. Найбільш сприйнятливі до нього діти віком від 5 місяців до 3 років.
ВПГ 2-го типу характеризується виникненням везикул на статевих губах, слизовій оболонці уретри, піхви, шийки матки, шкіри промежини. Не так часто, проте з наявністю тяжкого стану, перебігають неонатальний герпес, мультиформна еритема, герпетична екзема, ураження очей і ЦНС.
Герпес є однією з найбільш поширених хвороб, що передається статевим шляхом і входить у спеціальну програму досліджень, проведених ВООЗ. За даними Національного медичного центру в Англії, генітальний герпес зустрічається в 7 разів частіше, ніж сифіліс. У США щорічно виявляється близько 20 тис. випадків генітального герпесу. У країнах Європи серед хвороб, що передаються статевим шляхом, герпес посідає 2-ге місце після статевого трихомоніазу.
Групи ризику у разі генітального герпесу такі ж, як і при вірусному гепатиті або ВІЛ-інфекції: повії, гомосексуалісти, а також особи з множинними і випадковими сексуальними контактами і великим числом статевих партнерів. Поширеності генітального герпесу сприяє алкоголізм, наркоманія, що ведуть до безладного статевого життя і позашлюбних зв’язків.
Вірус варицелла зостер в осіб молодого віку викликає вітряну віспу, що починається гостро з висипань і підвищення температури тіла. Висипання з’являється спочатку на волосистій частині голови, животі, грудях, плечах, стегнах, а потім без певної закономірності поширюється по всьому тілу, його майже не буває на долонях і підошвах. Цей же вірус в осіб похилого і старечого віку викликає оперізувальний герпес. Важливою передумовою захворювання є зниження імунної реактивності організму. При оперізувальому герпесі процес, як правило, однобічний. Герпетичні пухирці з’являються вздовж нервових стовбурів і сплетінь та супроводжуються сильним болем.
Герпетична і цитомегаловірусна інфекція належать до так званого TORCH-комплексу, викликають внутрішньоутробні хвороби. У дорослого населення ЦМВ-захворювання має переважно латентний перебіг, однак існує можливість внутрішньоутробного ураження внутрішніх органів та ЦНС плода. Клінічне значення має при імунодефіцитних станах і захворюваності вагітних.
Встановлено, що ЦМВ-хвороба є найпоширенішою причиною інфікування плода. Плід інфікується від матері, яка має локалізовану (латентну чи гостру) форму захворювання. Якщо зараження відбувається в ранні терміни вагітності, то може настати смерть плода і мимовільний викидень. Тератогенна дія вірусу може спричинити народження дитини з вадами розвитку.
Більше ніж у 90 % інфікованих новонароджених перебіг ЦМВ хвороби безсимптомний. У решти тяжкість її значно варіює, такі діти відчувають труднощі у навчанні.
Природжена цитомегалія характеризується множинними ураженнями різних органів і систем. Діти частіше народжуються недоношеними. Характерними проявами гострої форми є тривала жовтяниця, гепато- і спленомегалія, геморагічний синдром, ураження органів дихання, ЦНС і гематологічні порушення. До тяжких наслідків може призвести цитомегаловірусний енцефаліт, що спостерігають у 15–20 % хворих із природженою цитомегалією. Перенесений енцефаліт зумовлює утворення кальцифікатів, мікро- та гідроцефалію, відставання в психомоторному розвитку. Зміни ЦНС часто поєднуються з ураженням очей (катаракта, хоріоретиніт, атрофія зорового нерва).
Віруси 3-ї групи (гамма-герпесвіруси) викликають лімфопроліферативні захворювання, інфекційний мононуклеоз (ВЕБ), інтоксикацію, ураження піднебінних і глоткових мигдаликів, збільшення лімфатичних вузлів, печінки, селезінки, зміни у крові. ВЕБ викликає розмноження В-лімфоцитів і персистує в них, тим самим обумовлюючи латентну інфекцію лімфоїдної тканини, епітеліальних клітин, порожнини рота і глотки, слинних залоз. ВЕБ викликає безсимптомну, хронічну чи гостру інфекцію у вигляді інфекційного мононуклеозу, а також лімфопроліферативні захворювання. Інфекційний мононуклеоз характеризується високою лихоманкою, нездужанням, фарингітом, лімфаденопатією, спленомегалією. Хронічна інфекція може розвиватись як циклічна рекурентна хвороба, що супроводжується низькою лихоманкою, підвищеною втомлюваністю, головними болями та запаленням горла.
Лімфопроліферативні захворювання також можуть індукуватися ВЕБ, який є мітогеном для В-лімфоцитів, може сприяти розвитку пухлин. Люди з дефектом Т-клітинного імунітету замість інфекційного мононуклеозу можуть страждати поліклональною лейкемієподібною В-клітинною проліферативною хворобою та лімфомою. Можливий також розвиток Х-зв’язаної лімфопроліферативної хвороби. Реципієнти трансплантата після імуносупресивної терапії є групою ризику для посттрансплантаційної лімфопроліферативної хвороби після контакту з вірусом або реактивації латентного вірусу. Подібні захворювання розвиваються у хворих на СНІД. Діагностика ґрунтується на врахуванні провідних клінічних симптомів (гарячка, тонзиліт, поліаденіт, гепато- і спленомегалія) та характерної гематологічної картини (збільшення числа лімфоцитів більше як на 15 % порівняно з віковою нормою, появою атипових мононуклеоцитів.
Вірус герпесу 7-го типу (ВГ‑7) належить до вірусів, що ростуть повільно, лише на CD4-лімфоцитах людини, які мають клітинні рецептори до цього вірусу. Вірус визначається в периферичній крові та слині. Дуже часто у людей з вірусом герпесу 7-го типу виділяють вірус герпесу 6-го типу. У людини є можливою причиною синдрому хронічної втоми (Chronic Fatigue Syndrome, CFS). Вважають, що вірус герпесу людини 7-го типу може спричинити лімфопроліферативні захворювання.
Синдром хронічної втоми можна запідозрити за сукупністю ряду ознак: безпричинна слабкість, підвищена плаксивість; висока стомлюваність; підвищений рівень тривожності; депресії; порушення сну (фази засипання). На ранок почуття розбитості; температура 36,9–37,3 °С протягом 6 місяців і довше; безпричинне збільшення лімфовузлів — лімфаденопатія.
ДНК вірусу герпесу 8-го типу (ВГ‑8) постійно виявляється в тканинах СНІД-асоційованої саркоми Капоші, в той час як у нормальній тканині сусідніх ділянок не виявляється. Було встановлено, що ВГ‑8 пов’язаний з усіма типами саркоми Капоші, включаючи ендемічну форму цієї патології в африканців, класичну — у літніх людей Середземномор’я та трансплантат-пов’язану. Доведено, що за 3–10 років розвитку саркоми Капоші передує інфекція, викликана ВГ‑8. За допомогою полімеразної ланцюгової реакції (ПЛР) вірус можна виявити в спермі, хоча не завжди. ВГ‑8 був виявлений в ендотеліальних клітинах, циркулюючих CD20 + лімфоцитах (В-клітини), носовому секреті, бронхоальвеолярній рідини у хворих із легеневою локалізацією саркоми Капоші.
Класична форма інфекції проявляється у вигляді локалізованих вузлів коричнево-червоного — синюшно-червоного кольору з локалізацією переважно на шкірі нижніх кінцівок. Виділяють такі стадії захворювання: шкірні прояви, локалізований торпідний перебіг (класичний), локалізований агресивний перебіг зі збільшенням або без збільшення лімфатичних вузлів (африканський локалізований агресивний варіант), генералізовані шкірні прояви або ураження лімфатичних вузлів (африканська лімфаденопатія й ендемічний варіант), вісцеральні прояви (епідемічний варіант).
Нині не викликає сумніву той факт, що найтяжчими проявами герпесвірусної інфекції, після яких відзначається високий процент інвалідизації і смертності, є ушкодження ЦНС. Діапазон неврологічної симптоматики надзвичайно широкий: від синдрому пригнічення, ушкодження черепно-мозкових нервів, судомного синдрому до розвитку менінгоенцефаліту.
Герпесвірусні інфекції належать до групи СНІД-асоційованих інфекцій і вважаються частою причиною ураження ЦНС і внутрішніх органів в осіб зі вторинним імунодефіцитом. Останніми роками роль цих інфекцій як безпосередньої причини летальних випадків серед пацієнтів зі СНІДом стає все більш відчутною. Віруси простого герпесу в цій категорії хворих є провідними етіологічними чинниками різноманітної патології. При традиційно доброякісному перебігу герпесвірусні інфекції можуть проявлятися в тяжких формах, особливо якщо розвиваються на фоні імунодефіцитного стану.
В осіб з імунодефіцитом — при СНІДі, онкологічних, гепатологічних захворюваннях, після терапії імунодепресантами — герпес може набувати поширеного характеру. При цьому везикульозні висипання на шкірі з’являються на тулубі, волосистій частині голови, обличчі, кінцівках, можуть з’являтися виразки, розвивається тяжкий загальноінфекційний синдром. Така форма ГІ нерідко маскується під вітряну віспу. Крім типових везикулярних висипань можуть зустрічатися атипові варіанти висипань. На стоншених ділянках шкіри, частіше на пальцях рук, виникають ледь помітні папульозні елементи — абортивна форма простого герпесу. На ділянках шкіри з дуже пухкою підшкірною клітковиною спостерігається набрякова форма хвороби, коли через виражений набряк і гіперемію везикульозні елементи не помітні.
За потреби для діагностики герпесвірусної інфекції використовуються різні лабораторні методи — від цитологічних до молекулярно-біологічних (ДНК, ДНК-гібридизація і ПЛР). Розпізнавання типових форм ГІ не викликає труднощів і ґрунтується на характерних клінічних проявах.
При неможливості провести диференціальну діагностику на підставі клінічної симптоматики проводять лабораторні дослідження (рис. 2).
Експрес-методом діагностики є метод флюоресцуючих антитіл, при цьому специфічне світіння можна виявити в мазках-відбитках шкіри, слизових оболонок. Використовують серологічні методи дослідження (реакції зв’язування комплементу). Наростання титру антитіл в 4 рази і більше характерно для первинної ГІ. Може бути використаний цитологічний метод, заснований на виявленні в мазках-відбитках багатоядерних гігантських клітин із внутрішньоклітинними включеннями. Створені комерційні ДНК-зонди для молекулярної діагностики простого герпесу в реакції гібридизації та ПЛР.
/57.jpg)
Найпоширенішим є імуноферментний аналіз (ІФА), що дозволяє виявити як вірусоспецифічні антигени, так і специфічні антитіла класів IgM, IgG. Найпростішим і доступним методом лабораторної діагностики ЦМВ-хвороби є цитологічні дослідження осаду слини, сечі, вагінального секрету, ліквору, шлункового вмісту після забарвлення за Папаніколау. Виявлення цитомегалів розглядають як специфічний прояв ЦМВ-хвороби. Спостерігають невеликі клітини овальної чи круглої форми, у ядрі яких відзначають включення, оточене світлим обідком («совине око»).
Для лабораторного підтвердження інфекційного мононуклеозу можна використати серологічні реакції гетерогемаглютинації з баранячими або конячими еритроцитами (Пауля — Брунеля, Гоффа — Бауера, Ловріка — Лі — Давидсона); діагностичним вважають зростання титрів антитіл у 4 рази і більше в парних сироватках, узятих через 7–10 днів. Безперечним підтвердженням діагнозу слід вважати виявлення антигенів збудника або його ДНК за допомогою сучасних високочутливих методів — ІФА, ПЛР, радіоімунологічного аналізу, а також специфічних антитіл до нього (IgM, IgG). Виявлення антитіл класу М свідчить про гостре захворювання, реінфекцію або загострення латентної інфекції. Проте цей імуноглобулін визначається в сироватці крові лише на 10–14-й день захворювання, що зменшує його діагностичне значення. Наявність антитіл класу G у крові свідчить про хронічну інфекцію, персистенцію вірусу в організмі, а чотириразове зростання їх титру в динаміці вказує на активацію ГІ. Діагностика захворювань, викликаних ВГ‑7, полягає у використанні ПЛР, ІФА, імунограми, на якій можна відзначити зниження NK (природні кілери), збільшення CD8-лімфоцитів, ЦВК, IgG; аналіз особистості хворого (симуляція).
Отже, значне поширення герпевірусних інфекцій, можливість пожиттєвої персистенції герпесвірусів в організмі людини, їх реактивація на фоні імунодефіциту, небажані наслідки, труднощі лабораторної діагностики є приводом для подальшого вивчення невирішених аспектів цієї проблеми, що стають актуальними для науки практичної медицини. Це пов’язано з різноманіттям клінічних проявів, особливостями збудників і можливістю їх поширення практично всіма відомими шляхами.
Список литературы
1. Абатуров О.Є. Імунотропний ефект фітопрепарату «Флавозид» / О.Є. Абатуров, І.Л. Височина // Современная педиатрия. — 2008. — № 4(21). — С. 99-102.
2. Знаменська Т.К. Лечение герпесвирусных инфекций (цитомегаловирусной, неонатального герпеса) у детей первого года жизни с применением препарата Флавозид / Т.К. Знаменська, А.О. Писарєв // Здоровье женщины. — 2009. — № 4(40). — С. 60-61.
3. Казмирчук В.Е. Ретроспективный анализ применения препарата Гепримун‑6 у пациентов с инфекцией, вызванной вирусом герпеса 6 типа / В.Е. Казмирчук, Д.В. Мальцев // Клін. імунологія, алергологія, інфектологія. — 2010. — № 5–6(34–35). — С. 64-70.
4. Колоскова О.К. Особливості сучасного перебігу енцефалітів у дітей (огляд клінічних випадків) / О.К. Колоскова, Л.А. Іванова, О.В. Бєлашова, У.І. Марусик, Р.Ю. Білейчук // Актуальная инфектология. — 2015. — № 2(7). — С. 23-29.
5. Крамарєв С.О. Використання препарату «Флавозид» у комплексному лікуванні хронічної активної Епштейна — Барр вірусної інфекції у дітей / С.О. Крамарєв, О.В. Виговська, Л.О. Палатна [та ін.] // Современная педиатрия. — 2008. — № 3(20). — С. 111-114.
6. Мальцев Д.В. Ефективність противірусного лікування при герпесвірусній нейроінфекції зі скроневою епілепсією / Д.В. Мальцев, В.Є. Казмірчук // Міжнарод. неврол. журн. — 2011. — № 4(42). — C. 21-28.
7. Чоп’як В.В. Ефективність монотерапії препаратом протефлазид при лікуванні хворих на хронічну ЕВV вірусну інфекцію в стадії реактивації / В.В. Чоп’як, Г.О. Потьомкіна, І.В. Вальчук [та ін.] // Імунологія та алергологія. — 2008. — № 1. — С. 3-9.
8. Шамсиев Ф.М. Состояние иммунного статуса и эффективность протефлазида в комплексной терапии детей с бронхолегочной патологией, ассоциированной с TORCH-инфекцией / Ф.М. Шамсиев, Н.Х. Мирсалихова, К.И. Алимова [та ін.] // Современная педиатрия. — 2011. — № 2 (36). — С. 39-41.
9. Юліш Є.І. Етіопатогенетична терапія рекурентних респіраторних захворювань у дітей раннього віку на фоні різного перебігу персистуючих інфекцій: Методичні рекомендації / Є.І. Юліш, С.Г. Гадецька, І.В. Баличевцева [та ін.] — Донецьк, 2010. — 48 с.
10. Ярошенко С.Я. Реабілітація дітей з підвищеною захворюваністю на гострі респіраторні інфекції, які мешкають в дитячих закладах закритого типу: Автореф. дис… канд. мед. наук: спец. 14.01.10 «Педіатрія» / С.Я. Ярошенко. — Донецьк: Донецький. нац. мед. ун-т ім. М. Горького, НДІ мед. пробл. сім’ї, 2011. — 25 с.
11. Bao L. Adoptive immunotherapy with CMV-specific cytotoxic T lymphocytes for stem cell transplant patients with refractory CMV infections / L. Bao, M.J. Cowan, K. Dunham // J. Immunother. — 2012. — № 35(3). — S. 293-298. (PMID:22421947 [PubMed — indexed for MEDLINE] PMCID: PMC3306600 Free PMC Article) doi: 10.1097/CJI.0b013e 31824300a2.
12. Doubrovina E. Adoptive immunotherapy with unselected or EBV-specific T cells for biopsy-proven EBV+ lymphomas after allogeneic hematopoietic cell transplantation / E. Doubrovina, B. Oflaz-Sozmen, S.E. Prockop [et al.] // Blood. — 2012. — № 119(11). — S. 2644-2656. (PMID:22138512 [PubMed — indexed for MEDLINE] PMCID: PMC3311278 Free PMC Article) doi: 10.1182/blood‑2011-08-371971. Epub 2011 Dec 2.
13. Nigro G. Immunoglobulin therapy of fetal cytomegalovirus infection occurring in the first half of pregnancy — a case-control study of the outcome in children / G. Nigro, S.P. Adler, G. Parruti // J. Infect. Dis. — 2012. — № 205(2). — S. 215-227. PMID: 22140265 [PubMed — indexed for MEDLINE] Free full text doi: 10.1093/infdis/jir718. Epub 2011 Dec.

/54.jpg)
/55.jpg)
/57.jpg)