Статтю опубліковано на с. 47-52
Хвороба, спричинена вірусом Зіка (ХСВЗ) — це арбовірусне інфекційне захворювання, що характеризується гострим початком, помірним інтоксикаційним синдромом, кон’юнктивітом, висипаннями на шкірі, множинними механізмами передачі та внутрішньоутробним ураженням плода.
За словами голови Всесвітньої організації охорони здоров’я (ВООЗ) Маргарет Чен, нинішній спалах ХСВЗ у Південній Америці свідчить про високу мінливість вірусів та їх здатність до поширення по всій земній кулі, а також можливість викликати хвороби з новими проявами внаслідок реалізації різних механізмів передачі вірусу.
Сучасна епідемія загрожує не лише новими втратами, але й серйозними соціально-економічними збитками, високим рівнем розвитку інвалідності та ризиком поширення в інших державах та на інших континентах. Велика небезпека полягає в тому, що при тривалій циркуляції серед людей вірус Зіка мутує й адаптується [1].
На підставі вищезазначеного хворобу, спричинену вірусом Зіка, та ускладння, що з нею пов’язані, з 1 лютого 2016 р. ВООЗ визнали такими, що здатні серйозно впливати на здоров’я населення і можуть швидко поширюватися у міжнародних масштабах. Хвороба увійшла до переліку подій, що спричинюють надзвичайну ситуацію в галузі охорони здоров’я на світовому рівні та контролюється згідно з вимогами Міжнародних медико-санітарних правил (2005) [1, 2].
Код за МКХ‑10:
А92.8. Інша уточнена лихоманка, що передається комарами.
А93. Інші вірусні лихоманки, що передаються членистоногими, які не класифіковані в інших рубриках.
Вперше вірус Зіка був виділений у 1947 р. від макак-резусів в Уганді, що мешкали в лісі Зіка в межах моніторингу жовтої лихоманки, так званого І типу джунглів. У 1952 р. вірус був виділений від людей, які проживали в Уганді та Об’єднаній Республіці Танзанія. З того часу спалахи ХСВЗ реєструються в Африці, Північній і Південній Америці, Азії та Тихоокеанському регіоні.
До 2007 року спалахи ХСВЗ реєструвалися дуже рідко. Починаючи з 2007 р. до ВООЗ надходили повідомлення про спалахи ХСВЗ із Тихоокеанського регіону (Мікронезії, Французької Полінезії) та островів Яп. У Південній Америці з 2014 р. підтверджена ендемічна передача вірусу Зіка в Чилі. З лютого до червня 2014 р. надходили повідомлення про спалахи цього інфекційного захворювання [3].
У травні 2015 р. органи суспільної охорони здоров’я Бразилії підтвердили автохтонну (що не залежить від зовнішніх факторів) передачу вірусу Зіка в північно-східній частині держави. У жовтні цього ж року зареєстровані випадки інфікування вірусом Зіка в Колумбії, а також надіслані повідомлення про спалахи з Африки (Кабо-Верде). Більше як у 13 державах Північної та Південної Америки зареєстровані окремі випадки інфікування вірусом Зіка, що свідчить про швидке його поширення [5, 10, 21].
До кінця січня 2016 р. були зареєстровані підтверджені випадки ХСВЗ у США, Данії та Швеції. Спалахи ХСВЗ у різних регіонах світу свідчать про потенційні можливості поширення арбовірусів на територіях, де присутні комарі роду Aedes, які є переносниками вірусу Зіка [4, 27, 28].
Від моменту виявлення захворювання, з’ясування його природи та до сьогодні було зафіксовано багато невеликих спалахів. Особливе занепокоєння викликає географічне розширення захворювання.
Станом на лютий 2016 р. маємо перелік країн з автохтонною циркуляцією вірусу Зіка: Аруба, Барбадос, Болівія, Бонайре, Бразилія, Кабо-Верде, Колумбія, Коста-Ріка, Кюрасао, Домініканська Республіка, Еквадор, Сальвадор, Французька Гвіана, Гваделупа, Гватемала, Гайана, Гаїті, Гондурас, Ямайка, Мартініка, Мексика, Нікарагуа, Панама, Парагвай, Сен-Мартен, Самоа, Суринам, Тонга та Венесуела [6–8].
Етіологія
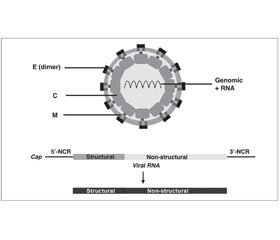
Збудник — РНК-вмісний вірус Зіка (Zika virus), роду Flavivirus, член родини Flaviviridae. Вірус Зіка має оболонку, подібно до інших флавівірусів. Нуклеокапсид у діаметрі близько 20–30 нм із несегментованим одноланковим позитивно-спрямованим РНК-геномом. Геном вірусу оточений мембраною з двошаровою ліпідною оболонкою, на якій розташовані білки. Віріон діаметром 40 нм із поверхневими виступами, що становлять приблизно 5–10 нм. Поверхневі білки розташовані в ікосаедроподібній симетрії. Має дві ділянки, що не кодуються, відомі як 5'-NCR i 3'-NCR. Відкрита рамка зчитування вірусу Зіка кодує поліпротеїни, які згодом розщеплюються в капсид (С), мембранний попередник (PRM), білок (Е) і неструктурні білки (NS). Білок Е становить більшість поверхні вібріона і бере участь у зв’язуванні з клітинами хазяїна і злитті їх мембран [10, 11].
Епідеміологія
Джерело інфекції та резервуар у дикій природі остаточно невідомі. Вчені вважають, що джерелом є деякі мавпи та люди. Людина є джерелом інфекції під час гострого прояву у неї ознак хвороби.
Механізми передачі вірусу Зіка, що на сьогодні підтверджені:
A. Трансмісивний — через укуси інфікованих комарів роду Aedes aegypti та Aedes albopictus у тропічних та екваторіальних регіонах. Дані види комарів поширені у субтропічній та тропічній кліматичних зонах, здатні переносити віруси жовтої лихоманки, Чикунгунья, лихоманки Денге, Західного Нілу та інших арбовірусних захворювань [11, 12, 17].
B. Вертикальний — від матері до дитини, що призводить до проявів тяжких вад внутрішньоутробного розвитку плода (вроджена мікроцефалія та смерть плода, особливо в першому триместрі) [39].
C. Статевий — у 2009 р. уперше встановлений факт передачі вірусу від людини до людини при статевих контактах [15]. Під час останнього спалаху, який виник у Південній Америці, доведено, що вірус Зіка в спермі зберігається понад 30 днів, а на 62-й день не виявлявся у тих, хто перехворів [12].
D. Парентеральний — за допомогою препаратів крові [13, 14]. Вірус Зіка був виявлений у крові, сечі, слині, спинномозковій та амніотичній рідинах, а також у грудному молоці [9].
Про тривалість та напруженість імунітету після перенесеної хвороби поки що невідомо. Хвороба є небезпечною через можливість легкого зараження мандрівників у регіонах Океанії та Америки [15, 16].
За словами керівника Українського центру з контролю та моніторингу захворювань МОЗ України, в нашій державі налічуються 53 види комарів з роду Aedes, щоправда можливість переносу ними вірусу Зіка потребує вивчення [34]. Згідно з повідомленням фахівців Українського науково-дослідного протичумного інституту імені І.І. Мечнікова, фауна України нараховує 32 види кровосисних комарів роду Aedes, проте види Aedes aegypti та Aedes albopictus відсутні [35].
Патогенез
Патогенез хвороби, спричиненої вірусом Зіка, сьогодні достеменно не вивчений. Цьому сприяє відносно легкий клінічний перебіг хвороби, через що немає смертельних наслідків, тому патологоанатомічні зміни взагалі невідомі. Існує припущення, що розмноження вірусу відбувається у найближчих до місця укусу дендритних клітинах. Звідти він надходить до лімфатичних вузлів і кровоносних судин на початку хвороби, і таке триває протягом усього періоду гарячки [38, 39]. Відзначено, що хоча інших представників родини Flaviviridae було виявлено у цитоплазмі сприйнятливих клітин, вірус Зіка натомість спостерігали у ядрах клітин [30–32].
Починаючи з 2013 р., з часів епідемії на теренах Океанії і в подальшому Південної Америки, особливо в Бразилії, було сповіщено про можливість неврологічних та автоімунних ускладнень хвороби, що спричинює вірус Зіка. У випадках мікроцефалії, високий рівень якої у новонароджених у Бразилії пов’язують з дією вірусу, не було поки що виявлено будь-яких особливих рис чи ознак, які б з високою вірогідністю підтвердили зв’язок цих двох патологічних процесів.
У 2015 р. РНК вірусу було виявлено в амніотичній рідині двох плодів, що підтверджує здатність вірусу до проникнення від зараженої вагітної через плаценту до плода [39]. Хоча у багатьох матерів і новонароджених дітей із мікроцефалією знаходили антитіла до вірусу Зіка, однак поки офіційного висновку з приводу того, чи вірус породив мікроцефалію, не було зроблено. Відомо, що інші флавівіруси здатні уражати нервову систему людини, але жодного не було виявлено при вроджених вадах ЦНС у плодів.
Проведені дослідження показують, що в певних випадках при розтині померлих із мікроцефалією в ЦНС були знайдені окремі патологічні зміни структур, а також виявлені у клітинах ультраструктурні компоненти вірусу Зіка. Наведені вище дані не є підставою для повної доказовості, адже незрозуміло, як вірус потрапляє саме у вищі нервові структури плода. Разом із тим показано, що вірус Зіка здатний уражати культури людських нервових клітин [35, 38].
Клінічна картина хвороби
Тривалість інкубаційного періоду досі достеменно не встановлена. Вважають, що вона триває від 2 до 10 діб.
Клінічні симптоми ХСВЗ розвиваються в 20–25 % людей, які були інфіковані вірусом Зіка.
Хвороба починається гостро з підвищення температури тіла до 37,5–38,5 °C, нездужання, з незначними ознаками інтоксикації. Спостерігаються біль у суглобах, особливо дрібних, рук і ніг та помірно виражена міалгія. Хворі скаржаться на головний біль розлитого характеру, макулопапульозний висип на шкірі, виразки на слизових оболонках ротової порожнини та шкіри. При огляді відзначаються ознаки двобічного кон’юнктивіту [1, 2, 10, 38, 39]. Рідше мають місце прояви ураження шлунково-кишкового тракту: спазмоподібні болі в животі, рідкі випорожнення, нудота [30].
Як правило, тривалість вищеописаних симптомів від 2 до 12 днів, у середньому 7 діб. Перебіг ХСВЗ легкий та середнього ступеня тяжкості. Тяжкий перебіг ХСВЗ, що вимагає госпіталізації, реєструється вкрай рідко. Імунітет після перенесеної ХСВЗ стійкий, специфічний, тривалий. Летальність низька [27].
На другому засіданні комітету Міжнародних медико-санітарних правил 8 березня 2016 р. обговорювалося питання можливого зв’язку між хворобою, яку спричинює вірус Зіка, та неврологічними розладами: синдромом Гійєна — Барре і вродженою аномалією — мікроцефалією. Було відзначено, що більш імовірним вважається прямий зв’язок між ними, але остаточний висновок робити ще зарано. Комітет і ВООЗ закликають до всеосяжного продовження наукових досліджень та їх інтенсифікації для більш швидкого розв'язання цього питання [32].
Діагностика
Сьогодні основним методом діагностики та підтвердження ХСВЗ є ПЛР у зразках крові хворого. Серологічні дослідження проводять при обов’язковому паралельному дослідженні на інші флавівіруси, оскільки можуть бути неспецифічні результати внаслідок подібності антитіл проти вірусу Зіка з такими, що утворюються при інших флавівірусних хворобах [25, 26, 28].
На ендемічних територіях тестування рекомендують для тих вагітних жінок, у яких в анамнезі є клінічні ознаки, характерні для ХСВЗ. Разом із тим слід зважати на потенційно велике навантаження на наявні у даний час місцеві ресурси охорони здоров’я. ВООЗ не рекомендує тестування всіх вагітних жінок у районах передачі вірусу Зіка [39]. Проте фахівцям у галузі охорони здоров’я рекомендують розглянути питання щодо проведення у першому триместрі вагітності ультразвукового дослідження для всіх жінок, які звертаються за допологовою медичною допомогою, щоб точно датувати вагітність і зробити базову оцінку морфології плода [38, 39].
При обстеженні хворого слід провести такі лабораторні тести, що є в арсеналі лабораторії «Сінево»:
1033 Тест на вагітність. β-ХГЛ загальний (хоріонічний гонадотропін загальний), для невагітних і вагітних до 4 тижн. + 6 днів.
091 Пакет № 4.1. «Печінкові проби» (9 показників; АЛТ, АСТ, ГГТ, ЛФ, білірубін фракційно, загальний білок, альбумін).
1092 Пакет № 4.3. «Ниркові проби» (3 показники; креатинін, сечовина, сечова кислота).
4019 Клінічний аналіз крові (30 показників; автоматизований + ручна лейкоформула).
1104 Коагулограма (ПВ, % за Квіком, МНО/INR, АЧТЧ, фібриноген, ТВ).
ВООЗ виробила такі критерії діагностики хвороби, спричиненої вірусом Зіка:
1. Підозрюваний випадок. Пацієнт має гарячку та/або висип і щонайменше один із зазначених проявів: артралгія, артрит; кон’юнктивіт (негнійний/з гіперемією).
2. Можливий випадок. У пацієнта з ознаками підозрюваного випадку виявлені антитіла IgM до вірусу Зіка [24] та епідеміологічні критерії (контакт із хворим, у якого підтверджено ХСВЗ; або проживання в регіоні, де підтверджено локальну передачу вірусу Зіка, або подорож за два тижні до появи проявів хвороби).
3. Підтверджений випадок. Пацієнт, у якого лабораторно було виявлено:
A. Наявність РНК вірусу Зіка або його антигену в сироватці крові чи інших зразках (зокрема, слина, біоптати органів, сеча, кров).
B. Наявність IgM проти вірусу Зіка і реакція нейтралізації (PRNT90) [24] для вірусу Зіка з титром ≥ 20 та PRNT90 ≥ 4 порівняно з титром до інших флавівірусів.
C. Виключення можливості хвороб, які спричинюють інші флавівіруси [26].
Лікування
Етіотропне противірусне лікування не розроблено. Легкий перебіг хвороби не спонукає до створення таких ліків, тому провідними є патогенетичні заходи — відновлення втраченої організмом рідини, боротьба з такими симптомами, як головний біль, нездужання тощо.
Гарячку слід зменшувати за допомогою заходів фізичного охолодження (наприклад, протирання шкіри вологими серветками, носіння легкого одягу, прийняття прохолодної ванни або душу) і використання ацетамінофену (парацетамол). Використання ацетилсаліцилової кислоти (аспірин) або інших нестероїдних протизапальних засобів слід уникати до виключення у пацієнта лихоманки Денге [20, 22, 25, 27].
За наявності вираженого головного болю слід приймати ацетамінофен у дозах, які рекомендують для боротьби з високою температурою тіла, некомфортною для конкретної хворої людини [18, 19].
Для зменшення можливого свербіння під час висипань можуть бути використані засоби місцевого застосування: каламіновий лосьйон або ментол на основі водних агентів і пероральні антиалергічні засоби (лоратадин, левоцетиризин, цетиризин).
Хворі, а особливо вагітні, повинні пити багато рідини, щоб уникнути зневоднення внаслідок гарячки, блювання та інших втрат, які можуть відбуватися у період лихоманки [33].
Профілактика
Загальні напрямки. Комітет із Міжнародних медико-санітарних правил не вважає за необхідне введення обмежень на поїздки в країни, де існує циркуляція вірусу Зіка, або на торгівлю з такими країнами з метою запобігання таким чином поширення цього вірусу [15].
ВООЗ підкреслює, що заходи запобігання ХСВЗ мають бути однаковими для всіх верств і категорій населення, в тому числі для вагітних [33, 34].
Специфічна профілактика: вакцинацію на сьогодні не розроблено.
Запобігання укусам комарів (москітів) — головний напрямок профілактики [15] з використанням репелентів. Вони повинні містити DEET (N-діетил‑3-метилбензамід) або ікаридин. Наносити їх треба не тільки на поверхню тіла, але й на одяг. Носіння у вранішній і вечірній час закритого одягу (бажано світлого кольору). Використання фізичних бар’єрів на шляху комарів (екрани, закриті двері та вікна, москітні сітки). Останні потрібно застосовувати й під час денного сну. Постійне провітрювання приміщень [21, 30, 35].
Важливо уникати накопичення вологи у побутовому начинні: контейнерах, відрах, квіткових горщиках або шинах, де комарі знайдуть добрі умови для розмноження (стояча вода) [34, 35].
Особливу увагу слід приділити тим, хто не в змозі захистити себе адекватно, наприклад маленьким дітям, хворим або літнім людям. Зважаючи на неспростоване припущення про зв’язок вірусу з народженням дітей з уродженими вадами, виняткову увагу слід приділяти захисту вагітних, особливо на ранніх тижнях вагітності [27, 39]. Рекомендують проводити захист від укусів комарів і під час першого тижня захворювання на ХСВЗ для того, щоб запобігти подальшому поширенню інфекції серед людей [15, 33].
Список литературы
1. Various (June 2014). Etyologia: Zika Virus // Emerg. Infect. Dis. [Internet] (CDC) 20 (6). doi:10.3201/eid2006.ET2006.
2. Altman L.K. (July 3, 2007). Little-Known Virus Challenges a Far-Flung Health System.
3. WHO. Emergencies preparedness, response. Zika virus infection — Haiti // Disease Outbreak News. 21 January 2016.
4. Anthony S. Fauci, David M. Morens. Zika Virus in the Americas — Yet Another Arbovirus Threat // N. Engl. J. Med. 2016; 374: 601-604. February 18, 2016. Doi: 10.1056/NEJMp1600297
5. WHO. Emergencies preparedness, response. Zika virus infection — France — French Guiana and Martinique // Disease Outbreak News. 8 January 2016.
6. WHO. Emergencies preparedness, response. Zika virus infection — France — Saint Martin and Guadeloupe // Disease Outbreak News. 21 January 2016.
7. WHO. Emergencies preparedness, response. Zika virus infection — United States of America — Puerto Rico // Disease Outbreak News. 8 January 2016.
8. WHO. Emergencies preparedness, response. Zika virus infection — United States of America — United States Virgin Islands // Disease Outbreak News. 29 January 2016.
9. WHO. Emergencies preparedness, response. Microcephaly — Brazil // Disease Outbreak News. 8 January 2016.
10. Epidemiological update: Outbreaks of Zika virus and complications potentially linked to the virus Zika infection. European Centre for Disease Prevention and Control. 18 January 2016.
11. Eric J. Rubin, Michael F. Greene, and Lindsey R. Baden. Zika Virus and Microcephaly // NEJM February 10, 2016. Doi: 10.1056/NEJMe1601862.
12. Jernej Mlakar, Misa Korva, Nataša Tul, Mara Popović, Mateja Poljšak-Prijatelj et al. Virus Associated with Microcephaly // NEJM. February 10, 2016. Doi: 10.1056/NEJMoa1600651.
13. WHO. Emergencies preparedness, response. Guillain-Barré syndrome — El Salvador // Disease Outbreak News. 21 January 2016.
14. Media centre. WHO to convene an International Health Regulations Emergency Committee on Zika virus and observed increase in neurological disorders and neonatal malformations. WHO statement. 28 January 2016.
15. WHO. Media centre WHO Director-Generalsummarizes the outcome of the Emergency Committee on Zika WHO statement on the first meeting of the International Health Regulations (2005) Emergency Committee on Zika virus and observed increase in neurological disorders and neonatal malformations. 1 February 2016.
16. Zika Virus a Global Health Emergency, W.H.O. Says.
17. WHO. Emergencies preparedness, response Zika virus infection — Region of the Americas // Disease Outbreak News. 8 February 2016.
18. WHO. Emergencies preparedness, response. Zika virus infection — Maldives // Disease Outbreak News. 8 February 2016.
19. WHO. Emergencies preparedness, response. Guillain-Barré syndrome — France — Martinique // Disease Outbreak News. 8 February 2016.
20. WHO. Emergencies preparedness, response Guillain — Barré syndrome — Brazil // Disease Outbreak News. 8 February 2016.
21. Emergencies preparedness, response. WHO involvement in Zika // R&D. 8 February 2016.
22. WHO. Emergencies preparedness, response Guillain — Barré syndrome — Colombia and Venezuela // Disease Outbreak News. 12 February 2016.
23. WHO. Emergencies preparedness, response. Microcephaly — United States of America // Disease Outbreak News. 12 February 2016.
24. WHO. Emergencies preparedness, response. Zika virus infection — United States of America // Disease Outbreak News. 12 February 2016.
25. WHO. Emergencies. Zika Outbreak: WHO's Global Emergency Response Plan Global prevention and control strategy. 16 February 2016.
26. WHO. Emergencies preparedness, response. Zika virus infection — Netherlands — Bonaire and Aruba // Disease Outbreak News. 22 February 2016.
27. WHO. Emergencies preparedness, response. Zika virus infection — Saint Vincent and the Grenadines // Disease Outbreak News. 1 March 2016.
28. WHO. Emergencies preparedness, response. Zika virus infection — Netherlands — Sint Maarten // Disease Outbreak News. 4 March 2016.
29. WHO. Emergencies. Zika situation report. 4 March 2016.
30. WHO. Emergencies preparedness, response. Zika virus infection — Argentina and France // Disease Outbreak News. 7 March 2016.
31. WHO. Emergencies preparedness, response. Guillain-Barré syndrome — France — French Polynesia // Disease Outbreak News. 7 March 2016.
32. WHO statement on the 2nd meeting of IHR Emergency Committee on Zika virus and observed increase in neurological disorders and neonatal malformations. WHO statement. 8 March 2016.
33. Faye Oumar; Freire Caio C.M., Iamarino Atila, Faye Ousmane, de Oliveira Juliana Velasco C., Diallo Mawlouth, Zanotto Paolo M.A., Sall Amadou Alpha, Bird Brian (9 January 2014). Molecular Evolution of Zika Virus during Its Emergence in the 20th Century // PLoS Neglected Tropical Diseases. 8 (1): 2636.
34. Вірус Зіка можуть переносити 53 види українських комах — МОЗ. Укрінформ. 2016.02.09.
35. В Україні відсутні комарі видів Aedes aegypti та Aedes albopictus — переносники вірусу Зіка. МОЗ. 2016.02.12.
36. Foy B.D., Kobylinski K.C., Foy J.L. C., Blitvich B.J., Travassos Da Rosa A., Haddow A.D., Lanciotti R.S., Tesh R.B. Probable Non-Vector-borne Transmission of Zika Virus, Colorado, USA // Emerging Infectious Diseases. 2011; 17 (5): 880-882.
37. Buckley A., Gould E.A. Detection of virus-specific antigen in the nuclei or nucleoli of cells infected with Zika or Langat virus // Journal of General Virology. 1988; 69 (Pt 8) (8): 1913-20.
38. Hengli Tang, Christy Hammack, Sarah C. Ogden, Zhexing Wen, Xuyu Qian et al. Zika Virus Infects Human Cortical Neural Progenitors and Attenuates Their Growth Cell Stem Cell. on-line doi: http://dx.doi.org/10.1016/j.stem.2016.02.2016.
39. WHO. Women in the context of microcephaly and Zika virus disease.

/48.jpg)