Резюме
Мета роботи — провести порівняльний аналіз профілю загальнопопуляційних чинників ризику розвитку кардіоваскулярних ускладнень у пацієнтів з ішемічною хворобою серця (ІХС) на тлі нормального та порушеного вуглеводного обміну. Матеріали та методи. З метою оцінки частоти різних форм ІХС залежно від стану вуглеводного обміну були сформовані такі групи: група I — 113 хворих на цукровий діабет (ЦД) 2-го типу, група II — 69 осіб із порушеною толерантністю до глюкози (ПТГ) і група III — 60 осіб без порушень вуглеводного обміну. У подальшому з цих груп обстежених для порівняння профілю чинників ризику розвитку серцево-судинних захворювань були виділені підгрупи хворих з ІХС: 32 хворі на ЦД 2-го типу та ІХС, 14 хворих із ПТГ та ІХС, 10 пацієнтів з ІХС без порушень вуглеводного обміну. Результати. Безбольова ішемія міокарда (ББІМ) була виявлена в 21 (18,6 %) хворого на ЦД 2-го типу, у 5 (7,2 %) осіб із ПТГ і у двох пацієнтів (3,3 %) із нормальним вуглеводним обміном. З показників, що характеризують чинники ризику розвитку серцево-судинних захворювань і мають високу прогностичну цінність щодо наявності ББІМ, комбінація з таких предикторів, як чоловіча стать, тривалість ЦД 2-го типу, наявність обтяженого сімейного анамнезу за ІХС і/або ЦД 2-го типу, вміст HbA1c, холестерину ліпопротеїнів високої щільності, наявність гіпертрофії і діастолічної дисфункції I типу лівого шлуночка, має найбільшу здатність прогнозувати наявність обговорюваної патології у хворих на ЦД 2-го типу. Висновки. Профіль загальнопопуляційних чинників ризику розвитку серцево-судинних захворювань у хворих на ЦД 2-го типу та ІХС є найбільш несприятливим. В осіб із ранніми порушеннями вуглеводного обміну і нормальним вуглеводним обміном він статистично значимо не відрізняється. Хворі на ЦД 2-го типу з ББІМ порівняно з хворими на ЦД 2-го типу без ІХС мають статистично значимо більш виражені порушення показників загальнопопуляційних чинників ризику розвитку серцево-судинних захворювань (куріння, обтяжена спадковість за ІХС і/або ЦД 2-го типу, порушення в системі гемостазу, дисліпідемія), а також додаткових чинників ризику (гіперглікемія, діабетична нефропатія, дисфункція лівого шлуночка).
Цель работы — провести сравнительный анализ профиля общепопуляционных факторов риска развития кардиоваскулярных осложнений у пациентов с ишемической болезнью сердца (ИБС) на фоне нормального и нарушенного углеводного обмена. Материалы и методы. С целью оценки частоты различных форм ИБС в зависимости от состояния углеводного обмена были сформированы следующие группы: группа I — 113 больных сахарным диабетом (СД) 2-го типа, группа II — 69 лиц с нарушенной толерантностью к глюкозе (НТГ) и группа III — 60 лиц без нарушений углеводного обмена. В дальнейшем из этих групп обследованных для сравнения профиля факторов риска развития сердечно-сосудистых заболеваний были выделены подгруппы больных с ИБС: 32 больных СД 2-го типа и ИБС, 14 больных с НТГ и ИБС, 10 пациентов с ИБС без нарушений углеводного обмена. Результаты. Безболевая ишемия миокарда (ББИМ) была выявлена у 21 (18,6 %) больного СД 2-го типа, у 5 (7,2 %) лиц с НТГ и у двух пациентов (3,3 %) с нормальным углеводным обменом. Из показателей, которые характеризуют факторы риска развития сердечно-сосудистых заболеваний и имеют высокую прогностическую ценность относительно наличия ББИМ, комбинация из следующих предикторов: мужской пол, длительность СД 2-го типа, наличие отягощенного семейного анамнеза по ИБС и/или СД 2-го типа, уровень HbA1c, холестерина липопротеинов высокой плотности, наличие гипертрофии и диастолической дисфункции I типа левого желудочка, имеет наибольшую способность прогнозировать наличие обсуждаемой патологии у больных СД 2-го типа. Выводы. Профиль общепопуляционных факторов риска развития сердечно-сосудистых заболеваний у больных СД 2-го типа и ИБС является наиболее неблагоприятным. У лиц с ранними нарушениями углеводного обмена и нормальным углеводным обменом он статистически значимо не отличается. Больные СД 2-го типа с ББИМ по сравнению с больными СД 2-го типа без ИБС имеют статистически значимо более выраженные нарушения показателей общепопуляционных факторов риска развития сердечно-сосудистых заболеваний (курение, отягощенная наследственность по ИБС и/или СД 2-го типа, нарушения в системе гемостаза, дислипидемия), а также дополнительных факторов риска (гипергликемия, диабетическая нефропатия, дисфункция левого желудочка).
Aim of investigation — to conduct the comparative analysis of profile of general population cardiovascular risk factors in patients with ischemic heart disease (IHD) on a background of normal and impaired carbohydrate metabolism. Materials and methods. In order to evaluate the incidence of different forms of IHD depending on the state of carbohydrate metabolism, the following groups were formed: group I — 113 patients with type 2 diabetes mellitus (DM), group II — 69 persons with impaired glucose tolerance (IGT) and group III — 60 individuals without carbohydrate metabolism disorders. In future, subgroups of patients with IHD were formed from these groups to compare cardiovascular risk factors profile: 32 patients with type 2 DM and IHD, 14 persons with IGT and IHD, 10 individuals with IHD without carbohydrate metabolism disorders. Results. Silent myocardial ischemia (SMI) was detected in 21 (18.6 %) patients with type 2 DM, in 5 (7.2 %) persons with IGT and in 2 patients (3.3 %) with a normal carbohydrate metabolism. From indexes that characterize cardiovascular risk factors and have a high prognostic value in relation to the presence of SMI, the combination of such predictors, as sex, type 2 DM duration, family history of IHD and/or type 2 DM, the content of HbA1c, high density lipoproteins, the presence of hypertrophy and type 1 left ventricular diastolic dysfunction, have the greatest ability to predict the development of the discussed pathology in patients with type 2 DM. Conclusions. A profile of general population risk factors of cardiovascular diseases in patients with type 2 DM and IHD is most unfavorable. In persons with early violations of carbohydrate metabolism and with normal carbohydrate metabolism, it does not differ statistically significant. Patients with type 2 DM and SMI, as compared to the patients with type 2 DM without IHD, have statistically significantly more severe violations of general population risk factors for cardiovascular disease (smoking, family history of IHD and/or type 2 DM, disorders in the hemostasis system, dyslipidemia), as well as additional risk factors (hyperglycaemia, diabetic nephropathy, left ventricular dysfunction).
Статтю опубліковано на с. 27-31
Вступ
Поширеність порушень вуглеводного обміну висока і продовжує постійно збільшуватися переважно за рахунок зростання числа хворих на цукровий діабет (ЦД) 2-го типу, яких у світі налічується 415 млн осіб [1]. При ЦД 2-го типу в 33,3–87 % випадків розвивається ішемічна хвороба серця (ІХС), а кардіоваскулярні ускладнення є причиною смерті в 75 % таких пацієнтів [2]. До того ж найбільший внесок у розвиток фатальних серцево-судинних ускладнень робить безбольова ішемія міокарда (ББІМ), що трапляється в 16–60 % асимптомних щодо ІХС хворих на ЦД 2-го типу [3].
Попри те, що ББІМ давно відома і раннє її виявлення має очевидні переваги, скринінг цієї патології у хворих на ЦД практично не здійснюється. Існуючі критерії відбору хворих із можливою ББІМ в основному ґрунтуються на оцінці профілю загальнопопуляційних чинників ризику розвитку серцево-судинних захворювань (ССЗ) і показників електрокардіографії у спокої [4]. Однак, зважаючи на багатогранність патогенезу ББІМ і наявність множинних загальнопопуляційних чинників ризику розвитку ССЗ у хворих на ЦД 2-го типу, можна стверджувати про недостатню ефективність вищезгаданих критеріїв. Висока частота ЦД 2-го типу і потенційна наявність ББІМ практично у кожного пацієнта роблять рутинний скринінг економічно невигідним.
Крім того, для ЦД 2-го типу притаманні поступовий розвиток і прогресування через стадію порушення толерантності до глюкози (ПТГ) [5]. Здійснення скринінгу різних форм ІХС в осіб із ранніми стадіями порушення вуглеводного обміну суттєво збільшить фінансові витрати. Найбільш раціональним розв’язанням цієї проблеми є стратифікація пацієнтів за групами ризику наявності ББІМ із подальшим цілеспрямованим обстеженням тільки пацієнтів високого ризику. Однак на сьогодні не запропоновані методи стратифікації осіб із порушеннями вуглеводного обміну за ризиком наявності в них ББІМ.
Мета дослідження — провести порівняльний аналіз профілю загальнопопуляційних чинників ризику розвитку кардіоваскулярних ускладнень у пацієнтів з ІХС на тлі нормального та порушеного вуглеводного обміну.
Матеріали та методи
Під спостереженням перебували 242 особи віком понад 40 років. Критеріями включення були відсутність діагнозу ІХС згідно з медичною документацією, інформована згода. Критерії виключення — захворювання щитоподібної залози, онкологічна патологія, анемія.
На початковому етапі з метою оцінки частоти ББІМ залежно від стану вуглеводного обміну були сформовані такі групи: група I — 113 хворих на ЦД 2-го типу, група II — 69 осіб із ПТГ і група III — 60 осіб без порушень вуглеводного обміну. У подальшому з цих груп обстежених для порівняння профілю чинників ризику розвитку ССЗ були виділені підгрупи хворих з ІХС: 32 хворі на ЦД 2-го типу та ІХС, 14 хворих із ПТГ та ІХС, 10 пацієнтів з ІХС без порушень вуглеводного обміну.
Усі чинники ризику ССЗ були розділені на загальнопопуляційні (чоловіча стать, похилий вік, куріння, зловживання алкоголем, обтяжений сімейний анамнез щодо раннього розвитку ІХС, менопауза, гіподинамія, ожиріння, артеріальна гіпертензія (АГ), дисліпідемія, гіперфібриногенемія), притаманні для ЦД (тривалість ЦД 2-го типу, глікований гемоглобін, гіперінсулінемія, інсулінорезистентність, діабетична нефропатія, діабетична ретинопатія, діабетична периферична полінейропатія, діабетична автономна кардіоваскулярна нейропатія) і додаткові (потенційні) — віковий андрогенний дефіцит, дисфункція лівого шлуночка (ЛШ).
Сімейний анамнез (СА) щодо наявності ІХС і/або ЦД 2-го типу оцінювали за бальною системою. Показник, що дорівнює 0, — відсутність у всіх близьких родичів (батьків, рідних братів і сестер) як ІХС, так і ЦД 2-го типу. Показник дорівнює 1 за наявності в одного або декількох із вказаних родичів одного і того ж захворювання. У процесі об’єктивного огляду вимірювали артеріальний тиск (АТ) за стандартною методикою, ріст, масу тіла, окружність талії (ОТ) і розраховували індекс маси тіла (ІМТ).
У хворих на ЦД 2-го типу визначали концентрації глюкози плазми натще і через 2 години після їди, а в осіб без порушення вуглеводного обміну в анамнезі виконували пероральний глюкозотолерантний тест (ГТТ) із 75 г глюкози. Дослідження проводили глюкозооксидазним методом. Визначали концентрацію фібриногену, глікованого гемоглобіну (НbА1с), креатиніну плазми, загального холестерину (ЗХС), тригліцеридів (ТГ), холестерину ліпопротеїнів високої (ХС ЛПВЩ) і низької щільності (ХС ЛПНЩ). У всіх обстежених визначали концентрацію імунореактивного інсуліну, у чоловіків — додатково концентрацію загального тестостерону. Розраховували індекс інсулінорезистентності НОМА (homeostasis model assessment) (НОМА-ІР), при значенні НОМА-ІР понад 2,77 діагностували синдром інсулінорезистентності. Функцію ЛШ вивчали в процесі ехокардіографії за стандартним протоколом. Наявність гіпертрофії ЛШ визначали за індексом маси міокарда ЛШ. Діастолічну дисфункцію ЛШ I типу діагностували за часом ізоволюметричного розслаблення ЛШ, співвідношенням пікових швидкостей раннього та пізнього наповнення ЛШ.
Для виявлення ішемічних змін міокарда проводили амбулаторний добовий моніторинг електрокардіографії з обов’язковим досягненням субмаксимальної частоти серцевих скорочень у процесі дослідження. Критеріями ішемії міокарда були наявність одного або більше епізодів депресії сегмента ST > 2 мм тривалістю не менше однієї хвилини і часу між окремими епізодами не менше однієї хвилини. За наявності кореляції з больовим епізодом діагностували больову ІХС, за відсутності — ББІМ.
Статистичний аналіз результатів дослідження проводився з використанням програми Statistica 7.0 (StatSoft Inc., США). Результати кількісних показників подані у вигляді M ± SD, де М — середнє значення, SD (standard deviation) — стандартне відхилення, а якісних — у вигляді абсолютних і відносних (%) величин. Для порівняння кількісних показників використали критерій Стьюдента (при нормальному розподілі ознак) і критерій Манна — Уїтні (при розподілі, відмінному від нормального).
Результати
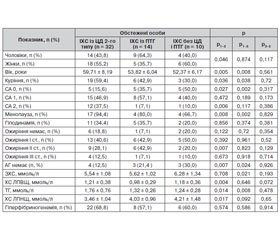
На початковому етапі нами була визначена відносна частота ББІМ у хворих із порушеним і нормальним вуглеводним обміном. ББІМ була виявлена в 21 (18,6 %) хворого на ЦД 2-го типу, у 5 (7,2 %) осіб із ПТГ і у двох пацієнтів (3,3 %) із нормальним вуглеводним обміном. Як бачимо, ББІМ траплялася у хворих на ЦД 2-го типу частіше, ніж у пацієнтів із ранніми порушеннями вуглеводного обміну. ІХС (больова форма) була виявлена в 32 (28,3 %) хворих на ЦД 2-го типу, у 14 (20,3 %) осіб із ПТГ і в 10 (16,7 %) пацієнтів без порушень вуглеводного обміну. Відносна частота ІХС серед хворих на ЦД 2-го типу була вищою, ніж серед обстежених із ПТГ і нормальним вуглеводним обміном. При цьому в останніх двох категоріях обстежених однаково часто відмічалися як ББІМ, так і больова форма ІХС. У процесі порівняльного аналізу загальнопопуляційних чинників ризику ССЗ серед хворих на ІХС були виявлені певні відмінності (табл. 1).
/29.jpg)
Такі чинники ризику ССЗ, як куріння, обтяжений сімейний анамнез за наявності ІХС і/або ЦД 2-го типу, АГ, менопауза, частіше спостерігалися серед пацієнтів з ІХС із ЦД 2-го типу порівняно з пацієнтами з ІХС із ПТГ та ІХС із нормальним вуглеводним обміном. Крім цього, пацієнти з ІХС і ЦД 2-го типу були вірогідно більш старшого віку. З лабораторних показників пацієнти з ІХС усіх трьох груп мали відмінності лише за концентрацією ТГ.
Як свідчать дані табл. 1, у процесі порівняльного аналізу загальнопопуляційних чинників ризику ССЗ у пацієнтів з ІХС і ЦД 2-го типу були виявлені статистично значущі відмінності кількісних і якісних показників порівняно з пацієнтами з ІХС і ПТГ та ІХС із нормальним вуглеводним обміном. До того ж профілі усіх розглянутих загальнопопуляційних чинників ризику ССЗ між пацієнтами з ІХС і ПТГ та ІХС із нормальним вуглеводним обміном вірогідно не відрізнялися.
З урахуванням того, що відносна частота ІХС була вірогідно вищою у хворих на ЦД і ці пацієнти мали найбільш несприятливий профіль загальнопопуляційних чинників ризику ССЗ за відсутності відмінностей в групах осіб із ПТГ і нормальним вуглеводним обміном, доцільним було подальше дослідження тільки групи хворих на ЦД 2-го типу з метою виявлення предикторів ББІМ.
Нами проведений порівняльний аналіз різних груп чинників ризику ССЗ у хворих на ЦД 2-го типу з ББІМ і ЦД 2-го типу без ІХС, а також у хворих на ЦД 2-го типу з ББІМ і ЦД 2-го типу з ІХС.
При порівнянні загальнопопуляційних чинників ризику ССЗ між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу без ІХС були виявлені якісні і кількісні відмінності за показниками таких чинників ризику ССЗ: частота куріння (52,4 проти 26,7 %; р < 0,05); обтяжена спадковість за ІХС і/або ЦД 2-го типу; порушення в системі гемостазу (частота гіперфібриногенемії, 61,9 проти 35,0 %; р < 0,01); вміст ХС ЛПВЩ (р < 0,05).
При порівнянні загальнопопуляційних чинників ризику ССЗ між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу з ІХС були виявлені відмінності за такими показниками: вік (р < 0,001); частота куріння (р < 0,05); частота гіподинамії (р < 0,05); тривалість менопаузи (р < 0,05); ожиріння (р ≤ 0,005).
Як бачимо, такі чинники ризику ССЗ, як куріння, обтяжена спадковість, порушення в системі гемостазу вірогідно частіше спостерігалися в групі хворих на ЦД 2-го типу з ББІІМ порівняно з хворими на ЦД 2-го типу без ІХС. У той же час хворі на ЦД 2-го типу з ББІМ мали сприятливіший профіль загальнопопуляційних чинників ризику ССЗ порівняно з хворими на ЦД 2-го типу з ІХС.
При порівнянні характерних для ЦД чинників ризику ССЗ між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу без ІХС були виявлені статистично значимі відмінності за показниками HbA1c (р < 0,05); частоти нефропатії на стадії протеїнурії з розвитком хронічної хвороби нирок 2-ї ст. (р < 0,005). При порівнянні таких чинників ризику ССЗ між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу з ІХС були виявлені статистично значимі відмінності тільки в препроліферативної ретинопатії (р < 0,05). При порівнянні характерних для цукрового діабету чинників ризику ССЗ між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу без ІХС були виявлені статистично значимі якісні і кількісні відмінності за показниками дисфункції лівого шлуночка (р < 0,05), маси міокарда лівого шлуночка (р < 0,001), індексу маси міокарда лівого шлуночка (р < 0,05).
Загалом хворі на ЦД 2-го типу з ББІМ мали сприятливіший профіль чинників ризику ССЗ порівняно з хворими на ЦД 2-го типу з ІХС, але менш сприятливий — порівняно з хворими на ЦД 2-го типу без ІХС.
Обговорення
У проведеному дослідженні нами була визначена відносна частота різних форм ІХС у групах пацієнтів із порушеним і нормальним вуглеводним обміном. Установлено, що профілі загальнопопуляційних чинників ризику розвитку ССЗ у хворих на ІХС із ранніми порушеннями вуглеводного обміну і осіб без порушення вуглеводного обміну статистично значимо не відрізняються. Це підтверджує результати проведених досліджень іншими авторами [6–8]. Нами виділені показники чинників ризику розвитку ССЗ, за якими можна прогнозувати наявність безбольової ішемії міокарда у хворих на ЦД 2-го типу. Серед усіх пацієнтів із порушеннями вуглеводного обміну ІХС найчастіше спостерігається в групі хворих на ЦД 2-го типу. Крім того, профіль загальнопопуляційних чинників ризику розвитку ССЗ у хворих на ЦД 2-го типу та ІХС є найбільш несприятливим. Відносна частота ІХС у пацієнтів із ранніми порушеннями вуглеводного обміну і нормальним вуглеводним обміном однакова. При цьому відсутні статистично значимі відмінності профілю чинників ризику розвитку ССЗ у вказаних групах.
Між хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу без ІХС спостерігаються статистично значимі відмінності за чинниками ризику розвитку ССЗ (куріння, обтяжена спадковість за ІХС і/або ЦД 2-го типу, порушення в системі гемостазу, дисліпідемія, гіперглікемія, діабетична нефропатія, дисфункція лівого шлуночка); хворими на ЦД 2-го типу з ББІМ і ЦД 2-го типу з ІХС — за чинниками ризику розвитку ССЗ (вік, куріння, гіподинамія, менопауза, ожиріння, діабетична ретинопатія).
З показників, що характеризують чинники ризику розвитку ССЗ і мають високу прогностичну цінність щодо наявності ББІМ, комбінація з таких предикторів, як чоловіча стать, тривалість ЦД 2-го типу, наявність обтяженого сімейного анамнезу за ІХС і/або ЦД 2-го типу, вміст HbA1c, ХС ЛПВЩ, наявність гіпертрофії та діастолічної дисфункції I типу лівого шлуночка, має найбільшу здатність прогнозувати наявність обговорюваної патології у хворих на ЦД 2-го типу.
Як бачимо, усім асимптомним щодо ІХС хворим на ЦД 2-го типу слід проводити оцінку ризику наявності безбольової ішемії міокарда. Для оцінки ризику наявності ББІМ у хворих на ЦД 2-го типу необхідно визначити такі параметри: тривалість ЦД 2-го типу, обтяжена спадковість, величина окружності талії, вміст HbA1c, наявність гіпертрофії лівого шлуночка, діастолічна дисфункція лівого шлуночка I типу.
Висновки
1. У хворих на ЦД 2-го типу відносна частота безбольової ішемії міокарда становить 18,6 %, 7,2 % — в осіб із ПТГ і 3,3 % — із нормальним вуглеводним обміном.
2. Профіль загальнопопуляційних чинників ризику розвитку серцево-судинних захворювань у хворих на ЦД 2-го типу та ІХС є найбільш несприятливим. В осіб із ранніми порушеннями вуглеводного обміну і нормальним вуглеводним обміном він статистично значимо не відрізняється.
3. Хворі на ЦД 2-го типу з безбольовою ішемією міокарда порівняно з хворими на ЦД 2-го типу без ІХС мають статистично значимо більш виражені порушення показників загальнопопуляційних чинників ризику розвитку серцево-судинних захворювань (куріння, обтяжена спадковість за ІХС і/або ЦД 2-го типу, порушення в системі гемостазу, дисліпідемія), а також додаткових чинників ризику (гіперглікемія, діабетична нефропатія, дисфункція лівого шлуночка).
Список литературы
1. Bulugahapitiya U., Siyambalapitiya S., Sithole J., Idris I. Is diabetes a coronary risk equivalent? Systematic review and meta-analysis // Diabet. Med. — 2009. — Vol. 26. — P. 142-148. — doi: 10.1111/j.1464-5491.2008.02640.x.
2. van Dieren S., Beulens J.W., Kengne A.P. et al. Prediction models for the risk of cardiovascular disease in patients with type 2 diabetes: a systematic review // Heart. — 2012. — Vol. 98. — P. 360-369. — doi: 10.1136/heartjnl‑2011-300734.
3. Juutilainen A., Lehto S., Rönnemaa T. et al. Type 2 diabetes as a «coronary heart disease equivalent»: an 18-year prospective population-based study in Finnish subjects // Diabetes Care. — 2005. — Vol. 28. — P. 2901-2907. — doi: 10.2337/diacare.28.12.2901.
4. Rodriguez-Poncelas A., Coll-de-Tuero G., Saez M. et al. Comparison of different vascular risk engines in the identification of type 2 diabetes patients with high cardiovascular risk // BMC Cardiovasc. Disord. — 2015. — Vol. 15(1). — P. 121. — doi: 10.1186/s12872-015-0120-3.
5. Rydén L., Grant P.J., Anker S.D. et al. ESC guidelines on diabetes, prediabetes, and cardiovascular diseases developed in collaboration with the EASD: the Task Force on diabetes, pre-diabetes, and cardiovascular diseases of the European Society of Cardiology (ESC) and developed in collaboration with the European Association for the Study of Diabetes (EASD) // Eur. Heart J. — 2013. — Vol. 34. — P. 3035-3087. — doi: 10.1093/eurheartj/eht108.
6. Seshasai S.R., Kaptoge S., Thompson A. et al. Diabetes mellitus, fasting glucose, and risk of cause-specific death. The Emerging risk factors collaboration. // N. Engl J. Med. — 2011. — Vol. 364. — P. 829-884. — doi: 10.1056/NEJMoa1008862.
7. Shah A.D., Langenberg C., Rapsomaniki E. et al. Type 2 diabetes and incidence of a wide range of cardiovascular diseases: a cohort study in 1,9 million people // Lancet. — 2015. — Vol. 26(385), Suppl. 1. — S. 86. — doi: 10.1016/S0140-6736(15)60401-9.
8. Timbie J.W., Hayward R.A., Vijan S. Variation in the net benefit of aggressive cardiovascular risk factor control across the US population of patients with diabetes mellitus // Arch. Intern. Med. — 2010. — Vol. 170. — P. 1037-1044. — doi: 10.1001/archinternmed.2010.150.

/29.jpg)