Журнал «Здоровье ребенка» 1 (69) 2016
Вернуться к номеру
Диагностика и лечение внебольничной пневмонии у детей
Авторы: Каримджанов И.А., Исканова Г.Х., Исраилова Н.А. - Ташкентская медицинская академия, г. Ташкент, Республика Узбекистан
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
На практике, особенно в амбулаторных условиях, серьезными проблемами педиатрии являются ранняя диагностика и рациональная терапия пневмонии у детей. Наиболее распространенными возбудителями при внебольничной пневмонии являются Streptococcus pneumoniae, Haemophilus influenzae и другие микроорганизмы, в том числе вирусы и грибы. Следует уточнить, что этиология заболеваний нижнего респираторного тракта резко отличается в разных возрастных группах. Самой частой причиной внебольничной пневмонии (до 50 %) является S.pneumoniae, реже встречаются такие палочки, как E.сoli, Klebsiella spp., C.trachomatis, Mycoplasma, Ureаplasma. У детей старше 5 лет в этиологической структуре внебольничной пневмонии наряду с S.рneumoniae возрастает значимость Mycoplasma рneumoniae. Резистентность возбудителей инфекции к антибактериальным препаратам — нарастающая глобальная проблема.
Алгоритм диагностики внебольничной пневмонии включает фебрильную температуру продолжительностью > 3 дней, цианоз, одышку при отсутствии признаков бронхиальной обструкции, кашель. Тахипноэ является одним из лучших предикторов пневмонии у детей всех возрастов. При физикальном обследовании — наличие укорочения перкуторного звука в зоне поражения, бронхиальное или ослабленное дыхание, звучные мелкопузырчатые или крепитирующие хрипы. Для диагностики нетяжелых внебольничных пневмоний вполне достаточно ограничиться клиническими симптомами, рентгенографией легких, общим анализом крови.
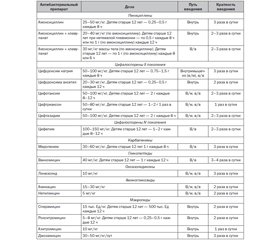
Начальная антибиотикотерапия внебольничной пневмонии проводится эмпирическим путем. При лечении нетяжелых внебольничных пневмоний у детей от 2 мес. до 5 лет препаратом выбора является амоксициллин перорально. Макролиды — препараты выбора у детей от 5 до 16 лет. При тяжелой пневмонии препаратами выбора являются амоксициллин/клавуланат, цефалоспорины II, III, IV поколения. В целом продолжительность антибиотикотерапии при внебольничной пневмонии, вызванной типичными бактериями, составляет 7–10 дней, атипичными бактериями — 10–14 дней. В реальной клинической практике при проведении антибактериальной терапии нередко наблюдаются ошибки, связанные с выбором препарата, пути введения, дозировки, режима применения, длительности курса.
На практиці, особливо в амбулаторних умовах, серйозними проблемами педіатрії є рання діагностика та раціональна терапія пневмонії у дітей. Найбільш поширеними збудниками при позалікарняній пневмонії є Streptococcus pneumoniae, Haemophilus influenzae та інші мікроорганізми, у тому числі віруси і гриби. Слід уточнити, що етіологія захворювань нижнього респіраторного тракту різко відрізняється в різних вікових групах. Найчастішою причиною позалікарняної пневмонії (до 50 %) є S.pneumoniae, рідше зустрічаються такі палички, як E.сoli, Klebsiella spp., C.trachomatis, Mycoplasma, Ureаplasma. У дітей старше 5 років в етіологічній структурі позалікарняної пневмонії поряд із S.рneumoniae зростає значимість Mycoplasma рneumoniae. Резистентність збудників інфекції до антибактеріальних препаратів — наростаюча глобальна проблема.
Алгоритм діагностики позалікарняної пневмонії включає фебрильну температуру тривалістю > 3 днів, ціаноз, задишку при відсутності ознак бронхіальної обструкції, кашель. Тахіпное є одним із кращих предикторів пневмонії у дітей різного віку. При фізикальному обстеженні — наявність укорочення перкуторного звуку в зоні ураження, бронхіальне або ослаблене дихання, звучні дрібнопухирчасті або крепітувальні хрипи. Для діагностики нетяжких позалікарняних пневмоній цілком достатньо обмежитися клінічними симптомами, рентгенографією легень, загальним аналізом крові.
Початкова антибіотикотерапія позалікарняної пневмонії проводиться емпіричним шляхом. При лікуванні нетяжких позалікарняних пневмоній у дітей від 2 міс. до 5 років препаратом вибору є амоксицилін перорально. Макроліди — препарати вибору у дітей від 5 до 16 років. При тяжкій пневмонії препаратами вибору є амоксицилін/клавуланат, цефалоспорини II, III, IV покоління. У цілому тривалість антибіотикотерапії при позалікарняній пневмонії, викликаній типовими бактеріями, становить 7–10 днів, атиповими бактеріями — 10–14 днів. У реальній клінічній практиці при проведенні антибактеріальної терапії нерідко спостерігаються помилки, пов’язані з вибором препарату, шляху введення, дозування, режиму застосування, тривалості курсу.
In practice, especially in the outpatient setting, serious problems of pediatrics are early diagnosis and rational therapy of pneumonia in children. The most common pathogens in community-acquired pneumonia are Streptococcus pneumoniae, Haemophilus influenzae and other microorganisms, including viruses and fungi. It should be clarified that the etiology of diseases of the lower respiratory tract is very different in various age groups. The most common cause of the community-acquired pneumonia (up to 50 %) is S.pneumoniae, such bacilli as E.сoli, Klebsiella spp., C.trachomatis, Mycoplasma, Ureaplasma are more rare. In children older than 5 years, in the etiological structure of the community-acquired pneumonia, along with S.pneumoniae, the importance of Mycoplasma pneumoniae are increasing. The resistance of pathogens to antibacterial therapy — the growing global problem.
Algorithm for the diagnosis of community-acquired pneumonia includes febrile temperature lasting > 3 days, cyanosis, dyspnea in the absence of signs of bronchial obstruction, cough. Tachypnae is one of the best pneumonia predictors in children of all ages. Physical examination reveals the presence of dullness on percussion in the affected area, the bronchial or diminished breath sounds, crackles or wheezing. For the diagnosis of moderate community-acquired pneumonia, it is enough to use clinical symptoms, X-ray of the lungs, common blood test.
The initial antibiotic therapy of community-acquired pneumonia is carried out empirically. In the treatment of severe community-acquired pneumonia in children from 2 months to 5 years, the drug of choice is amoxicillin orally. Macrolides are the drugs of choice for children aged 5 to 16 years. In severe pneumonia, drugs of choice are amoxicillin clavulanate, 2nd–4th generation cephalosporins. In general, the duration of antibiotic therapy in the community-acquired pneumonia caused by typical bacteria is 7–10 days, by atypical bacteria — 10–14 days. In the real clinical practice, the errors associated with the choice of drug, route of administration, dosage, regimen of application, length of treatment are frequent during antibacterial therapy.
внебольничная пневмония, диагностика, антибактериальная терапия.
позалікарняна пневмонія, діагностика, антибактеріальна терапія.
community-acquired pneumonia, diagnosis, antibacterial therapy.
Статья опубликована на с. 133-138
В настоящее время у врача общей практики особую актуальность имеет внебольничная пневмония (ВП) в связи с высокой распространенностью в детской популяции. На практике, особенно в амбулаторных условиях, серьезными проблемами являются ранняя диагностика и рациональная терапия пневмонии у детей. По данным Всемирной организации здравоохранения (ВОЗ), пневмония — главная причина детской смертности во всем мире. В частности среди причин летальности у детей до 5 лет на ее долю приходится 17,5 %, что ежегодно в мире составляет около 1,1 млн смертельных случаев [1, 3, 5].
1. Абатуров А.Е., Герасименко О.Н. Применение цефподоксима проксетила при лечении внебольничных пневмоний у часто болеющих детей раннего возраста // Совр. педиатрия. — 2008. — № 2(19). — С. 26-31.
2. Внебольничная пневмония у взрослых: практические рекомендации по диагностике, лечению и профилактике: Пособие для врачей / Чучалин А.Г., Синопальников А.И., Козлов Р.С. и др. — М., 2010. — 106 с.
3. Внебольничная пневмония у детей: распространенность, диагностика, лечение, профилактика. Научно-практическая программа. — М.: Оригинал-макет, 2010. — 64 с.
4. ВОЗ. Информационный бюллетень № 331 (ноябрь 2013 г.). — URL: http://www.who.int/mediacentre/factsheets/fs331/ru/
5. Геппе Н.А., Малахов А.Б., Волков И.К. и др. К вопросу о дальнейшем развитии научно-практической программы по внебольничной пневмонии у детей // Рус. мед. журн. — 2014. — Т. 22, № 3. — С. 188-193.
6. Геппе Н.А., Розинова Н.Н., Козлова Н.В. и др. Рациональная антибактериальная терапия при внебольничной пневмонии у детей // Клин. неотл. пед. — 2015. — Т. 1, № 1. — С. 24.
7. Каримджанов И.А., Исканова Г.Х., Исраилова Н.А. Ступенчатая терапия внебольничной пневмонии у детей // Здоровье ребенка. — 2014. — № 3. — С. 70-73.
8. Козлов Р.С., Сивая О.В., Кречикова О.И. и др. Динамика резистентности Streptococcus pneumoniae к антибиотикам в России за период 1999–2009 гг. Результаты многоцентрового проспективного исследования ПеГАС // Клин. микробиол. антимикроб. химиотер. — 2010. — № 12(4). — С. 329-341.
9. Козлов Р.С., Чагарян А.Н., Козлова Л.В., Муравьев А.А. Серологическая характеристика и чувствительность к антибиотикам пневмококков, выделенных у детей в возрасте до 5 лет в отдельных регионах Российской Федерации // Клин. микробиол. и антимикроб. химиотер. — 2011. — Т. 13, № 2. — С. 177-187.
10. Самсыгина Г.А. Инфекции респираторного тракта у детей раннего возраста. — М.: Миклош, 2006. — 279 с.
11. Синопальников А.И. Атипичная пневмония // Русский медицинский журнал. — 2002. — Т. 10, № 23. — С. 1080-1085.
12. Спичак Т.В., Ким С.С., Катосова Л.К. Критерии диагностики и соответствие лечения внебольничных пневмоний у детей современным стандартам // Вопросы диагностики в педиатрии. — 2010. — Т. 2, № 6. — С. 31-34.
13. Таточенко В.К. Клинические рекомендации // Педиатрия (Пневмония у детей) / Под ред. А.А. Баранова. — М.: –ГЭОТАР-Медиа, 2005. — 28 с.
14. Black R.E., Cousens S., Johnson H.L. et al.; Child Health –Epidemiology Reference Group of WHO and UNICEF. Global, regional, and national causes of child mortality in 2008: a systematic analysis // Lancet. — 2010. — № 375(9730). — Р. 1969-1987.
15. Black S., Shinefield H., Baxter R. et al. Postlicensure surveillance for pneumococcal invasive disease after use of heptavalent pneumococcal conjugate vaccine in Northern California Kaiser Perma–nente // Pediatr. Infect. Dis. J. — 2004. — № 23(6). — Р. 485-489.
16. Bradley J.S., Byington C.L., Shah S.S. et al. The management of community-acquired pneumonia in infants and children older than 3 months of age: clinical practice guidelines by the Pediatric Infectious Diseases Society and the Infectious Diseases Society of America // Clin. Infect. Dis. — 2011. — Vol. 53, № 7. — P. e25-e76.
17. Cincinnati Children’s Hospital Medical Center. Evidence-based care guideline. Community acquired pneumonia in children 60 days through 17 years of age. — http://www.cincinnatichildrens.org/service/j/andersoncenter/evidence-based-care/community-acquired-pneumonia. Accessed February 14, 2012.
18. Esposito S., Patria M.F., Tagliabue C. et al. CAP in children // European Respiratory Monograph 63: Community-Acquired Pneumonia / Ed. by J. Chalmers, M. Pletz, S. Aliberti. — 2014. — P. 130-139.
19. Jadavji T., Law B., Lebel M.H., Kennedy W.A., Gold R., Wang E.E. A practical guide for the diagnosis and treatment of pediatric pneumonia // CMAJ. — 1997. — № 156(5). — S703-S711.
20. Kimberly S.S., Burton L.H., Christa M.G. Community aguired pneumonia in children // Am. Fam. Physician. — 2012. — № 86(7). — Р. 661-667.
21. Korppi M. Non-specific host response markers in the diffe–rentiation between pneumococcal and viral pneumonia: what is the most accurate combination? // Pediatr. Int. — 2004. — № 46(5). — Р. 545-550.
22. Kumar S., Wang L., Fan J. et al. Detection of 11 common viral and bacterial pathogens causing community-acquired pneumonia or sepsis in asymptomatic patients by using a multiplex reverse transcription-PCR assay with manual (enzyme hybridization) or automated (electronic microarray) detection // J. Clin. Microbiol. — 2008. — № 46(9). — Р. 3063-3072.
23. Michelow I.C., Olsen K., Lozano J. et al. Epidemiology and clinical characteristics of community-acquired pneumonia in hospita–lized children // Pediatrics. — 2004. — № 113(4). — Р. 701-707.
24. Shuttleworth D.B., Charney E. Leukocyte count in childhood pneumonia // Am. J. Dis. Child. — 1971. — № 122(5). — Р. 393-396.
25. Swingler G.H., Hussey G.D., Zwarenstein M. Randomised controlled trial of clinical outcome after chest radiograph in ambulatory acute lower respiratory infection in children // Lancet. — 1998. — № 351(9100). — Р. 404-408.
26. World Health Organization. The Management of Acute Respiratory Infections in Children: Practical Guidelines for Outpatient Care. — Geneva, Switzerland: World Health Organization; 1995.

/135.jpg)
/136.jpg)