Журнал «» 2 (40) 2015
Вернуться к номеру
Сучасне лікування пацієнтів з артеріальною гіпертензією в умовах економічного сьогодення: фокус на дієві комбінації вітчизняного виробництва
Авторы: Радченко Г.Д., Торбас О.О., Сіренко Ю.М., Пономарьова Г.В., Сидоренко П.І., Поліщук С.А., Сніцаренко О.О. — ДУ «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, м. Київ
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Мета. Відомо, що ефективність препаратів, призначених як монотерапія, або їх комбінації різна. Метою цього дослідження було порівняння ефективності терапії на підставі комбінації високоселективного бета-адреноблокатора бісопрололу та гідрохлортіазиду («Б + ГХТ») із дієвою фіксованою комбінацією вітчизняного виробництва — інгібітору ангіотензинперетворюючого ферменту (іАПФ) лізиноприлу та гідрохлортіазиду («Ліз + ГХТ»).
Матеріали і методи. У дослідження було включено 59 пацієнтів із помірною та тяжкою артеріальною гіпертензією (АГ) (середній рівень систолічного (САТ)/діастолічного (ДАТ) артеріального тиску (АТ) — 171,3 ± 2,1/98,6 ± 1,3 мм рт.ст.). Усім пацієнтам на початку дослідження та на етапах лікування проводили такі дослідження: вимірювання маси тіла та зросту, офісного САТ, ДАТ та частоти серцевих скорочень (ЧСС), добове моніторування АТ (ДМАТ), визначення швидкості поширення пульсової хвилі по артеріях еластичного (ШППХе) та м’язового (ШППХм) типів, центрального САТ (цСАТ), біохімічне дослідження крові, електрокардіографію. Пацієнтам призначали або фіксовану комбінацію «Ліз + ГХТ» у добовій дозі 40 мг та 25 мг відповідно (n = 32), або нефіксовану комбінацію бісопрололу 10 мг та гідрохлортіазиду 25 мг (n = 27). Якщо рівень АТ через 1 місяць лікування становив понад 140/90 мм рт.ст., то додавали амлодипін 5 мг, дозу якого збільшували до 10 мг при неефективності терапії на 2-му місяці. Через 3 місяці, за необхідності, додавали доксазозин 2–4 мг.
Результати. Відбулося достовірно однакове зниження офісних рівнів САТ/ДАТ як у групі «Ліз + ГХТ», так і в групі «Б + ГХТ» (44,5 ± 1,9/19,0 ± 2,1 мм рт.ст. та 42,4 ± 2,1/18,8 ± 2,5 мм рт.ст. у кожній групі відповідно, Р = НД для різниці між групами). Кількість пацієнтів, які досягли цільового АТ, становила 31,2; 53,1; 84,4 і 93,8 % у групі «Ліз + ГХТ» та 22,2; 48,1; 85,2 і 92,6 % — у групі «Б + ГХТ» на 1, 2, 3 та 6-му місяці відповідно. Показники 24САТ/24ДАТ у групі «Ліз + ГХТ» знизилися на 19,0 ± 3,3/19,3 ± 2,8 мм рт.ст., у групі «Б + ГХТ» — на 24,1 ± 1,8/16,9 ± 1,2 мм рт.ст. Крім того, ми спостерігали достовірне зниження середньодобової ЧСС у цій групі. Зниження цСАТ у групі «Ліз + ГХТ» було достовірно більшим, ніж у групі комбінації бісопрололу та гідрохлортіазиду (25,9 ± 2,9 мм рт.ст. проти 15,4 ± ± 2,9 мм рт.ст. відповідно; Р < 0,05 для різниці ступеня зниження цСАТ між групами). У групі «Б + ГХТ» відбулося достовірне збільшення індексу аугментації (від 19,7 ± 1,7 % до 24,6 ± 1,5 %; Р < 0,05), у групі «Ліз + ГХТ» індекс достовірно не змінився. Достовірної динаміки ШППХе та ШППХм в жодній групі не спостерігалося. У групі «Ліз + ГХТ» ШППХе знизилася на 1,2 ± 0,08 м/с, у групі «Б + ГХТ» — на 0,63 ± 0,09 м/с, різниця між групами була достовірною (Р < 0,001). Спостерігалося достовірне зниження рівня креатиніну на 6-му місяці лікування у групі «Ліз + ГХТ» (від 88,9 ± 3,7 мкмоль/л до 74,7 ± 3,8 мкмоль/л; Р < 0,05), у той час як на фоні застосування комбінації бісопрололу та гідрохлортіазиду цей показник знизився від 88,6 ± 3,2 мкмоль/л до 83,3 ± 2,5 мкмоль/л (Р = НД).
Висновки. Незважаючи на майже еквівалентне зниження рівня брахіального АТ за результатами як офісного вимірювання, так і добового моніторування, терапія на основі комбінації «Ліз + ГХТ» достовірно краще впливала на зниження цСАТ. Крім того, лише у цій групі ми спостерігали достовірне зниження концентрації креатиніну сироватки наприкінці дослідження.
Цель. Известно, что эффективность препаратов, назначенных в виде монотерапии или комбинации, разная. Целью данного исследования было сравнение эффективности терапии на основе комбинации высокоселективного бета-адреноблокатора бисопролола и гидрохлортиазида («Б + ГХТ») с действенной фиксированной комбинацией отечественного производства ингибитора ангиотензинпревращающего фермента лизиноприла и гидрохлортиазида («Лиз + ГХТ»).
Материалы и методы. В исследование включили 59 пациентов с умеренной и тяжелой АГ (средний уровень систолического (САД)/диастолического (ДАД) артериального давления (АД) — 171,3 ± 2,1/98,6 ± 1,3 мм рт.ст.). Всем пациентам в начале исследования и на этапах лечения проводили: измерение массы тела и роста, офисного САД, ДАД и частоты сердечных сокращений (ЧСС), суточное мониторирование АД (СМАД), определение скорости распространения пульсовой волны по артериям эластичного (СРПВэ) и мышечного (СРПВм) типов, центрального САД (цСАД), биохимическое исследование крови, электрокардиографию. Пациентам назначали либо фиксированную комбинацию «Лиз + ГХТ» в дозе 40 мг и 25 мг соответственно (n = 32), либо нефиксированную комбинацию бисопролола 10 мг и гидрохлортиазида 25 мг (n = 27). Если уровень АД через 1 месяц лечения составлял свыше 140/90 мм рт.ст., то добавляли амлодипин 5 мг, дозу которого увеличивали до 10 мг при неэффективности терапии на 2-м месяце. Через 3 месяца, при необходимости, добавляли доксазозин 2–4 мг.
Результаты. Наблюдалось достоверно одинаковое снижение офисного уровня САД/ДАД как в группе «Лиз + ГХТ», так и в группе «Б + ГХТ» (44,5 ± 1,9/19,0 ± 2,1 мм рт.ст. и 42,4 ± 2,1/18,8 ± 2,5 мм рт.ст. в каждой группе соответственно, Р = НД для разницы между группами). Количество пациентов, достигших целевого АД, составляло 31,2; 53,1; 84,4 и 93,8 % в группе «Лиз + ГХТ» и 22,2; 48,1; 85,2 и 92,6 % — в группе «Б + ГХТ» на 1, 2, 3 и 6-м месяце соответственно. Уровни 24САД/24ДАД в группе «Лиз + ГХТ» снизились на 19,0 ± 3,3/19,3 ± 2,8 мм рт.ст., в группе «Б + ГХТ» — на 24,1 ± ± 1,8/16,9 ± 1,2 мм рт.ст., кроме того, мы наблюдали достоверное снижение среднесуточной ЧСС в этой группе. Снижение цСАТ в группе «Лиз + ГХТ» было достоверно больше, чем в группе применения комбинации бисопролола и гидрохлортиазида (25,9 ± 2,9 мм рт.ст. против 15,4 ± 2,9 мм рт.ст. соответственно; Р < 0,05 для разницы степени снижения цСАТ между группами). В группе «Б + ГХТ» произошло достоверное повышение индекса аугментации (с 19,7 ± 1,7 % до 24,6 ± 1,5 %; Р < 0,05), в группе «Лиз + ГХТ» индекс достоверно не изменился. Достоверной динамики СРПВэ и СРПВм ни в одной из групп не наблюдалось. В группе «Лиз + ГХТ» СРПВэ снизилась на 1,20 ± 0,08 м/с, в группе «Б + ГХТ» — на 0,63 ± 0,09 м/с, разница между группами была достоверной (Р < 0,001). Наблюдалось достоверное снижение уровня креатинина на 6-м месяце лечения в группе «Лиз + ГХТ» (с 88,9 ± 3,7 мкмоль/л до 74,7 ± 3,8 мкмоль/л; Р < 0,05), в то время как на фоне применения комбинации бисопролола этот показатель снизился с 88,6 ± 3,2 мкмоль/л до 83,3 ± 2,5 мкмоль/л (Р = НД).
Выводы. Несмотря на почти эквивалентное снижение уровня брахиального АД как по результатам офисного измерения, так и согласно данным суточного мониторирования, терапия на основе комбинации «Лиз + ГХТ» достоверно лучше влияла на снижение цСАД. Кроме того, только в этой группе мы наблюдали достоверное снижение концентрации креатинина сыворотки в конце исследования.
Objective. It is known that the effectiveness of medications prescribed alone or as a combination is different. The objective of this study was to compare the effectiveness of therapy based on a combination of highly selective beta-blocker bisoprolol and hydrochlorothiazide (B + HCT) and an effective fixed combination of angiotensin-converting enzyme inhibitor lisinopril and hydrochlorothiazide (Lis + HCT) of domestic production.
Materials and Methods. The study included 59 patients with moderate to severe arterial hypertension (mean systolic (SBP)/diastolic blood pressure (DBP) — 171.3 ± 2.1/98.6 ± 1.3 mmHg). All patients at baseline and during follow-up underwent following procedures: measurements of weight and height, office SBP, DBP and heart rate (HR), ambulatory BP monitoring, determination of the pulse wave velocity in arteries of elastic (PWVe) and muscle (PWVm) types, central SBP (cSBP), biochemical blood tests, electrocardiography. Either a fixed combination Lis + HCT in a daily dose of 40 and 25 mg (n = 32), or a free combination of bisoprolol 10 mg and hydrochlorothiazide 25 mg (n = 27) were prescribed to the patients. If BP level after 1 month of treatment was higher than 140/90 mmHg, amlodipine 5 mg was added, its dose was increased to 10 mg if the therapy was insufficient on the 2nd month. In 3 months, if necessary, doxazosin 2–4 mg was added.
Results. There was the same significant decrease of office SBP/DBP in both Lis + HCT, and B + HCT groups (44.5 ± 1.9/19.0 ± ± 2.1 mmHg and 42.4 ± 2.1/18.8 ± 2.5 mmHg in each group, respectively, P was non-significant (NS) for difference between groups). The proportion of patients achieved target BP was 31.2, 53.1, 84.4 and 93.8 % in Lis + HCT group and 22.2, 48.1, 85.2 and 92.6 % in B + HCT group on the 1st, 2nd, 3rd and 6th months, respectively. 24SBP/24DBP decreased by 19.0 ± 3.3/19.3 ± 2.8 mmHg in Lis + HCT group and by 24.1 ± 1.8/16.9 ± 1.2 mmHg in B + HCT group, in addition, we observed a significant reduction in average daily HR in this group. Decrease of cSBP in Lis + HCT group was significantly higher than in group of bisoprolol-based combination (25.9 ± 2.9 mmHg vs 15.4 ± 2.9 mmHg, respectively; P < 0.05 for the degree difference of cSBP reduction between groups). In B + HCT group, a significant increase of augmentation index (from 19.7 ± 1.7 % to 24.6 ± 1.5 %; P < 0.05) was observed, in Lis + HCT group this index was not significantly changed. Significant dynamics of PWVe and PWVm wasn’t observed in any of the groups. In Lis + HCT group, PWVe decreased by 1.20 ± ± 0.08 m/s, in B + HCT group — by 0.63 ± 0.09 m/s, the difference between groups was significant (P < 0.001). There was a significant reduction in creatinine level on 6th month of treatment in Lis + HCT group (from 88.9 ± 3.7 µmol/l to 74.7 ± 3.8 µmol/l; P < 0.05), while in the group of bisoprolol combination this parameter decreased from 88.6 ± 3.2 µmol/l to 83.3 ± 2.5 µmol/l (P = NS).
Conclusions. Despite almost equivalent brahial BP decrease, according to both office measurement and the data of 24-hour monitoring, therapy based on combination of Lis + HCT had significantly better effect on cSBP reducing. Besides, only in this group we observed a significant decrease of serum creatinine concentration at the end of the study.
центральний артеріальний тиск, лізиноприл, бісопролол, гідрохлортіазид.
центральное артериальное давление, лизиноприл, бисопролол, гидрохлортиазид.
central blood pressure, lisinopril, bisoprolol, hydrochlorothiazide.
Статья опубликована на с. 57-69
Вступ
Останнім часом науковці та клініцисти зійшлися у поглядах стосовно того, що, оскільки зниження рівня артеріального тиску (АТ) саме по собі допомагає покращити кардіоваскулярний прогноз [3], байдуже, що обрати для початку антигіпертензивної терапії — бета-адреноблокатор (ББ), діуретик, антагоніст кальцієвих каналів, інгібітор ангіотензинперетворюючого ферменту (іАПФ) або блокатор рецепторів ангіотензину ІІ (БРА). Проте є конкретні ситуації, у яких перевагу мають окремі класи антигіпертензивної терапії, що відкривають перед нами можливості оптимального підбору медикаментозного лікування.
У більшості нових рекомендацій ідеться про те, що лікування пацієнтів із помірною та тяжкою артеріальною гіпертензією (АГ) можна та навіть варто розпочинати з призначення комбінованої антигіпертензивної терапії, адже в світлі доказової медицини ці пацієнти належать до групи високого ризику, а тому комбінування декількох засобів для швидкого та тривалого досягнення ефективного контролю АТ і впливу одразу на декілька факторів ризику є цілком виправданим [1].
На практиці переваги має використання фіксованих комбінацій, що сприяють покращенню прихильності пацієнтів до терапії. Найбільш уживаними у цей момент є комбінації іАПФ або БРА з діуретиками. Згідно з українськими національними рекомендаціями, такі комбінації є одними з найбільш оптимальних для використання. Іншою схваленою комбінацією є додавання до блокаторів ренін-ангіотензинової системи (РАС) антагоністів кальцієвих каналів, що забезпечує достатній контроль АТ та сприятливо впливає на прогноз [1].
У 2013 році вийшли у світ нові і до сьогодні останні рекомендації Європейського товариства кардіологів/Європейського товариства гіпертензії, в яких наведено ці ж класи препаратів, кожен з яких можна використовувати для початку антигіпертензивної терапії як монотерапії, так і їх комбінацій. Зокрема, європейські фахівці звертають нашу увагу на те, що найбільш оптимальними для використання є комбінації іАПФ/БРА із блокаторами кальцієвих каналів (БКК) або діуретиком. Автори документа цитують результати великих досліджень, на підставі яких подібні комбінації вважаються раціональними [2, 6, 8].
Відповідно до наведених європейських та українських рекомендацій сучасна адекватна терапія АГ має складатися з іАПФ, або БРА з діуретиком (частіше за все тіазидним), або БКК, бажано дигідропіридинового ряду [11]. І на практиці ми вже звикли використовувати саме такі комбінації. Інша справа, будь-який фахівець з АГ, лікуючи пацієнтів високого ризику або з резистентним перебігом хвороби, буде надавати перевагу брендовим препаратам або якісним генеричним препаратам, бажано, якісного виробництва. У реальних клінічних умовах такий підхід цілком виправданий: у випадку, коли ми очікуємо потужного клінічного ефекту або коли оцінюємо терапевтичну відповідь на введення певного антигіпертензивного агента, неякісним препаратам просто немає місця. Більше того, коли антигіпертензивна, антитромбоцитарна або ліпідознижуюча терапія вже підібрана, але постійно рекомендовано приймати генеричні препарати, слід розуміти, що реальний вплив на прогноз буде дещо менший від того, що був показаний у рандомізованих клінічних дослідженнях для однойменних препаратів [5, 14].
У брендових препаратів або якісних генериків безліч переваг: висока ефективність, низька частота побічних ефектів, зручний режим дозування, висока прихильність пацієнтів та широкий асортимент вдалих, іноді потрійних фіксованих комбінацій. І при цьому в усіх є один вагомий недолік — доволі висока вартість. До недавнього часу на цей факт можна було б не зважати, пацієнти й самі схилялися до призначення лише якісних і ефективних препаратів, більшість орієнтувались на продукцію іноземного виробництва.
Проте наразі ми повинні зрозуміти і прийняти: економіка країни перебудовується. З цим пов’язані певні тимчасові труднощі, в тому числі в галузі охорони здоров’я. І не зважати на це ми не можемо. На сьогодні призначення подібних препаратів стало проблематичним: навіть якщо пацієнт і зможе дозволити собі купити декілька упаковок дорогих ліків, ми не до кінця впевнені в тому, чи зможе пацієнт приймати цей препарат надалі і тривало. Адже антигіпертензивна терапія — це не антибіотики, що можна «поприймати» курсом та забути. Лікування в кардіології не може складатися з курсів, ефективність такого підходу до лікування майже нульова. Скоріше за все, пацієнт закінчить приймати упаковку дорогого препарату, а потім перед ним постане вибір: або замінити препарат більш дешевим, або припинити прийом узагалі. І, як не сумно, доволі часто пацієнти обирають другий варіант, адже не знають, що існують більш дешеві дієві препарати, тим більше вітчизняного виробництва.
Ми зробили спробу підібрати таку комбінацію та оцінити ефективність терапії на її підставі у пацієнтів із помірною та тяжкою артеріальною гіпертензією, лікування яких, як правило, вимагає від нас стартово призначати високоефективне комбіноване лікування. Метою цього дослідження було порівняння терапії на підставі дієвої комбінації широковідомого, з достатньою доказовою базою іАПФ лізиноприлу [16] та гідрохлортіазиду («Ліз + ГХТ») вітчизняного виробництва з комбінацією бета-адреноблокатора бісопрололу [12] із гідрохлортіазидом («Б + ГХТ») європейського виробника. Особливістю цього дослідження було те, що препарати призначалися у високих дозах від самого початку дослідження.
Матеріали та методи
У дослідження було включено 59 пацієнтів із помірною та тяжкою АГ (середній рівень систолічного (САТ)/діастолічного (ДАТ) АТ — 171,3 ± 2,1/98,6 ± 1,3 мм рт.ст.). Критеріями включення у дослідження були: чоловіки та жінки віком від 18 до 75 років; есенціальна АГ 2–3-го ступеня; відсутність критеріїв виключення.
Критеріями виключення були: неконтрольована або резистентна АГ; ангіоневротичний набряк в анамнезі, гіперкаліємія (> 5,5 ммоль/л) або гіпокаліємія (< 3,5 ммоль/л), стенотичне двостороннє ураження судин нирок, гостра серцева недостатність, порушення серцевого ритму (хронічна фібриляція передсердь, часта екстрасистолічна аритмія, шлуночкова або надшлуночкова тахікардія, тахікардія (частота серцевих скорочень (ЧСС) понад 100 уд/хв), порушення АВ-провідності, або синусова брадикардія, або синдром слабкості синусового вузла, наявність вад серця, вагітність або лактація, злоякісний перебіг АГ, вторинна АГ, виражена артеріальна гіпотонія (САТ нижче 90 мм рт.ст.), бронхіальна астма, декомпенсовані захворювання печінки (рівень аспартатамінотрансферази (АСТ) та/або аланінамінотрансферази (АЛТ) вищий за верхню межу норми у 3 рази), гостра або хронічна ниркова недостатність (рівень креатиніну сироватки крові ≥ 133 мкмоль/л), серцева недостатність вище за II функціональний клас (ФК) (згідно з Нью-Йоркською класифікацією), гостре порушення мозкового кровообігу в анамнезі, наявність стенокардії напруження ІІІ–IV ФК або вазоспастичної стенокардії, інфекційні та онкологічні захворювання, стани, що супроводжуються ендогенною депресією (чи наявністю депресивних станів у сім’ї), цукровий діабет, ожиріння, тобто індекс маси тіла (ІМТ) > 35 кг/м2, виражені захворювання периферичних судин, синдром Рейно, стан після хірургічного втручання (менше 1 місяця), прийом стероїдних та нестероїдних протизапальних засобів, контрацептивів, значні психічні розлади, неможливість відмінити попередню антигіпертензивну терапію, участь в іншому дослідженні.
Методи дослідження. Усім пацієнтам на початку дослідження та на етапах лікування проводили: вимірювання маси тіла та зросту, офісного САТ, ДАТ та ЧСС, добове моніторування АТ (ДМАТ), визначення швидкості поширення пульсової хвилі по артеріях еластичного (ШППХе) та м’язового (ШППХм) типів, центрального САТ, біохімічне дослідження крові (рівні калію, натрію, креатиніну, сечової кислоти, АЛТ, АСТ, білірубіну, глюкози, загального холестерину, тригліцеридів, холестерину високої та низької щільності сироватки крові), електрокардіографію (ЕКГ).
Біохімічні аналізи проводили на автоматичному фотометрі Livia (Сormay, Польща) в лабораторії ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України. Швидкість клубочкової фільтрації (ШКФ) розраховували за формулою CKD-EPI [9]. Проводили також загальноклінічні дослідження крові та сечі.
Вимірювання офісного САТ та ДАТ здійснювали на початку дослідження, після семиденної (стосується пацієнтів, в яких був період «відмивання») відміни всіх антигіпертензивних препаратів та на етапах спостереження. Вимірювали АТ у положенні сидячи тричі з інтервалом 1–2 хвилини. Визначали середнє з трьох вимірів. ЧСС визначали після другого вимірювання.
ІМТ визначали за формулою:
ІМТ = маса тіла/(ріст), кг/м2.
ДМАТ проводили на портативному апараті АВРМ-04 (Meditech, Угорщина) у такому режимі: у денний час — кожні 15 хв, уночі (з 22:00 до 6:00) — кожні 30 хв. Хворі вели звичайний спосіб життя, виконуючи побутові фізичні та психоемоційні навантаження [13]. При цьому вивчали такі показники: середньодобовий (24), денний (д), нічний (н) та максимальний (макс.) САТ і ДАТ, ЧСС. При комп’ютерному аналізі ДМАТ для САТ і ДАТ розраховували індекс часу (Час.Ін.), що характеризує часове перевантаження тиском упродовж доби і визначається як відсоток вимірів АТ, що перевищує 140/90 мм рт.ст. удень і 120/80 мм рт.ст. уночі. Визначали індекс площі (Ін.Пл.), що є площею між кривою підвищеного АТ та лінією межі норми. Обидва ці індекси здатні впливати на перебіг АГ і, як наслідок, на прогноз. Варіабельність АТ (Вар.) обчислювали як стандартне відхилення величини САТ і ДАТ. Крім того, за допомогою програмного забезпечення разраховували добовий індекс (ДІ) — процент зниження нічного АТ порівняно з денним.
ШППХ та центральний АТ визначалися на апараті Sphygmocor-PVx (AtCor Medical Pty Ltd, Австралія), з’єднаному з персональним комп’ютером, що дозволяє проводити аналіз форми пульсової хвилі та визначати ШППХе і ШППХм [15]. П’єзодатчики встановлювали на правій загальній сонній артерії, на стегновій артерії та на радіальній артерії правого передпліччя під візуальним (за допомогою монітора) та автоматичним контролем якості, що здійснювався згідно з програмою приладу. Час запізнення пульсової хвилі та ШППХ, центральний АТ визначали приладом автоматично після введення величини відстані між датчиками, що вимірювалася сантиметровою смужкою. Для оцінки пружно-еластичних властивостей артерій еластичного типу ШППХ визначали на сегменті «сонна артерія — стегнова артерія», для оцінки пружно-еластичних властивостей артерій м’язового типу — на сегменті «сонна артерія — радіальна артерія». Центральний АТ визначали за допомогою програмного забезпечення приладу на підставі АТ на плечовій артерії та форми отриманої пульсової хвилі у висхідній аорті. Також за допомогою програмного забезпечення визначали індекс часу викиду (ED) та індекс субендокардіальної життєздатності (SEVR).
Методи лікування. Схему титрації наведено на рис. 1.
Якщо пацієнти не приймали ліки на момент скринінгу, то у день рандомізації методом сліпих конвертів їм призначали фіксовану комбінацію «Ліз + ГХТ» у добовій дозі 40 та 25 мг відповідно (препарат ліпразид 20/12,5 мг 2 табл. вранці натще; виробництво «Борщагівський ХФЗ», Україна) або нефіксовану комбінацію бісопрололу (конкор у добовій дозі 10 мг; виробництво компанії Nycomed, Німеччина) та гідрохлортіазид (гіпотіазид у добовій дозі 25 мг; виробництво Sanofi-Aventis, Франція). Перший прийом ліків відбувався в офісі лікаря-дослідника. Оцінку антигіпертензивної ефективності проводили через 1 місяць лікування. Якщо рівень АТ через 1 місяць лікування становив понад 140/90 мм рт.ст., то до лікування основним препаратом додавали амлодипін 5 мг (тенокс; виробництво компанії KRKA, Словенія), дозу якого збільшували до 10 мг при неефективності терапії на 2-му місяці лікування. Якщо на 3-му місяці лікування рівень АТ залишався вищим за 140/90 мм рт.ст., то до лікування додавали доксазозин (кардура; виробництво компанії Pfizer, США) у добовій дозі 2–4 мг.
Якщо пацієнт до включення у дослідження отримував антигіпертензивні препарати, то рандомізації передував період відмивання, що становив 7 днів. Наприкінці періоду відміни повторно оцінювали критерії включення у дослідження. Якщо пацієнт відповідав критеріям включення і не мав критеріїв виключення, то відбувалася рандомізація пацієнта за наведеною вище схемою.
Супутнє лікування включало модифікацію способу життя, прийом статинів та ацетилсаліцилової кислоти. Групи рандомізації були порівнянними за кількістю пацієнтів, яким призначали супутні препарати.
Прихильність хворих до лікування визначалася нами за допомогою обчислення індексу на підставі розрахунку кількості таблеток, що пацієнту було видано (пацієнт забезпечувався ліками на 4 тижні), кількості таблеток, що їх пацієнт повернув, та кількості днів, що пацієнт мав приймати ліки.
(Кількість таблеток, що ви-
дано, – кількість таблеток,
що повернув)
Прихильність = ________________________ • 100, %.
Кількість днів, що пацієнт мав приймати
Прихильність > 80 % вважалася високою, 60–80 % — помірною, < 60 % — низькою. Визначення прихильності проводили тільки для комбінацій «Ліз + ГХТ» та «Б + ГХТ».
Статистична обробка. Статистичну обробку результатів проводили після створення баз даних у системах Microsoft Excel. Середні показники обстежених пацієнтів визначали за допомогою пакета аналізу у системі Microsoft Excel. Усі інші статистичні розрахунки проводили за допомогою програми SPSS 21.0. Достовірність різниці середніх між групами визначалася методом незалежного t-тесту для середніх. Порівняння динаміки показників на етапах лікування проводили за допомогою парного двовідбіркового t-тесту для середніх. Кореляційний аналіз проводили після визначення характеру розподілу за Spearman.
Результати
У табл. 1 подано характеристику груп на початку дослідження. Згідно з показниками, наведеними у табл. 1, обидві групи терапії достовірно не відрізнялися за основними клініко-демографічними характеристиками.
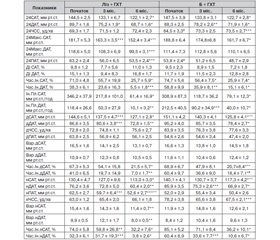
Ефективність терапії за даними офісного вимірювання АТ і ЧСС. Динаміку офісних АТ та ЧСС подано у табл. 2.
На фоні лікування відбулося однакове достовірне зниження офісних рівнів САТ/ДАТ як у групі «Ліз + ГХТ», так і в групі «Б + ГХТ» (44,5 ± 1,9/19,0 ± 2,1 мм рт.ст. та 42,4 ± 2,1/18,8 ± 2,5 мм рт.ст. у кожній групі відповідно, Р = НД для різниці між групами). Кількість пацієнтів, які досягли цільових цифр АТ (< 140/90 мм рт.ст.) на 1, 2, 3 та 6-му місяці становила 31,2; 53,1; 84,4 і 93,8 % у групі «Ліз + ГХТ» та 22,2; 48,1; 85,2 і 92,6 % — у групі «Б + ГХТ» відповідно (Р = НД для різниці між групами).
Пацієнти, рівень офісного АТ яких наприкінці дослідження був вищим за 140 та/або 90 мм рт.ст., були направлені на більш розширене обстеження щодо виключення вторинних причин резистентності гіпертензії, наявності резистентної гіпертензії, можливої корекції схеми лікування та підбору додаткових препаратів медикаментозної терапії. З цього приводу їх було залишено для подальшого спостереження у відділі симптоматичних гіпертензій.
Як у групі «Ліз + ГХТ» (84,4 %), так і у групі «Б + ГХТ» (74,1 %), більшість пацієнтів приймали амлодипін (Р = НД). Крім того, майже половині з них довелося збільшувати дозу доданого амлодипіну до 10 мг на добу — 59,4 та 59,3 % в кожній групі відповідно (Р = НД). Крім того, двом пацієнтам у групі «Ліз + ГХТ» та трьом пацієнтам у групі «Б + ГХТ» довелося додавати до обох схем лікування доксазозин (Р = НД).
Отже, призначене лікування було однаково ефективним щодо досягнення цільового рівня АТ в обох групах. У групі «Б + ГХТ» спостерігалося достовірне зниження ЧСС на 6-му місяці лікування (табл. 2) на відміну від групи «Ліз + ГХТ».
Ефективність терапії за даними амбулаторного моніторування. Динаміку середньодобових САТ, ДАТ і ЧСС наведено у табл. 2. Наприкінці дослідження в обох групах спостерігалося достовірне та значне зниження середньодобових САТ/ДАТ (P < 0,001).
Загальне зниження АТ протягом доби достовірно не відрізнялося у групі «Ліз + ГХТ» (24САТ/24ДАТ знизилися на 19,0 ± 3,3/19,3 ± 2,8 мм рт.ст.) та у групі «Б + ГХТ» (24САТ/24ДАТ знизилися на 24,1 ± 1,8/16,9 ± 1,2 мм рт.ст.; Р = НД для різниці між групами).
Як і слід було очікувати, у групі «Б + ГХТ» ми спостерігали значне зниження ЧСС протягом усіх 6 місяців періоду спостереження. В цей же час у групі «Ліз + + ГХТ» достовірного впливу на ЧСС та значної динаміки цього показника не спостерігалося.
Через 3 місяці лікування цільового рівня середньодобового АТ було досягнуто в 50 % пацієнтів у групі «Ліз + ГХТ» та у 51,9 % пацієнтів у групі «Б + ГХТ», а через 6 місяців терапії цей показник становив 71,4 та 66,7 % відповідно для обох груп (Р = НД).
Обидва режими терапії виявилися однаково ефективними у зниженні показників добових Час.Ін. та Ін.Пл., а також середніх САТ/ДАТ у денний та нічний час. Останнє є особливо позитивним, адже в нашому дослідженні препарати призначали 1 раз на добу, і підтвердилося, що вони забезпечують 24-годинний контроль АТ.
Оцінка жорсткості артерій та динаміки центрального АТ. Показники цСАТ та пружно-еластичних властивостей артерій наведено у табл. 4. У групі комбінації «Ліз + ГХТ» зниження цСАТ було достовірно більшим, ніж у групі комбінації бісопрололу (25,9 ± 2,9 мм рт.ст. проти 15,4 ± 2,9 мм рт.ст. відповідно; Р < 0,05 для різниці ступеня зниження цСАТ між групами). ED достовірно (Р < 0,05) зросла у групі «Б + ГХТ» від 32,2 ± 1,3 % до 36,7 ± 1,3 %, оскільки бісопролол збільшує тривалість систоли, внаслідок чого збільшується і час викиду. У групі комбінації іАПФ індекс ED достовірно не змінився — від 37,6 ± 3,6 % до 35,2 ± 2,4 %, тобто як такої динаміки зміни часу викиду у цій групі не спостерігалось, оскільки жоден препарат комбінації прямо не впливає на провідну систему серця.
Цікавою знахідкою було достовірне збільшення індексу SEVR у групі «Ліз + ГХТ» (зростання на 22,8 ± 5,6 % порівняно з початковим; Р < 0,05), в той час як у групі комбінації «Б + ГХТ» динаміки цього показника майже не спостерігалося. Збільшення індексу SEVR говорить про підвищення гемодинамічної ефективності діастоли, завдяки чому збільшується коронарний кровотік і кровопостачання самого міокарда. Це дуже корисний ефект, особливо у пацієнтів з АГ, в яких, як правило, вже є гіпертрофія лівого шлуночка. Гіпертрофований міокард, особливо в умовах неефективної гемодинаміки, перебуває в умовах хронічної гіпоксії. Тому доцільно застосовувати препарати, що мають здатність підвищувати індекс SEVR, тобто покращувати гемодинамічну ефективність діастоли не лише через подовження її тривалості, а й унаслідок збільшення «площі під кривою» тиску в діастолу, і відтворювати співвідношення «потреба — доставка» крові та перфузію міокарда. Отже, шляхом покращення коронарного кровотоку в діастолу можливо зменшити негативний наслідок хронічної гіпоксії міокарда і прогресування подальшого ремоделювання серця та розвиток ішемічної хвороби серця.
У групі «Б + ГХТ» відбулося достовірне збільшення індексу аугментації (з 19,7 ± 1,7 % до 24,6 ± 1,5 %; Р < 0,05), із чим, напевно, пов’язаний менший ступінь зниження цСАТ у цій групі, адже у групі «Ліз + ГХТ», де ми спостерігали найбільше зниження цСАТ, цей показник достовірно не змінився, хоча і була деяка тенденція до його зниження (табл. 4).
ШППХе та ШППХм суттєво не змінилися в обох групах. Можливо, це пов’язано з нетривалим періодом спостереження (6 місяців). Проте, коли ми порівняли ступінь зміни ШППХе, то виявили, що у групі «Ліз + ГХТ» ШППХе знизилася на 1,20 ± 0,08 м/с, тоді як у групі «Б + ГХТ» — знизилася на 0,63 ± 0,09 м/с, проте різниця динаміки ШППХе між групами виявилася достовірною (Р < 0,001). Крім того, у групі «Ліз + ГХТ» спостерігалася тенденція до зниження ШППХм, у той час як у групі «Б + ГХТ» — тенденція до зростання цього показника, а тому різниця між групами за ступенем впливу на ШППХм виявилася достовірною (Р < 0,001). Це говорить про те, що терапія комбінацією «Ліз + ГХТ» достовірно краще впливає на зменшення жорсткості артерій, ніж «Б + ГХТ».
Вплив терапії на біохімічні показники та рівень креатиніну сироватки крові. На початку лікування між групами не було виявлено достовірної різниці між вихідними параметрами, що вивчалися. Крім того, зовсім не було відмічено негативної динаміки показників біохімічного дослідження крові.
Спостерігалося достовірне зниження рівня креатиніну на 6-му місяці лікування у групі «Ліз + ГХТ» (від 88,9 ± 3,7 мкмоль/л до 74,7 ± 3,8 мкмоль/л; Р < 0,05), у той час як у групі комбінації бісопрололу цей показник знизився менше і недостовірно (від 88,6 ± 3,2 мкмоль/л до 83,3 ± 2,5 мкмоль/л). Оцінивши динаміку ШКФ за формулою СKD-EPI, ми не виявили достовірного впливу жодної досліджуваної комбінації на цей показник. Отже, наше дослідження підтвердило, що обидві комбінації були метаболічно нейтральні та що лізиноприл, як і інші іАПФ, має виражені нефропротекторні властивості, які не залежали від впливу на рівень АТ.
Оцінка прихильності та переносимості. Більшість пацієнтів у нашому дослідженні мали високу та помірну прихильність — 30 пацієнтів (93,8 %) у групі «Ліз + ГХТ» та 25 (92,6 %) — у групі «Б + ГХТ». Отримані дані дещо відрізняються від літературних [4], в яких було показано більш низьку прихильність до антигіпертензивної терапії, що частково можливо пояснити тим, що препарати видавали пацієнтам, всі учасники дослідження перебували під пильним наглядом лікарів.
Терапія добре переносилася, лише 11 (34,4 %) пацієнтів у групі «Ліз + ГХТ» сповістили про появу небажаних явищ: у 3 пацієнтів відмічався головний біль на першому місяці лікування, що було пов’язано більше з наявністю АГ; у 4 пацієнтів реєструвалися короткочасні епізоди запаморочення при зміні положення тулуба, що стали менш вираженими на 6-му місяці лікування; у 4 пацієнтів відмічалися незначні периферичні набряки також на 6-му місяці лікування. В той же час як у групі «Б + ГХТ» побічні ефекти спостерігали 12 (44,4 %) пацієнтів: у 4 пацієнтів відмічався головний біль на першому місяці лікування, що було пов’язано більше з підвищенням АТ; у 2 пацієнтів ЧСС зменшилася до < 50 уд/хв, що потребувало зменшення дози бісопрололу до 5 мг/добу; в 1 пацієнта на першому місяці прийому відмічалося відчуття похолодіння кінцівок, що значно зменшилося після додавання амлодипіну; у 3 пацієнтів відмічалися периферичні набряки на фоні прийому амлодипіну, що не призвели до відміни призначеного лікування. На 6-му місяці побічні реакції у даній групі були зареєстровані у 12 (44,4 %) пацієнтів: в одного пацієнта з’явилися набряки та ще в однієї пацієнтки почервоніння обличчя, що, скоріше, було пов’язано з прийомом амлодипіну.
Однак усі явища були класифіковані як м’які і не потребували відміни призначеної терапії або корекції дози препаратів.
Обговорення
Загалом нам вдалося отримати добру ефективність в обох групах терапії: як у групі комбінації іАПФ, так і в групі комбінації ББ спостерігалося достовірне і майже однакове зниження рівня АТ, виміряного на плечовій артерії в умовах клініки і за даними ДМАТ. Відомо, що обидва препарати (як лізиноприл, так і бісопролол) — високоефективні антигіпертензивні агенти з тривалим досвідом застосування в реальній практиці, ефективність впливу яких у нашому дослідженні була потенційована додаванням до обох препаратів ГХТ на початку дослідження, та амлодипіну і доксазозину під час титрації. Проте ступінь впливу препаратів на рівень цСАТ виявився різним, і терапія на підставі комбінації «Ліз + ГХТ» — більш ефективною в плані зниження АТ в аорті, що в подальшому може впливати на прогноз у таких пацієнтів, навіть при їх однаковому впливі на рівень брахіального АТ [10]. І це особливо важливо, оскільки в нашому дослідженні комбінація «Ліз + ГХТ» — вітчизняного виробництва, бюджетна за ціною та доступна в багатьох аптеках.
Окремо слід відзначити вплив досліджуваної терапії на концентрацію креатиніну. Загалом ми спостерігали зниження рівня креатиніну в обох групах, що і не дивно, оскільки зниження АТ саме по собі здатне покращувати функцію нирок, що ми і спостерігали у групі «Б + ГХТ», де зниження концентрації креатиніну відбувалося проградієнтно поряд із зниженням АТ протягом усього періоду спостереження. У групі «Ліз + ГХТ» відбулося більш виражене зниження рівня креатиніну при однаковому ступені зниження рівня АТ, виміряного на плечовій артерії, що, як ішлося раніше, може бути пов’язане з нефропротекторними властивостями лізиноприлу та, ймовірно, більшим зменшенням центрального АТ у групі іАПФ. Адже в деяких дослідженнях [7] показано, що функція нирок найбільше пов’язана з рівнем систолічного тиску в аорті. У нашому дослідженні ми зробили спробу визначити, чи пов’язане покращення функції нирок у цій групі з позитивною динамікою центрального АТ. Для цього ми зробили кореляційний аналіз за Spearman, щоб дослідити наявність та спрямованість взаємозв’язку між ступенем зниження цСАТ, оСАТ і креатиніну в цій групі. Але достовірного взаємозв’язку між динамікою цих показників ми не виявили. Тобто можна сказати, що зміна концентрації креатиніну, що була достовірною лише у групі комбінації з іАПФ, не була пов’язаною зі змінами рівня цСАТ, а, скоріше, з іншими нефропротекторними властивостями лізиноприлу. Це особливо важливо при лікуванні пацієнтів з АГ і супутнім ураженням нирок, адже в такому випадку непотрібно додатково призначати інші, більш дорогі препарати для лікування гіпертензивної нефропатії. У нашому дослідженні, крім прямого антигіпертензивного ефекту, ми отримали і додатковий нефропротекторний на фоні терапії препаратом вітчизняного виробництва, що свідчить про його значну ефективність та високу якість сировини.
Особливу увагу звертає на себе прихильність пацієнтів до лікування. Дійсно, терапія добре переносилася, адже у групі «Б + ГХТ» призначали брендовий препарат і якісний генеричний. Проте висока прихильність і низька частота побічних ефектів у групі «Ліз + ГХТ» дозволяють нам говорити про те, що препарати вітчизняного виробництва можуть бути вдалою альтернативою більш дорогим іноземним.
Прихильність пацієнтів до лікування — дуже важливий момент у веденні кардіологічних пацієнтів. Адже це забезпечує не лише короткочасний, видимий ефект, а й те, чого ми очікуємо від кардіологічної групи препаратів — тривалий вплив на прогноз, забезпечити який буде неможливо, якщо пацієнт із певних причин припинить прийом антигіпертензивної терапії. Призначення дієвих вітчизняних препаратів дозволяє нам ефективно покращувати прогноз, адже прихильність до них є дійсно високою. Крім того, такі ліки доступні навіть у найбільш віддалених куточках України, де асортимент аптечних мереж не такий широкий і наразі чимало препаратів закордонного виробництва починають зникати з полиць.
Отже, можна стверджувати, що обидва режими терапії високоефективні й добре переносяться, а тому можуть бути рекомендовані для лікування пацієнтів із помірною та тяжкою АГ. Проте терапія на підставі комбінації «Ліз + ГХТ» забезпечувала більший ступінь зменшення цСАТ та більш позитивний вплив на пружно-еластичні властивості артерій та функцію нирок.
Висновки
1. За даними офісного вимірювання АТ, лікування на основі комбінації «Ліз + ГХТ» було таке ж ефективне, як і лікування на основі комбінації «Б + ГХТ»: офісний САТ/ДАТ достовірно знизився від 171,3 ± 2,1/98,6 ± 1,0 до 128,7 ± 1,8/80,0 ± 1,4 мм рт.ст. у групі «Ліз + ГХТ» та від 172,4 ± 1,6/97,6 ± 1,3 мм рт.ст. до 131,2 ± 1,5/81,1 ± 1,7 мм рт.ст. у групі «Б + ГХТ», цільового рівня АТ було досягнуто у 93,8 та 92,6 % пацієнтів відповідно.
2. Середньодобові рівні САТ/ДАТ знизилися на 19,0 ± 3,3/19,3 ± 2,8 мм рт.ст. у групі «Ліз + ГХТ» та на 24,1 ± 1,8/16,9 ± 1,2 мм рт.ст. у групі «Б + ГХТ». Групи достовірно не відрізнялися за ступенем зниження денного та нічного АТ. Цільовий середньодобовий рівень АТ було досягнуто у 50 та 51,9 % (Р = НД) на 3-му місяці лікування, у 71,4 та 66,7 % хворих (Р = НД) — на 6-му місяці відповідно у групах «Ліз + ГХТ» та «Б + ГХТ». Антигіпертензивна ефективність обох комбінацій підтверджувалась достовірними та значними зниженнями індексів навантаження часом і площею.
3. З огляду на те, що будь-яке ефективне за даними вимірювання АТ на плечовій артерії лікування АГ супроводжувалося достовірним зниженням цСАТ при однаковому зниженні АТ на плечовій артерії, терапія на підставі комбінації «Ліз + ГХТ» забезпечувала достовірно більший ступінь зниження цСАТ (25,9 ± 2,4 мм рт.ст. проти 15,4 ± 2,9 мм рт.ст., Р < 0,05) та досягнення меншого рівня цСАТ, ніж терапія на базі комбінації «Б + ГХТ».
4. Не спостерігалося негативного впливу обох комбінацій антигіпертензивних препаратів на показники біохімічного дослідження крові, а рівень креатиніну достовірно зменшувався лише у групі «Ліз + ГХТ» від 88,9 ± 3,7 мкмоль/л до 74,7 ± 3,8 мкмоль/л (Р < 0,05) на 6-му місяці спостереження. При цьому достовірне зниження концентрації креатиніну не було пов’язане з більш вираженим зниженням цСАТ у цій групі.
5. Терапія на підставі комбінації «Ліз + ГХТ» достовірно не впливала на середні величини показників, що характеризують пружно-еластичні властивості артерій, тоді як комбінація «Б + ГХТ» достовірно збільшувала АІх. На фоні лікування комбінацією «Ліз + ГХТ» ступінь зменшення ШППХe, ШППХм та АІх був достовірно більшим, ніж на фоні лікування комбінацією «Б + ГХТ».
6. Призначене хворим лікування добре переносилось, що характеризувалося відносно невеликою кількістю виникнення м’яких побічних реакцій, які не потребували відміни препаратів, лише у 34,4 % пацієнтів у групі «Ліз + ГХТ» та у 44,4 % пацієнтів у групі «Б + ГХТ». Обидві схеми комбінованого лікування характеризувалися високою прихильністю.
1. Наказ МОЗ України № 384 від 24.05.2012. «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при артеріальній гіпертензії».
2. Practice guidelines for the management of arterial hypertension of the European Society of Hypertension (ESH) and the European Society of Cardiology (ESC): ESH/ESC Task Force for the Management of Arterial Hypertension // J. Hypertens. — 2013. — Vol. 31(10). — P. 1925–1938.
3. Black H.R. The paradigm has shifted to systolic blood pressure // J. Hum. Hypertens. — 2004. — Vol. 18 (Suppl 2). — S3–7.
4. Bloom B.S. Daily regimen and compliance with treatment // BMJ. — 2001. — Vol. 323(7314). — P. 647.
5. Cağlar N., Dincer I. Comparison between nebivolol and ramipril in patients with hypertension and left ventricular hypertrophy: a randomized open blinded end-point (PROBE) trial. // Eur. Rev. Med. Pharmacol. Sci. — 2011. — Vol. 12. — P. 1359–1368.
6. Dahlof B., Sever P.S., Poulter N.R. et al. ASCOT Investigators. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial // Lancet. — 2005. — Vol. 366(9489). — P. 895–906.
7. Hashimoto J. Central hemodynamics and target organ damage in hypertension // Tohoku J. Exp. Med. — 2014. — Vol. 233(1). — P. 1–8.
8. Kjeldsen S.E., Lyle P.A., Kizer J.R. et al. LIFE Study Group. The effects of losartan compared to atenolol on stroke in patients with isolated systolic hypertension and left ventricular hypertrophy. The LIFE study // J. Clin. Hypertens (Greenwich). — 2005. — Vol. 3. — P. 152–158.
9. Levey A., Stevens L., Schmid C. et al. CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration). A new equation to estimate glomerular filtration rate // Ann. Intern. Med. — 2009. — Vol. 150(9). — P. 604–612.
10. Nakamura M., Sato K., Nagano M. Estimation of aortic systolic blood pressure in community-based screening: the relationship between clinical characteristics and peripheral to central blood pressure differences // J. Hum. Hypertens. — 2005. — Vol. 3. — P. 251–253.
11. Redon J., Trenkwalder P.R., Barrios V. Efficacy of combination therapy with angiotensin-converting enzyme inhibitor and calcium channel blocker in hypertension // Expert. Opin. Pharmacother. — 2013. — Vol. 2. — P. 155–164.
12. Schliep H.J., Harting J. Beta 1-selectivity of bisoprolol, a new beta-adrenoceptor antagonist, in anesthetized dogs and guinea pigs // J. Cardiovasc. Pharmacol. — 1984. — Vol. 6. — P. 1156–1160.
13. White W. Blood pressure monitoring in Cardiovascular Medicine and Therapeutic. — N. Jersy: Humana Press, 2001. — P. 308.
14. Wikstrand J., Wedel H., Castagno D. The large-scale placebo-controlled beta-blocker studies in systolic heart failure revisited: results from CIBIS-II, COPERNICUS and SENIORS-SHF compared with stratified subsets from MERIT-HF // J. Intern. Med. — 2014. — Vol. 2. — P. 134–143.
15. Wilkinson I.B., Hall I.R., MacCallum H. et al. Pulse-wave analysis: clinical evaluation of a noninvasive, widely applicable method for assessing endothelialfunction // Arterioscler. Thromb. Vasc. Biol. — 2002. — Vol. 1. — P. 147–152.
16. Wu M.T., Douglas A.W., Ondeyka D.L. et al. Synthesis ofN2-[(S)-1-carboxy-3-phenylpropyl]-L-lysyl-L-proline (lisinopril) // J. Pharm. Sci. — 1985. — Vol. 3. — P. 352–354 .

/62/62.jpg)
/63/63.jpg)
/64/64.jpg)
/65/65.jpg)
/66/66.jpg)