Журнал «Здоровье ребенка» 7 (58) 2014
Вернуться к номеру
Вірусні діареї у дітей: клінічні прояви, інновації в лікуванні
Авторы: Крамарьов С.О., Виговська О.В., Палатна Л.О., Євтушенко В.В., Марков А.І. - Національний медичний університет імені О.О. Богомольця, м. Київ; Євтушенко О.М., Дзюба О.Л. - Київська міська дитяча клінічна лікарня № 2
Рубрики: Инфекционные заболевания, Педиатрия/Неонатология
Версия для печати
Проведений літературний пошук із вивчення клінічних особливостей вірусних діарей у дітей залежно від збудника. Обстежено 1484 дитини з гострою кишковою інфекцією (ГКІ), які знаходились на стаціонарному лікуванні в інфекційному відділенні Київської міської дитячої клінічної лікарні № 2 у 2013 р. Встановлено, що серед пацієнтів із ГКІ із ротавірусною інфекцією було 25,9 % хворих, ГКІ нез’ясованої етіології — 56 %, сальмонельозом — 8 %, шигельозом — 0,1 %, ГКІ іншої етіології — 10 %. Проведений літературний пошук показав ефективність використання пробіотиків, що містять різноманітні штами, для лікування ГКІ, яка проявилася скороченням інтоксикаційного синдрому, діареї, лихоманки на 2–3 дні. Показано, що використання пробіотика Субалін, що містить культуру Bacillus subtilis 2335/105, у лікуванні вірусних діарей у дітей у сучасних умовах як етіопатогенетичної терапії є перспективним.
Проведен литературный поиск по изучению клинических особенностей вирусных диарей у детей в зависимости от возбудителя. Обследовано 1484 ребенка с острой кишечной инфекцией (ОКИ), которые находились на стационарном лечении в инфекционном отделении Киевской городской детской клинической больницы № 2 в 2013 г. Установлено, что среди пациентов с ОКИ с ротавирусной инфекцией было 25,9 % больных, ОКИ невыясненной этиологии — 56 %, сальмонеллезом — 8 %, шигеллезом — 0,1 %, ОКИ другой этиологии — 10 %. Проведенный литературный поиск показал эффективность использования пробиотиков, содержащих различные штаммы, для лечения ОКИ, которая проявилась сокращением интоксикационного синдрома, диареи, лихорадки на 2–3 дня. Показано, что использование пробиотика Субалина, содержащего культуру Bacillus subtilis 2335/105, в лечении вирусных диарей у детей в современных условиях в качестве этиопатогенетической терапии является перспективным.
A literature search on the study of the clinical features of viral diarrhea in children has been carried out depending on the pathogen. 1,484 children with acute enteric infections (AEI) were examined, they underwent inpatient treatment in infectious disease department of Kyiv city children’s clinical hospital № 2 in 2013. It was found that among patients with AEI, 25.9 % had rotavirus infection, 56 % — AEI of uncertain aetiology, 8 % — salmonellosis, 0.1 % — shigellosis, 10 % — AEI with other origin. A literature search showed the effectiveness of the use of probiotics, containing different strains, for AEI treatment, which manifested with reduction of intoxication syndrome, diarrhea, fever by 2–3 days. It is shown that the use of probiotic Subalin, containing Bacillus subtilis strain 2335/105, is promising as etiopathogenetic therapy in the treatment of viral diarrhea in children under current conditions.
діти, вірусні діареї, пробіотики, Субалін, Bacillus subtilis.
дети, вирусные диареи, пробиотики, Субалин, Bacillus subtilis.
children, viral diarrhea, probiotics, Subalin, Bacillus subtilis.
Статья опубликована на с. 49-55
За даними ВООЗ та Дитячого фонду ООН (ЮНІСЕФ), у світі щорічно реєструється від 68,4 до 275 млн діарейних захворювань, близько 1,5 млн дітей віком до 5 років помирають у результаті зневоднення, пов’язаного з гострою інфекційною діареєю [1]. Діарейні захворювання — третя найбільш часта причина смертності серед дітей молодше 5 років у світі після перинатальних захворювань і захворювань респіраторного тракту [2]. Частота захворюваності та ризик смертності від діареї найвищі серед дітей віком до 1 року. В Україні щорічно реєструється 50–60 тисяч випадків гострих інфекційних діарей у дітей, які у 20–30 з них закінчуються летально [3].
Найчастішими збудниками гострих кишкових інфекцій (ГКІ) у дітей є віруси [1, 2]. Вірусна діарея — група гострих кишкових інфекцій, що спричинюється різними вірусами, характеризується симптомами інтоксикації, ураженням шлунково-кишкового тракту (ШКТ) у вигляді гастроентериту, ентериту, рідше гастриту, ентероколіту та в ряді випадків також перебігає з ураженням дихальних шляхів [1, 3].
Основними етіологічними факторами вірусних діарей є ротавіруси, каліцивіруси (норовіруси і саповіруси), аденовіруси, астровіруси, коронавіруси, торовіруси, ентеровіруси, цитомегаловіруси, реовіруси, бокавіруси, пестивіруси, пікорнавіруси, агент Аuru, пареховіруси та ін. [1, 2].
Вірусні діареї характеризуються гіперсекрецією клітин слизової оболонки кишечника чи зменшенням їх здатності до абсорбції без інвазивного пошкодження збудниками слизових оболонок. В основі патогенезу вірусних гастроентеритів лежить запальний процес, у який залучаються оболонки шлунка, тонкого кишечника, ушкоджується епітелій війок кишечника, на поверхні якого відбувається синтез дисахаридаз (лактази, мальтази, сукрази), недостатній їх синтез призводить до накопичення дисахаридів у порожнині кишечника, підвищення осмотичного тиску в кишечнику, що перешкоджає всмоктуванню води. Окрім цього, при вірусних діареях в ентероцитах знижується активність К-Nа-АТФази, унаслідок чого знижується транспортування натрію і глюкози в середину клітин кишечника, які, у свою чергу, є провідниками води [1, 3–5]. За рахунок запального процесу в подальшому розвивається порушення дисбалансу про- і протизапальних цитокінів, функції макрофагів, синтезу інтерферонів, клітинних і гуморальних реакцій імунного захисту [4]. Запальні процеси у слизовій оболонці кишечника, що виникають у процесі вірусних діарей, створюють передумови для зниження місцевого протиінфекційного імунного захисту [4].
Клініко-епідеміологічними особливостями вірусних діарей є: гострий початок зі швидкопрогресуючим токсико-ексикозом, швидке поширення у вогнищах, висока стійкість до факторів зовнішнього середовища, висока контагіозність, безсимптомне вірусоносійство і тривале виділення вірусів після клінічного одужання, можливість повітряно-краплинного механізму передачі інфекції, з водянистим характером випорожнень, відсутність запальних зсувів із боку аналізу крові і в копроцитограмі [1, 3].
Діагностика вірусних діарей базується на клініко-епідеміологічних даних. Для підтвердження діагнозу використовують вірусологічні, серологічні, молекулярно-генетичні методи. Для експрес-діагностики можна використовувати реакцію імунофлюоресценції та метод імунної електронної мікроскопії. Матеріалом для дослідження є фекалії, блювотні маси, сироватка крові, носоглотковий слиз. Виявлення сироваткових антитіл проводять за допомогою групоспецифічної реакції зв’язування комплементу і типоспецифічних реакцій гальмування гемаглютинації і нейтралізації. При постановці цих реакцій із парними сироватками, взятими в гострий період захворювання і в період реконвалесценції, діагностичне значення має наростання титрів антитіл не менше ніж у 4 рази. Також застосовують ІФА з груповим антигеном [3].
Лікування вірусних діарей є комплексним і включає регідратаційну, етіотропну, патогенетичну, симптоматичну та дієтотерапію [1, 2, 4, 6]. У цей час етіотропне лікування вірусних діарей залишається ще не до кінця вирішеною проблемою. Світова практика і власний досвід показують, що використання адекватної регідратаційної терапії, дієтотерапії, а за необхідності — антибактеріальної терапії майже завжди забезпечує одужання хворого [2, 3]. Разом із цим існує ряд препаратів, що можуть позитивно впливати на організм дитини під час хвороби, сприяти скороченню тривалості симптомів ГКІ, полегшенню стану хворого. Такими препаратами є пробіотики, які при вірусних діареях можуть виступати як самостійні засоби лікування [1, 4, 7].
Метою нашою роботи було: провести літературний пошук та виділити основні клінічні особливості вірусних діарей залежно від етіологічного фактора, згідно з літературними даними дослідити вплив пробіотика, що містить культури Bacillus subtilіs 2335/105 (Субаліну) на організм дітей.
Матеріал і методи
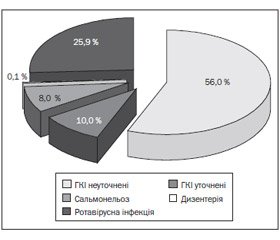
Під нашим спостереженням упродовж 2013 року перебували 1484 дитини, хворі на ГКІ. Серед госпіталізованих дітей у 56 % етіологію ГКІ не вдалося уточнити, у 25,9 % реєструвалася ротавірусна інфекція, у 8 % — сальмонельоз, в 0,1 % — шигельоз та в 10 % — ГКІ іншої етіології (рис. 1).
/50/50.jpg)
Результати та їх обговорення
Проведений літературний пошук вказує на те, що найчастішим збудником вірусних діарей є ротавіруси. Характерною для даного збудника є висока контагіозність, тропність вірусу до ентероцитів тонкого кишечника. Ротавіруси людини були відкриті в 1973 році австралійськими вченими R. Bishop, G. Barnes під час електронно-мікроскопічних досліджень ультратонких зрізів біоптатів дванадцятипалої кишки, отриманих від дітей, хворих на гострий гастроентерит. Родову назву ротавірус отримав через схожість вібріонів із маленькими колесами (rota — «колесо»). За антигенними властивостями ротавіруси розподіляють на 9 серотипів. Інші серотипи виділяють у тварин, вони є непатогенними для людини. Всі ротавіруси за наявності типоспецифічного антигену поділяються на 7 груп: А, B, C, D, E, F, G. Найбільш численна — група А, до неї належать більшість ротавірусів людини. Зараження людини може відбуватися також ротавірусами груп В та С. У людини захворювання викликають серотипи 1–4, 8, 9. Хворіють переважно діти віком від 3 місяців до 2 років. Наявність тріади симптомів (діарея, лихоманка, блювота) дозволила H. Champsaur et al. (1984) виділити DFV-синдром (diarrhea, febrile, vomit) як найбільш характерний прояв гострої ротавірусної інфекції. Ротавірусна діарея перебігає з синдромом ентериту, гастроентериту. У низці випадків у процес може залучатися товстий кишечник. Для ротавірусної діареї характерними є гострий початок захворювання, лихоманка, прояви загальної інтоксикації, часте поєднання катаральних проявів зі сторони верхніх дихальних шляхів та змін зі сторони ШКТ у вигляді гострого гастроентериту, ентериту (повторна блювота, метеоризм, біль у животі, часті водянисті випорожнення) [1–3]. У частини дітей розвиваються симптоми дегідратації легкого чи середнього ступеня вираженості. Важливою диференційно-діагностичною ознакою є наявність у частини хворих катаральних змін із боку верхніх дихальних шляхів: гіперемія і зернистість задньої стінки глотки, пирхота і біль у горлі, нежить, кашель. Ураження кишечника здатні викликати лише ентеральні аденовіруси. Зустрічаються аденовіруси з винятковою тропністю до епітелію ШКТ — підряду F, серотипів 40 і 41, що викликають кишкові форми захворювання. Кишкова форма зустрічається переважно в дітей перших 3 років життя і є причиною діарей у 7–8 % госпіталізованих дітей [1–3]. Для аденовірусної інфекції характерні поступовий початок захворювання з симптомів ураження носоглотки, ексудативний характер запалення, слабка або помірна інтоксикація та поліморфізм клінічних проявів у динаміці захворювання: симптоми ураження дихальних шляхів (риніт, ринофарингіт, тонзиліт, фарингіт, ларингіт, трахеїт, бронхіт), очей (кон’юнктивіт), лімфаденопатія, іноді екзантема, порушення з боку ШКТ, гепатолієнальний синдром, мезаденіт, хвилеподібний перебіг захворювання. Діарейний синдром проявляється нерізко вираженим і нетривалим ентеритом. У дітей старшого віку аденовірусна інфекція часто перебігає з мезаденітом, її викликають аденовіруси серотипів 12, 18, 31 із підроду А [3]. Реовіруси можуть мати переважну тропність до епітелію слизових оболонок дихальних шляхів або ШКТ. Унаслідок цього виділяють респіраторні і кишкові форми інфекції. За клінічною картиною реовірусний гастроентерит ідентичний ротавірусному, але з більш вираженими катаральними проявами (серозні виділення з носа, герпетична ангіна, гіперемія та зернистість задньої стінки глотки) [1–3]. Назва родини коронавірусів походить від латинського слова corona — «корона». Це пов’язано з тим, що навколо оболонки вірусу наявне виражене обрамлення, що нагадує зубці корони. До родини належать два роди — коронавірус та торовірус. Коронавірус уперше був виділений у 1965 р. На підставі генетичних і антигенних властивостей коронавіруси розподілені на три групи: 1-ша група — коронавірус людини 229Е і деяких тварин, 2-га група — коронавірус людини OG43, гепатиту гризунів, 3-тя група — кишкові коронавіруси людини й віруси бронхіту курей. Є коронавіруси з переважною тропністю як до епітелію верхніх дихальних шляхів, так і до епітелію ШКТ. Описані спалахи коронавірусної інфекції, що виявлялась лише симптомами ураження ШКТ, хвороба перебігала за типом гострого гастроентериту. З випорожнень хворих були виділені коронавіруси штамів HECоV-24 і HECоV-25. Під час спалаху SARS у 2003 р. у 21 % хворих відзначалися симптоми гострого гастроентериту. У дітей раннього віку основним симптомом захворювання є діарея з виділенням значної кількості води, прозорого слизу. У половини хворих паралельно з діареєю спостерігається блювота. У новонароджених і дітей перших 3 місяців життя коронавірусний гастроентерит може супроводжуватися явищами токсикоексикозу, а в деяких випадках захворювання може ускладнюватися некротичним ентероколітом і закінчитися летально [1, 2]. Назва «торовірус» походить від латинського слова torus — «тор», форму якого має нуклеокапсид представників цього роду. Вони були виявлені у 1994 р. та відіграють роль у розвитку діареї в дітей зі зниженим імунітетом при нозокоміальній інфекції. Всього описано 7 морфологічних і 4 серологічних типи. Торовіруси були виділені у 27–35 % пацієнтів із гострою діареєю, за даними інших авторів, — у 3 % випадків діарей [1]. Найбільш часто парвовірусна інфекція проявляється як інфекційна еритема («п’ята хвороба»). В основному хворіють діти шкільного віку (70 %). Контагіозний індекс становить 50 %. Збудником цього інфекційного захворювання є парвовірус В19 із родини Parvoviridae. Початок захворювання гострий. Лихоманка зустрічається в 30 % хворих. Скарги на слабкість, адинамію, нудоту, блювоту, у 50 % хворих зустрічаються рідкі випорожнення. Характерні переймоподібний біль у животі, гучне бурчання кишечника. Тривалість захворювання — до 3 діб [1].
Як причина розвитку вірусних діарей стали вже відомими каліцивіруси. Назва родини походить від латинського calix — «кубок», що нагадує заглиблення на поверхні вібріона, помітні під електронним мікроскопом. Родина включає норовіруси й саповіруси. Норовірусні й саповірусні діареї за частотою посідають 2–ге місце (14–17 %) після ротавірусних серед збудників ГКІ у людей. Норовірусна інфекція уражає всі вікові групи. У США причиною 1/3 випадків вірусних гастроентеритів у дітей віком від 6 до 24 місяців є норовіруси. У Європі за період з 1995 по 2000 рік норовірус став причиною більше ніж 85 % небактеріальних гастроентеритів [1]. Спочатку норовірус називався на честь місцевості Норфолк (штат Огайо, США), де в листопаді 1968 року був зареєстрований спалах гострого гастроентериту серед школярів однієї початкової школи. У 1972 році в результаті імуноелектронної мікроскопії консервованих проб фекалій був виявлений вірус, що отримав назву «вірус Норфолк». Клонування й секвенування його геному показало, що ці віруси мають таку ж організацію геному, як і віруси родини Саlісіvіrіdае. Назва «норовірус» була затверджена Міжнародним комітетом із таксономії вірусів у 2002 році. Норовіруси мають 5 геногруп (GІ, GII, GIII, GIV і GV). Геногрупи І, ІІ і IV викликають захворювання в людини, а геногрупа ІІІ — у великої рогатої худоби. Геногрупа V нещодавно була виявлена у мишей. Найбільш небезпечний норовірус для фізично ослаблених та літніх осіб, дітей раннього віку. Саповірус уражає також усі вікові групи, але частіше немовлят і дітей раннього віку. На його частку припадає близько 9 % від усіх вірусних діарей у дітей молодшого віку. Для норовірусного та саповірусного гастроентериту характерний гострий початок захворювання, клініка гастроентериту з переважанням повторної блювоти та меншою мірою водянистої діареї при нормальній або субфебрильній температурі [1, 2].
Астровіруси людини асоційовані з 2–8 % гострих небактеріальних гастроентеритів у дітей. Свою назву вони отримали від грецького слова astro — «зірка», яку нагадують вібріони при електронній мікроскопії. Близько 65 % дітей віком 3–4 роки і 87 % дітей 5–10 років мають антитіла до астровірусів. У клінічній картині характерні нечасті водянисті випорожнення, помірна блювота, біль у животі, лихоманка. Часто астровіруси зустрічаються в мікст-інфекціях із рота- й норовірусами [1].
Пікорнавіруси отримали свою назву від італійських слів piccolo — «маленький», rna — «РНК». Це дрібні РНК-вмісні віруси, що можуть викликати ураження ШКТ у людини. У розвитку вірусних діарей мають значення кобувіруси (від японського слова kobu — «горб», назва виникла у зв’язку з ікосаедричною симетрією вібріона), ентеровіруси. Рід кобувіруси (прототипний представник — вірус Auru) може бути причиною гастроентериту в людей. Серологічні дослідження, проведені в Японії, показали, що у 80 % обстежених віком до 35 років виявляють антитіла до цього вірусу [2].
Назва роду «ентеровірус» відображає важливе значення органів ШКТ у патогенезі захворювань, які спричиняють ці віруси. У людини прояви хвороби спричиняють три підгрупи ентеровірусів — поліовіруси, віруси Коксакі й ECHO. Назва вірусу Коксакі походить від назви району Нью-Йорка, де цей збудник уперше було відкрито. Назва ECHO — це абревіатура з англійських слів enteric cytopathic human orphan viruses. Протягом останніх років у світі спостерігається чітка тенденція до збільшення кількості випадків захворювань, що зумовлені ентеровірусами, епідеміологічно значимі підвищення захворюваності спостерігаються як у розвинутих країнах, так і у країнах, що розвиваються. Висока захворюваність обумовлена як значним прошарком у популяції неімунного до ентеровірусів контингенту населення, так і тривалим вірусоносійством (вірус може виділятися з організму людини до 5 місяців), що сприяє поширенню збудника серед осіб різних вікових груп. Ентеровірусні інфекції поширені в усіх регіонах планети. У країнах із помірним температурним кліматом щорічно пік захворюваності припадає на літо й початок осені. Ентеровіруси спричиняють до 33–65 % усіх захворювань із лихоманкою. До факторів ризику захворюваності та тяжкого перебігу інфекції зараховують ранній вік дитини, чоловічу стать, порушення правил гігієни, перенаселення житла, низький соціально-економічний статус. Ентеровірусні захворювання об’єднують велику групу гострих вірусних захворювань, що мають подібні патогенетичні механізми розвитку й характеризуються широким спектром клінічних проявів від безсимптомного перебігу до тяжких уражень нервової системи, внутрішніх органів. Спектр клінічних проявів ентеровірусної інфекції широкий: неспецифічна гарячка, екзантема, герпетична ангіна, полінейропатія, серозний менінгіт, міокардити, менінгоенцефаліти, сепсис, діарея та ін. В етіології гастроентеритів мають значення ентеровіруси –68–71–го типів, віруси ECHO 5, 7, 9, 11, 17, 18 та Коксакі 1, 2, 5. В основному на ентеровірусну діарею хворіють діти раннього віку. Ентеровірусна діарея характеризується груповою захворюваністю, клінічно проявляється нерізко вираженими синдромами інтоксикації та гастроентериту чи ентериту. Типове поєднання з гіперемією і зернистістю м’якого піднебіння й задньої стінки глотки, можливі герпетична ангіна та інші симптоми ураження верхніх дихальних шляхів. Нерідко реєструється лімфаденопатія, у частини хворих спостерігається коре-, чи краснухоподібна екзантема. Захворювання розпочинається гостро, з підвищення температури тіла, блювоти, появи частих рідких випорожнень. Частота випорожнень може досягати 10–15 разів на добу, випорожнення рідкі, жовті чи жовто–зелені, з домішками слизу, іноді пінисті. Живіт здутий, бурчить, іноді різко болючий при пальпації. Окрім гастроентериту, в більшості дітей спостерігаються запальні зміни верхніх дихальних шляхів — гіперемія слизової оболонки ротоглотки, гіперемія мигдаликів [2, 3].
Проведений аналіз етіологічної структури ГКІ у дітей, які були госпіталізовані до інфекційного відділення Київської міської дитячої клінічної лікарні (КМДКЛ), упродовж останніх 5 років (із 2009 по 2013 рік) показав, що щороку зростає питома вага ротавірусної інфекції у структурі ГКІ, на високих цифрах залишається захворюваність на ГКІ неуточненої етіології, зменшується відсоток дітей із бактеріальною діареєю (рис. 2).
/52/52.jpg)
ГКІ неуточненої етіології у 38,3 % випадків реєстрували у дітей віком 1–3 роки, у 37,5 % — 3–15 років, 22,9 % — 0–12 місяців, 1,3 % — 15–18 років. Серед дітей із ротавірусною інфекцією майже половина (49,5 %) були віком 1–3 роки, 28,4 % — віком 3–15 років, 21,9 % — діти першого року життя і лише 0,2 % становили підлітки.
Враховуючи те, що на відміну від ГКІ бактеріальної етіології для кишкових інфекцій, викликаних вірусами, у даний час не існує остаточно розробленого етіотропного лікування, багатьох лікарів хвилює питання пошуку альтернативних схем терапії вищезазначеної патології. Проведений літературний пошук свідчить про позитивний результат від застосування при вірусних діареях препаратів рекомбінантного інтерферону альфа-2, специфічних імуноглобулінів, індукторів інтерферонів. Все більше уваги у схемах лікування гострих кишкових інфекцій, у тому числі й вірусних діарей, приділяється групі пробіотиків.
Відповідно до визначення робочої групи ВООЗ, пробіотики — це живі мікроорганізми, що при використанні в адекватних кількостях викликають покращення стану здоров’я організму-господаря [12]. Вони сприяють нормалізації біоценозу кишечника, можуть виступати як антагоністи патогенних вірусів, бактерій за рахунок їх конкурентної дії [13–15].
Останнім часом усе більше уваги приділяється також імуномодулюючим властивостям деяких пробіотиків [4, 13, 15].
Більшість пробіотиків належить до роду біфідобактерій, лактобацил, деякі містять аеробні види — ентеро-, стрептококи, кишкові палички [7, 10]. Часто використовують небактеріальні пробіотики, що містять дріжджові грибки S.boulardii [7, 10].
На кафедрі дитячих інфекційних хвороб НМУ ім. О.О. Богомольця впродовж останніх десяти років накопичено великий досвід застосування пробіотиків у педіатрії та дитячій інфектології при різноманітній патології (ГКІ, антибіотикасоційовані діареї, інфекційний мононуклеоз, хронічна Епштейна — Барр вірусна інфекція, лікування та профілактика гострих респіраторно-вірусних інфекцій (ГРВІ)) [7–11]. У 2011 році в Київській міській дитячій клінічній лікарні № 2 на базі кафедри дитячих інфекційних хвороб НМУ ім. О.О. Богомольця проведене дослідження, що включало 63 дитини віком від 5 місяців до 6 років із ротавірусним гастроентеритом. Одній із груп окрім традиційної терапії призначались пробіотики, що дозволило прискорити нормалізацію випорожнень на 16–23 години [16].
З урахуванням попереднього досвіду, нашу особливу увагу привернув принципово новий пробіотик Субалін, що являє собою мікробну масу живої антагоністично активної культури Bacillus subtilіs 2335/105 (виробник ПрАТ «Біофарма», Україна) [17]. Специфічна активність Субаліну визначається кількістю життєздатних бактерій в одній дозі препарату та антагоністичною активністю. Одна доза препарату містить 1–8 • 109 живих мікробних клітин штаму В.subtilіs 2335/105 [17, 18]. Препарат має високу антагоністичну активність щодо тест-штамів патогенних та умовно-патогенних мікроорганізмів (Shigella sonnei, S.flexneri, Salmonella typhimurium, S.derby, S.greis, S.reading, S.stenly, S.weslaco, Staphylococcus aureus, Pseudomonas aeruginosa, Proteus vulgaris, Klebsiella pneumoniae), ентеропатогенних мікроорганізмів (Escherichia coli, Сandida albicans), C.tropicalis та сприяє нормалізації якісного та кількісного складу кишкової мікрофлори [17, 19]. Крім того, унікальною здатністю цього штаму є властивість самостійно виробляти альфа-інтерферон (α-ІФН), що особливо цікаво з точки зору перспективи лікування саме вірусних діарей. Здатність Субаліну до індукції ІФН вивчали в дослідах in vivo, in vitro та в дослідженнях на добровольцях і отримали дані, що Субалін при пероральному введенні продукує α2-ІФН людини [17, 19]. Проведені дослідження продемонстрували спроможність Субаліну позитивно впливати на показники неспецифічної резистентності організму [18–20]. Це свідчить про перспективність застосування препарату для лікування інфекцій ШКТ та інфекцій, що локалізуються поза ШКТ [19].
Проведені результати клінічних досліджень застосування препарату Субалін при різних захворюваннях (менінгоенцефалітах, вірусних гепатитах, ГКІ, дисбіозі кишечника, синдромі ендотоксикозу, ГРВІ в пацієнтів, які часто і тривало хворіють, вірусних і бактеріальних інфекціях), в офтальмології, в отоларингології, дані бактеріологічних і клінічних аналізів свідчать про достатню ефективність препарату при вищезазначеній патології, а також про відсутність побічних явищ та ускладнень, пов’язаних із прийомом препарату, у тому числі в осіб з обтяженим алергологічним анамнезом [4, 21–24].
Встановлено, що культура, яка входить до складу препарату, не персистує тривалий час в організмі, і, ймовірно, з цим пов’язане швидке зниження рівня ІФН у крові після закінчення прийому препарату, що є важливим, оскільки можна регулювати кількість інтерферону в організмі призначенням певних доз і курсів введення Субаліну [18]. При цьому застосування препарату при різних патологіях та у здорових добровольців не призводить до вироблення антитіл до інтерферону, що додатково свідчить про безпечність препарату [4, 18, 20].
Пробіотик Субалін належить до групи антагоністів, що здатні до самоелімінації. Дані антагоністичні бактерії є стійкими до літичних і травних ферментів, зберігають життєздатність уздовж усього ШКТ. Завдяки антибіотикорезистентності пробіотичного штаму B.subtilіs 2335/105 Субалін може успішно комбінуватися з антибіотиками в разі виникнення вторинних бактеріальних ускладнень на фоні вірусних інфекцій та при бактеріальних інфекціях із першого дня антибіотикотерапії [18].
Під час узагальнення проведених клінічних досліджень із вивчення ефективності і безпечності Субаліну при різних захворюваннях встановлено його переваги: здатність самостійно синтезувати α2-ІФН, виробляти понад 70 антибіотикоподібних речовин та ферментів, що викликають загибель патогенних мікроорганізмів, закислювати середовище і тим самим створювати несприятливі умови для життя патогенних мікроорганізмів, стійкість до впливу антибіотиків і шлункового соку, здатність підсилювати клітинний і гуморальний імунітет, підвищувати стійкість організму до захворювань різної етіології [18, 21–24].
З огляду на все вищезазначене, на кафедрі дитячих інфекційних хвороб НМУ ім. О.О. Богомольця проводиться робота з вивчення ефективності й безпечності Субаліну при вірусних діареях у дітей (зокрема, при ротавірусній інфекції). У зв’язку з незавершеністю роботи, в цій статті ми не викладаємо отримані результати. Але попередні дані свідчать про перспективність застосування Субаліну при вірусних діареях. Для отримання ефекту при лікуванні вірусних діарей у дітей Субалін рекомендовано приймати по 1 дозі 2–3 рази на добу впродовж 5–10 днів. Цікаво, що препарат не має вікових обмежень та протипоказань для призначення.
Клінічний приклад. Хворий С., 1 року, був госпіталізований 10.04.2014 р. до КМДКЛ зі скаргами матері хворого на високу температуру тіла — до 39,6 °C, нежить із незначними серозними виділеннями, утруднене носове дихання, водянисті випорожнення, збільшення лімфатичних вузлів у ділянці шиї, гіперемію кон’юнктив. Анамнез хвороби: захворів гостро вночі з 09.04 на 10.04 2014 року, коли вперше підвищилася температура тіла до 38,7 °C. Була викликана швидка медична допомога (ШМД). Лікар ШМД установив діагноз ГРВІ, зробив ін’єкцію літичної суміші. Вдома мати самостійно давала дитині генферон, панадол, нурофен. Температура знизилася до 37,2 °C. 10.04.2014 р. температура знову підвищилася до 39,6 °C, з’явилися нежить, кон’юнктивіт, часті водянисті випорожнення, у зв’язку з чим мати повторно викликала ШМД. Дитину разом із матір’ю госпіталізували в КМДКЛ. Під час надходження до стаціонару був установлений діагноз: ГРВІ: гострий ринофарингіт, двобічний фолікулярний кон’юнктивіт, синдром діареї середнього ступеня тяжкості, аденовірусна інфекція? Призначено лікування: смекта, регідрон, Субалін по 1 дозі 2 рази на день упродовж 7 днів, інфузійна терапія глюкозо-сольовими розчинами, жарознижуючі, обробка слизової ротоглотки хлорофіліптом, в очі — софрадекс, у ніс — сольовий розчин. Епідеміологічний анамнез: виявити джерело інфекції не вдалося. Анамнез життя: народився від 2-ї вагітності, 2-х пологів. Антенатальний період без особливостей. Вагітність перебігала благополучно. Розродження в термін 38 тижнів (плановий кесарів розтин). При народженні: зріст 45 см, вага 3600 г. Пологи без ускладнень. На грудному вигодовуванні знаходився близько 2 місяців, з причини розвитку маститу в матері з 3 місяців — штучне харчування. У даний час дитина вживає фрукти, овочеві страви, крупи. Вага дитини 9600 г. Прорізалося 4 зуби. Добре тримав голову в 3 міс., навчився сидіти в 6 міс., повзати — у 8 міс., стояти — у 10 міс., у 12 міс. — ходити. Зі слів матері, у родині хронічних захворювань немає. Побутові умови хороші. Живуть у квартирі. З перенесених захворювань — ГРВІ у 8 міс., лікувався амбулаторно. Щеплений за віком. Алергічний анамнез не обтяжений. Стан хворого на момент огляду: загальний стан середньої тяжкості. Свідомість ясна. Статура правильна, харчування хороше, відхилень у рості та фізичному розвитку немає. Підшкірна клітковина розвинена помірно. Лімфовузли доступні пальпації, збільшені з двох сторін: пахові, підщелепні, передньошийні в діаметрі до 1,5 см, щільні, болісні, не спаяні один з одним і з оточуючими тканинами. Шкіра чиста, бліда. Температура тіла 37,6 °C. Слизова оболонка порожнини рота волога, зів гіперемований. Піднебінні мигдалини гіперемовані, без нальотів. Задня стінка глотки гіперемована, набрякла. Тургор тканин і вологість задовільні. Кон’юнктиви з двох сторін гіперемовані, набряклі, збільшенні фолікули, виділення відсутні. Патології з боку кістково-м’язово-суглобового апарату не виявлено. Дихання через ніс утруднене внаслідок його закладеності. У носі — невелика кількість безбарвного слизового виділення. Задишка відсутня. Грудна клітка нормостенічного типу, активно бере участь в акті дихання. Частота дихальних рухів — 30 за 1 хв. Дихання ритмічне. При аускультації дихання везикулярне, патологічних хрипів та шуму тертя плеври немає. Верхівковий поштовх визначається у 4-му міжребер’ї на 1 см всередину від лівої середньоключичної лінії. Пульс 140 уд. за 1 хв, ритмічний, задовільного наповнення і напруження. Тони серця ясні, ритмічні. Живіт звичайної форми, обидві його половини однаково беруть участь в акті дихання. При пальпації живіт здутий, болючий у правій здухвинній ділянці. Нижній край печінки визначається по правій середньоключичній лінії на 3 см нижче від краю реберної дуги. При пальпації край печінки еластичний, гладкий, безболісний. Селезінка на 1,5 см виступає з-під краю реберної дуги. Напруження передньої черевної стінки відсутнє. Перитонеальні симптоми відсутні. Випорожнення 5–7 разів на день, із невеликою кількістю слизу, жовто-зеленого кольору, водянисті. Сечовипускання безболісне, 6 разів на добу. Сеча світло-жовтого кольору. Болі в поперековій ділянці відсутні. Менінгеальні симптоми й вогнищева неврологічна симптоматика відсутні.
Дані лабораторних, інструментальних та спеціальних методів дослідження: загальний аналіз крові від 11.04.2014 р.: еритроцити — 3,94 • 1012/л, гемоглобін — 124 г/л, колірний показник — 0,91, швидкість осідання еритроцитів — 3 мм/год, лейкоцити — 2,8 • 109/л, моноцити — 8 %, лімфоцити — 62 %, сегментоядерні — 25 %, паличкоядерні — 5 %. У змиві з носоглотки від 11.04.2014 р. виділений антиген аденовірусу.
Динамічне спостереження за хворим: 17.04.2014 р. температура тіла — 37,6 °C, пульс — 140 уд. за 1 хв, скарги відсутні. Загальний стан задовільний, свідомість ясна. Дитина активна. Шкіра рожева, чиста, нормальної вологості. Лімфовузли не збільшені. Слизова порожнини рота волога, зів рожевий, мигдалики не збільшені, звичайного кольору. Язик не обкладений. Задня стінка глотки звичайного кольору. Кон’юнктива з двох сторін звичайного кольору. Виділень з очей немає. Над легенями везикулярне дихання. Тони серця ритмічні, звучні. Живіт м’який, безболісний у всіх відділах. Печінка на 1 см виступає з-під краю реберної дуги. Селезінка не пальпується. Симптоми подразнення очеревини негативні. Випорожнення 2 рази на добу, звичайної консистенції і звичайного кольору, без патологічних домішок. Сечовипускання безболісне, 5 разів на день. Менінгеальні й загальномозкові симптоми відсутні. У задовільному стані був виписаний додому під нагляд лікаря.
Висновки
1. На вірусні діареї на даний час припадає велика частка у структурі етіологічних факторів ГКІ у дітей. При цьому серед збудників домінує ротавірусна інфекція.
2. Особливостями вірусних діарей у більшості випадків є поєднання водянистої діареї із симптомами ураження верхніх дихальних шляхів.
3. Доведена ефективність пробіотиків у комплексному лікуванні ГКІ: відмічено зниження тривалості лихоманки, інтоксикаційного синдрому та діареї на 2–3 дні.
4. Застосування пробіотика Субалін для лікування вірусних діарей у дітей є перспективним напрямком сучасної етіотропної і патогенетичної терапії вірусних діарей у дітей.
1. Малий В.П., Романцов М.Г. Вірусні діареї / В.П. Малий, М.Г. Романцов // Інфекційні хвороби. — 2013. — № 4. — С. 5–16.
2. Вирусные диареи у детей: особенности клинической картины, диагностика, современные подходы к терапии / С.А. Крамарев, О.В. Выговская, Л.А. Большакова [и др.] // Дитячий лікар. — 2014. — № 3–4 (32–33). — С. 3–10.
3. Інфекційні хвороби в дітей: Підручник / С.О. Крамарьова, О.Б. Надрага, Л.В. Пипа [та ін.] / За ред. проф. С.О. Крамарьова, О.Б. Надраги. — К.: ВСВ «Медицина», 2010. — 392 с.
4. Патогенетичне обґрунтування оптимізації лікування вірусних діарей у дітей за допомогою спороутворювальних бацил, здатних до самоелімінації / О.К. Колоскова, Т.М. Білоус, М.Н. Гарас // Актуальна інфектологія. — 2014. — № 3 (4). — С. 185–188.
5. Mucosal flora in inflammatory bowel disease / А. Swidsinski, А. Ladhoff, А. Pemthaler [et al.] // Gastroenterology. — 2002. — 122. — 44–54.
6. Тихомирова О.В. Вирусные диареи у детей: особенности клинического течения и тактика терапии / О.В. Тихомирова // Детские инфекции. — 2003. — № 3. — С. 7–10.
7. Двойные слепые плацебо-контролируемые исследования по изучению эффективности мультипробиотика Симбитер в профилактике ОРВИ у детей, проживающих в доме ребенка / С.А. Крамарев, В.В. Бережной, О.В. Выговская [и др.] // Здоровье женщины. — 2010. — № 6. — С. 149–154.
8. Крамарєв С.О., Виговська О.В., Палатна Л.А. Ефективність застосування мультипробіотиків групи Симбітер у комплексному лікуванні хронічної активної форми Епштейна — Барр вірусної інфекції у дітей / С.О. Крамарєв, О.В. Виговська, Л.А. Палатна // Современная педиатрия. — 2008. — № 1. — С. 140–145.
9. Крамарєв С.О., Янковский Д.С., Дымент Г.С. Антибиотико-ассоциированные диареи у детей с инфекционными заболеваниями и возможности их профилактики / С.А. Крамарєв, Д.С. Янковский, Г.С. Дымент // Современная педиатрия. — 2007. — № 4. — С. 157–161.
10. Современные подходы к лечению острой кишечной инфекции у детей / Л.В. Закордонец, С.А. Крамарев, Т.В. Береговая [и др.] // Здоровье ребенка. — 2013. — № 5(48). — С. 107–111.
11. Крамарев С.А., Выговская О.В., Тарадий Н.Н. Влияние мультипробиотика на показатели иммунитета при Эпштейна — Барр вирусной инфекции у детей / С.А. Крамарев, О.В. Выговская, Н.Н. Тарадий // Здоровье ребенка. — 2014. — № 1(52). — С. 164–169.
12. Пробиотики и пребиотики. Всемирная гастроэнтерологическая организация (практические рекомендации). — 2008. — 24 с.
13. Clinicalevidence of immunomodulatory effects of probioticbacteria / F.M. Ruemmelle, D. Bier, P. Marteau [et al.] // J. Pediatr. Gastroenterol. Nutr. — 2009. — 48(2). — 126–41.
14. Resta-Lenert S., Barrett K.E. Live probiotics protect intestinal epithelial cells from the effects of infection with enteroinvasive Esche–richia coli (EIEC) / S. Resta-Lenert, K.E. Barrett // Gut. — 2003. — 52. — 988–97.
15. Янковский Д.С., Дымент Г.С. Микрофлора и здоровье человека. — К.: ТОВ «Червона Рута–Турс», 2008. — 552 с.
16. Ефективність пробіотичних препаратів при лікуванні ротавірусного гастроентериту у дітей / С.О. Крамарев, В.В. Євтушенко, О.В. Корбут [та ін.] // Проблеми військової охорони здоров’я: збірник наукових праць Української військово-медичної академії. — 2014. — Вип. 42, Т. 2. — С. 187–194.
17. Теоретичне обґрунтування і практика застосування бактерій роду Bacillus для конструювання нових пробіотиків: Автореф. дис… д-ра біол. наук: 03.00.07 / І.Б. Сорокулова; НАН України. Ін-т мікробіології і вірусології ім. Д.К. Заболотного. — К., 1999. — 36 с.
18. Субалин: принципиально новый поход к лечению бактериальных и вирусных инфекций / И.Б. Сорокулова, С.Л. Рыбалко, А.А. Руденко [и др.]. — К., 2013. — 36 с.
19. Пробиотик субалин — принципиально новый поход к лечению бактериальных и вирусных инфекций / И.Б. Сорокулова, С.Л. Рыбалко, А.А. Руденко [и др.]. — К.: ДИА, 2007. — 36 с.
20. Соцька Я.А. Вплив комбінації лаферобіону та субаліну на фагоцитарну активність моноцитів у хворих на хронічний вірусний гепатит С низького ступеня активності / Я.А. Соцька // Укр. мед. альманах. — 2010. — Т. 13, № 6. — С. 143–146.
21. Єршова І.Б. Особливості кишкового мікробіоценозу при вірусних гепатитах і можливості його корекції / І.Б. Єршова // Актуальна інфектологія. — 2014. — № 2 (3) — С. 97–103.
22. Лупырь А.В. Возможности применения бактериальных иммуномодуляторов при полипозном риносинусите / А.В. Лупырь // Международный медицинский журнал. — 2011. — № 1. — С. 63–68.
23. Псахис И.Б. Современные возможности и перспективы использования прбиотиков группы самоэлиминирующихся антагонистов в терапии инфекционных заболеваний / И.Б. Псахис, Т.Е. Маковская // Здоровье ребенка. — 2014. — № 4 (55). — С. 132–136.
24. Сакович В.Н., Аль-Кайяли Фади З.И. Изучение эффективности применения пробиотика Субалина в комплексном лечении больных передними увеитами / В.Н. Сакович, З.И. Аль-Кайяли Фади // Офтальмология. Восточная Европа. — 2013. — № 2 (17). — С. 137–143.