Журнал «Здоровье ребенка» 6 (57) 2014
Вернуться к номеру
Особливості диспансерного нагляду за надзвичайно недоношеними дітьми
Авторы: Яблонь О.С., Власенко Д.Ю. - Вінницький національний медичний університет імені М.І. Пирогова;
Сергета Д.П., Берцун К.Т., Харчук О.В. - Вінницька обласна дитяча клінічна лікарня; Шовкопляс Н.А. - Вінницька міська клінічна лікарня «Центр матері та дитини»; Власенко Т.А. - Вінницький клінічний пологовий будинок № 2
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Мета: дослідження проведене з метою аналізу та вдосконалення якості диспансерного нагляду за дітьми, народженими з масою тіла < 1000 г та гестаційним віком ≤ 28 тижнів. Матеріали і методи. Основну групу становили 42 дитини, за якими проводилось катамнестичне спостереження, що включало контроль захворюваності, сенсорних функцій, психомоторного та соціоемоційного розвитку, коморбідних станів щонайменше до 18 місяців скоригованого віку. До групи порівняння були включені 36 дітей, яким здійснювався стандартний нагляд. Результати. Дослідження продемонструвало зниження частоти постнеонатальної смертності вдвічі та частоти розвитку церебрального паралічу на 7,5 %. Якісна диспансеризація дозволяє своєчасно виявити відхилення в сенсорному, моторному, когнітивному та соціоемоційному розвитку, застосувати методи ранньої реабілітації та знизити рівень інвалідизації надзвичайно недоношених дітей.
Цель: исследование проведено с целью анализа и усовершенствования качества диспансерного наблюдения за детьми, рожденными с массой тела < 1000 г и гестационным возрастом ≤ 28 недель. Материалы и методы. Основную группу составили 42 ребенка, за которыми проводилось катамнестическое наблюдение, включавшее контроль заболеваемости, сенсорных функций, психомоторного и социально-эмоционального развития, коморбидных состояний как минимум до 18 месяцев скорректированного возраста. В группу сравнения были включены 36 детей, за которыми велось стандартное наблюдение. Результаты. Исследование продемонстрировало снижение частоты постнеонатальной смертности вдвое, а также снижение частоты развития церебрального паралича на 7,5 %. Качественная диспансеризация позволяет своевременно выявить отклонения в сенсорном, моторном, когнитивном и социально-эмоциональном развитии, применить методы ранней реабилитации и снизить уровень инвалидизации чрезвычайно недоношенных детей.
Objective. The study was conducted to analyze and improve the quality of case follow-up of children with birth weight < 1000 g and gestational age ≤ 28 weeks. Materials and Methods. The study group comprised 42 children, for whom case follow-up was conducted, which included control of disease rate, sensory functions, psychomotor and social-emotional development, comorbid conditions until at least 18 months of corrected age. The comparison group included 36 children with a standard observation. Results. The study showed a reduction in the incidence of postneonatal mortality by half, as well as decrease in the prevalence of cerebral palsy by 7.5 %. Qualitative clinical examination enables to detect timely abnormalities in sensory, motor, cognitive and socio-emotional development, to apply the techniques of early rehabilitation and to reduce disability in extremely premature infants.
недоношені діти, надзвичайно мала маса тіла, катамнез, диспансеризація, інвалідність.
недоношенные дети, экстремально малая масса тела, катамнез, диспансеризация, инвалидность.
preterm infants, extremely low body weight, catamnesis, clinical examination, disability.
Статья опубликована на с. 61-66
Вступ
Передчасне народження залишається провідною проблемою світової та вітчизняної неонатології впродовж останніх кількох десятків років. Нині досягнуто значного прогресу в цій галузі: новонароджені з екстремально малою вагою (500–999 г) та надзвичайно малим терміном гестації (22–28 тижнів) мають високі шанси на життя завдяки розробці та впровадженню новітніх перинатальних технологій та методів виходжування. Дитина, не доношена половину фізіологічного строку вагітності, з вагою 500 г, яка уміщається на долоні лікаря, дихає і живе, тоді як ще на початку XXI сторіччя таке немовля у нашій країні вважали «абортним» плодом.
Однак успіхи неонатології часом призводять до невдач педіатрії. Після виписки з неонатологічного стаціонару всі такі діти потрапляють під спостереження до дільничних лікарів загальної практики — сімейної медицини, уявлення яких про подальший розвиток глибоко недоношених новонароджених є обмеженими та супроводжуються, з одного боку, страхом непередбачуваності, упередженістю щодо таких дітей, з іншого — відсутністю знань про основні відмінності нагляду порівняно з дітьми інших вагових категорій та браком досвіду. Слід зауважити, що на цей момент у нашій державі відсутні чіткі принципи та інструкції щодо катамнестичного спостереження за дітьми з вагою при народженні менше 1000 г та гестаційним віком менше 28 тижнів, а відповідно, немає і реєстрації наслідків їх неонатальних проблем. Тому існує певний дисонанс між високотехнологічними та високовартісними методами невідкладної допомоги передчасно народженим новонародженим у неонатальному періоді та подальшим диспансерним спостереженням за ними. Результатом цього стають втрачені можливості щодо ранньої діагностики і прогнозування несприятливих віддалених наслідків та своєчасної реабілітації таких немовлят у наступні вікові періоди.
Ця категорія дітей належить до групи найвищого ризику щодо формування органічної патології у вигляді церебрального паралічу, сліпоти, глухоти, затримки ментального розвитку, розладів аутистичного спектра, соціоемоційних проблем, а також постнеонатальної смерті [4]. Проте, за даними зарубіжних авторів, якісний супровід дітей високого перинатального ризику, до яких належать і екстремально недоношені малюки, є пріоритетом і дозволяє досягти значного зниження частоти вищезазначених ускладнень [10].
Одним із найбільш загрозливих наслідків є дитячий церебральний параліч (ДЦП), частота якого серед надзвичайно недоношених дітей у 70–80 разів вища, ніж у доношених, і, за даними різних авторів, сягає від 7,2 до 13,4 % проти 0,13–0,19 % [4]. Ця патологія є результатом перенесених у неонатальному періоді тяжких внутрішньошлуночкових крововиливів та перивентрикулярної лейкомаляції, що є органічним підґрунтям для формування неврологічного дефіциту. Дискутабельною залишається теорія інфекційного провокуючого компонента в розвитку ДЦП, яка знаходить нині все більше доказів [12, 14].
Інша моторна дисфункція в екстремально недоношених дітей у вигляді координаційного розладу, затримки розвитку крупної моторики, м’язової дистонії, аномалій ходи може передувати формуванню спастичних парезів та потребує якомога ранньої діагностики, ретельного динамічного контролю з залученням таких дітей до програм раннього втручання вже в перші місяці життя. Такі діти повинні знаходитися на обліку в дитячого невролога та ортопеда, які визначають графік обстежень для оцінки як топографії ураження (нейросонографія, магнітно-резонансна томографія), так і функціонального стану (стандартизовані шкали) та програму реабілітації. Доведена ефективність раннього застосування методу Войта-діагностики та проведення Войта-терапії, лікувальної фізкультури та масажу, малюкового плавання, дельфінотерапії [3, 8].
Когнітивний розвиток немовлят з екстремально низькою вагою також має свої особливості. Близько 40 % із них мають когнітивний дефіцит, затримку сприйняття, мовленнєві проблеми, дефіцит уваги та академічну неспроможність. Третина таких дітей вимагають спеціалізованого медичного супроводу і дві третини — освітньої та психологічної підтримки протягом навчання у школі [5, 14]. У дорослому віці відзначається менша гнучкість мисленнєвих процесів, сповільнення цілеспрямованої виконавчої діяльності, труднощі з прийняттям рішень, плануванням та організацією, виснаження уваги та пам’яті. За даними досліджень, проведених у Швеції, Німеччині та Норвегії, 56,1–83,2 % дітей, народжених у 23–28 тижнів гестації закінчують 12-річну школу порівняно з 75–88 % народжених у строк. Такі діти мають гірші академічні досягнення, зокрема в математиці, частіше залишаються на повторний рік навчання (40 проти 27 %) та рідше вступають до вищих навчальних закладів (30 проти 53 %) [1, 4, 6].
Батькам часто важко об’єктивно оцінити інтелектуальні здібності власної дитини, особливо в ранньому віці, у зв’язку з чим усвідомлення проблеми приходить лише у шкільному віці, коли дорогоцінний час для адекватної стимуляції пізнавальних функцій вже втрачено і дитина потребує навчання у спеціалізованих закладах. Нині розроблено велику кількість методів оцінки когнітивного розвитку починаючи з перших місяців життя. Нормалізовані шкали Бейлі (1993), Мюллен (1995), Векслера (2000) та ін. дають можливість розрахувати еквівалентні показники розумового розвитку з урахуванням скорегованого віку, виокремити сектори відставання, а в старшому віці — оцінити коефіцієнт інтелекту (IQ). Необхідну допомогу повинні надати медичний психолог, логопед, педагог-дефектолог, розвитковий педіатр.
Частота сенсорних порушень у надзвичайно недоношених дітей теж перевищує аналогічні показники серед народжених у строк. Так, білатеральна сліпота як наслідок ретинопатії недоношених виникає у 7,4 % із них. У структурі дитячої інвалідності за зором ретинопатія посідає друге місце (17–18 %). Крім сліпоти, 64 % таких дітей вимагають призначення окулярів у віці до 7 років, тоді як серед доношених цей показник становить 37 %. Близько 4 % з них мають відстрочені проблеми з зором у вигляді пізнього відшарування сітківки в дорослому віці з необхідністю оперативної корекції [4]. Інші проблеми включають косоокість, порушення рефракції, амбліопію, дефекти полів зору. З метою своєчасної діагностики ретинопатії та обрання правильної лікувальної тактики (лазерокоагуляція) обов’язкове офтальмологічне обстеження повинно здійснюватись на 4–6-му тижні життя і надалі щонайменше до досягнення скорегованого віку 18 місяців.
Сенсоневральна приглухуватість реєструється у 8,7 % немовлят з екстремально малою вагою, тоді як серед доношених дітей цей показник не перевищує 0,4 % [4, 11]. Недостатня зрілість слухових центрів, кортієвого органа та провідникових шляхів слухового аналізатора відразу після передчасного народження обмежує можливості ранньої діагностики порушень слуху, даючи велику кількість хибнонегативних результатів. Доцільним є сурдологічний скринінг після досягнення дитиною 40 тижнів постконцептуального віку (або на момент виписки залежно від того, що відбувається раніше). Найбільш оптимальним методом для швидкого неінвазивного скринінгу слуху є визначення отоакустичної емісії продукта спотворення портативним скринером, що має бути наявний у кожному неонатологічному відділенні та кабінетах катамнезу. При підозрі на наявність аудіологічних проблем виконується реєстрація коротколатентних слухових викликаних потенціалів. Повторні обстеження повинні проводитись під час кожного візиту протягом першого року життя до отримання трьох послідовних позитивних результатів з інтервалом 1 місяць. Рання (з 3–4 місяців) корекція слуху слуховими апаратами, а в подальшому за показаннями кохлеарними імплантами дозволяє запобігти розвитку мовленнєвих, когнітивних проблем та соціальній дизадаптації.
Діти, народжені з екстремально малою вагою, схильні мати соціальні, емоційні та поведінкові проблеми більшою мірою, ніж їх доношені однолітки. Їх виявлення та об’єктивна оцінка можливі за умови використання поведінкових анкет, шкал та опитувальників. Серед найбільш апробованих: опитувальник дитячої поведінки (CBCL 1.5–5) опитувальник дитячих зусиль та труднощів (SDQ), оцінка дитячої поведінки Кауфмана (K-ABC), шкала соціоемоційного розвитку (ASQ:SE). Крім того, розроблені окремі інструменти для скринінгу аутизму: ADOS, M-CHAT-R/F, VABS, СARS та інші. Світовий досвід демонструє, що серед даної когорти дітей удвічі вищою є частота синдрому гіперактивності та дефіциту уваги, афективних станів та агресії, замкнутості, розладів сну, що корелюють із рівнем моторного та ментального розвитку [1, 5]. Так, розлади аутистичного спектра становлять 0,6–1,3 проти 0,05 %, депресивні стани — 14,1 проти 6 % у доношених малюків. Інші психіатричні синдроми зустрічаються з частотою 12,4 проти 4,9 %. Такі діти мають вищі індивідуальні ризики розвитку наркотичної та алкогольної залежності, а також фобій, пов’язаних із втратою батьківського піклування і початком самостійного життя. Не дивно, що репродуктивні рівні становлять лише 25,0 % для жінок та 13,9 % для чоловіків порівняно з 68,4 та 50,4 % відповідно серед народжених у строк [4].
Скринінг поведінкових проблем повинен застосовуватись протягом диспансерного спостереження при кожному візиті, що дозволить своєчасно виявити соціальну та емоційну дизадаптацію та спрямувати дитину на індивідуалізовані корегуючі програми, ефективність яких достатньо висока, зважаючи на пластичність та регенераторні можливості дитячої нервової системи та психіки.
Крім того, динамічному спостереженню повинна підлягати та сукупність проблем, що не асоціюється з інвалідністю, проте нерідко супроводжує ріст і розвиток цих дітей та впливає на якість їх життя. Зокрема, проблеми харчування, толерантності до їжі, дефіцитні стани (анемія, рахіт), проблеми імунологічного статусу та алергії, частота інфекційних захворювань та госпіталізацій у ранньому дитячому віці.
У цілому частота нейросенсорної інвалідизації серед екстремально недоношених дітей у країнах із високим економічним потенціалом коливається в діапазоні 10,9–26,8 % проти 0,1–2,3 % у доношених дітей. Близько 10,6–13,2 % із них отримують державну фінансову допомогу у зв’язку з хворобою чи втратою працездатності проти 1,3–1,7 % серед решти населення. Разом із тим якість життя таких людей у дорослому віці практично не відрізняється від решти, хоча в осіб із неврологічним дефіцитом вона є нижчою [4]. З іншого боку, ці показники дуже мінливі, оскільки прямо залежать від якості неонатальної допомоги, що зростає швидкими темпами.
Метою даного дослідження є підвищення якості диспансерного спостереження за глибоко недоношеними дітьми.
Матеріали і методи
У дослідження було залучено 78 недоношених дітей із вагою при народженні < 1000 г та гестаційним віком ≤ 28 тижнів, які були виписані зі стаціонару Вінницького обласного неонатального центру. Основну групу становили 42 дитини, яким у подальшому проводилось динамічне диспансерне спостереження в умовах кабінету катамнезу Він–ницької обласної дитячої клінічної лікарні з визначенням параметрів фізичного розвитку, психоневрологічного статусу та захворюваності. Групу порівняння становили 36 дітей, які спостерігалися стандартно.
Диспансерний нагляд за дітьми основної групи розпочинався одразу після виписки з неонатологічного стаціонару та тривав щонайменше до досягнення ними скорегованого віку 18 місяців. Скоригований вік обчислювався за сумою гестаційного та хронологічного віку до 24 місяців, після чого використовувався лише хронологічний вік. Клінічні діагнози встановлювали згідно з Міжнародною класифікацією хвороб 10-го перегляду.
Оцінка моторно-когнітивного розвитку здійснювалась щоквартально за допомогою шкали MSEL (Mullen Scales of Early Learning, 1995), яка є стандартизованим інструментом для виявлення взаємопов’язаних, але функціонально окремих моторно-когнітивних навичок у дітей віком від 0 до 69 місяців та включає оцінку великої та дрібної моторики, візуальної рецепції, рецептивної та експресивної мови. Шкала дозволяє отримати як загальні моторні та когнітивні індекси, так і виявити відставання в окремому функціональному секторі і спрямувати дитину на високоіндивідуалізовану програму.
Соціоемоційний розвиток оцінювався під час кожного візиту дитини за допомогою модифікованої оновленої анкети для скринінгу аутизму у малюків (M-CHAT-R/F) та опитувальника дитячої поведінки (CBCL 1.5–5) після досягнення дитиною скоригованого віку 16 місяців. Дані анкети для батьків дають можливість визначити інтерналізовані (емоційна реактивність, замкнутість, психосоматичні розлади, тривожно-депресивні синдроми), екстерналізовані (синдроми провини та агресії, гіперактивність та дефіцит уваги) проблеми поведінки, а також оцінити ступінь ризику розвитку аутизму. Рання діагностика поведінкових розладів чи підозра на них дає можливість своєчасно залучити дитячого психіатра до реабілітаційної програми.
Об’єктивна оцінка функції органів зору включала офтальмологічне обстеження під час кожного візиту з офтальмоскопією та контролем показань до оперативного втручання. Скринінг на порушення слуху виконувався всім дітям перед випискою зі стаціонару методом отоакустичної емісії продукту спотворення. При отриманні позитивного результату («чує») повторні обстеження проводились з інтервалом 1 місяць до отримання трьох послідовних позитивних результатів. При негативному результаті первинного скринінгу проводилась реєстрація коротколатентних слухових викликаних потенціалів сурдологом і, якщо мало місце підтвердження порушення слуху, дитина направлялась на раннє слухопротезування у віці до 6 місяців із метою уникнення розвитку дефектів мови та покращення соціальної інтеграції.
Крім того, під час кожного візиту оцінювався фізичний розвиток, нутритивний статус, показання до вакцинації, здійснювався загальний аналіз крові та сечі, визначення рівня глюкози крові, проводилось нейросонографічне обстеження та ультрасонографічне обстеження органів черевної порожнини та серця. Діти були консультовані неврологом, ортопедом, офтальмологом, сурдологом, імунологом-алергологом, а за потреби і нейрохірургом, ендокринологом, інфекціоністом, психіатром. Контролювались дотації заліза, вітаміну D.
Результати дослідження та їх обговорення
Діти з груп спостереження вірогідно не відрізнялись. Маса тіла при народженні коливалась у межах від 570 до 999 г, середній показник у дітей основної групи становив 890,7 ± 14,6 г, у дітей групи порівняння — 947,1 ± 12,3 г. В основній групі 6 (14,3 %) дітей народились з вагою менше 750 г, тоді як у групі порівняння не було жодної такої дитини. Гестаційний вік був у межах 23–28 тижнів, середні значення в основній та групі порівняння становили 26,9 ± 0,4 та 28,0 ± 0,3 відповідно. Дітей із гестацією 23–25 тижнів було 14 (33,3 %) в основній групі та 1 (2,8 %) у групі порівняння. В обох групах вірогідно переважали дівчатка — 11 із 31 в основній та 11 із 25 у групі порівняння.
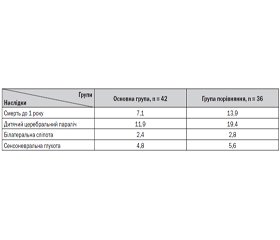
Отримані дані свідчать про високий рівень інвалідизуючої захворюваності серед надзвичайно недоношених дітей у ранньому дитинстві (кожна п’ята дитина (19,1 ± 6,1 %) основної групи та майже кожна третя (27,8 ± 7,5 %) — групи порівняння). Проте частота випадків постнеонатальної смертності зменшилась майже вдвічі (з 13,9 до 7,1 %), частота церебрального паралічу знизилась в 1,6 раза (на 7,5 %). Стабільною залишається частота сліпоти та приглухуватості, проте варто зазначити, що всі діти основної групи з дефектами слуху були протезовані на ранніх етапах (до 1 року), а їх розумовий та мовний розвиток не демонструє значного відставання, тоді як глухі діти групи порівняння розвивають вторинну німоту, яку практично неможливо ліквідувати навіть після успішного відновлення функції слуху. Не маючи адекватного звукового навантаження впродовж перших місяців життя, вже у віці 1,5–2 роки такі діти виробляють та закріплюють навички невербального спілкування, компенсуючи втрачену функцію. Виключення стимуляції нейронів мозку звуковими подразниками та їх інтерференції з інформаційними сигналами з інших аналізаторів веде до порушення формування другої сигнальної системи, субатрофічних змін кори та прилеглих центрів, зумовлюючи когнітивний дефіцит. Вчасно слухопротезована дитина має високі шанси на успішне навчання в загальноосвітній школі.
Близько половини дітей основної групи мають затримку моторного (45,2 ± 7,7 %) і когнітивного (54,7 ± 7,7 %) розвитку, у понад 60 % випадків демонструючи поєднаний її варіант. Поведінкові проблеми супроводжують розвиток кожної третьої дитини з екстремально малою вагою (31,0 ± 7,1 %) основної групи. Домінують серед них інтерналізовані розлади у вигляді замкнутості, аутистичних проявів, тривоги. Відсутність всебічного диспансерного нагляду за дітьми групи порівняння утруднила аналіз їх моторного, ментального та соціоемоційного розвитку, оскільки рутинні огляди педіатра не включають визначення цих параметрів, а батьки не можуть дати адекватну оцінку своїм дітям. Дані показники вдалося простежити лише у третини (27,8 %) дітей, яким був поставлений діагноз «затримка психомоторного розвитку» або «затримка статокінетичного розвитку» дитячим неврологом.
На прикладі дітей групи порівняння можна побачити, що левова частка відповідальності за здоров’я дитини лягає на плечі батьків. Проте вони, не маючи медичної освіти, не можуть об’єктивно, а головне вчасно сигналізувати про порушення у стані малюка. Субклінічні, без вираженої маніфестації, прояви інтелектуальних, соціоемоційних, сенсорних і навіть рухових проблем часто не привертають увагу батьків й оцінюються ними як неважливі, тимчасові чи навіть приймаються за особливості характеру дитини. За умов запізнілої діагностики втрачається цінність превентивних реабілітаційних заходів. Результатом стає інвалідність або низька якість життя.
Нині в Україні готується до затвердження національний протокол щодо диспансерного спостереження за дітьми з групи ризику розвитку моторних та нейропсихічних порушень, у яку входять і недоношені діти з надзвичайно малою вагою. Протоколом передбачається ідентифікація цільових груп ризику ще в пологових будинках. Батькам пропонуватиметься своєчасне обстеження та оцінювання ще до того, як ознаки порушень почнуть з’являтись у дитини [9]. Після виписки зі стаціонару до динамічного спостереження будуть залучені педіатр/неонатолог, дитячий психолог, невролог, офтальмолог, отоларинголог, дієтолог, медичні соціальні працівники, фізичний терапевт, логопед, окупаційний терапевт. Усі діти проходитимуть сурдологічний скринінг методом визначення отоакустичної емісії продукту спотворення і реєстрації коротколатентних слухових викликаних потенціалів портативними скринерами. Оцінка статокінетичного та інтелектуального розвитку здійснюватиметься за шкалами Бейлі (BSID-III), наявність поведінкових проблем та соціоемоційних розладів моніторуватиметься опитувальником ASQ:SE, скринінг на розлади аутистичного спектра проводитиметься за допомогою M-CHAT. Ініціатива раннього втручання включатиме індивідуальні тренувальні програми, починаючи з періоду новонародженості, реабілітацію порушеної дієздатності, корекцію сенсорних функцій, допомогу в налагодженні харчування, психологічний та соціальний супровід сім’ї, де зростає дитина з особливими потребами. Зауважимо, що вибір інструментів (шкал та анкет) для оцінки розвитку та поведінки не є принциповим, оскільки велика сукупність досліджень, проведених у різних країнах світу, показують еквівалентні цінність та недоліки кожної з них. Насправді важливим є сам факт спостереження і ранньої оцінки [1–3, 11].
Світовий досвід демонструє зниження показників інвалідності у скоригованому віці 2,5 року з 37–44 % у 1995 році до 13–18 % у 2011 році з запровадженням регіоналізації медичної допомоги та активного follow-up супроводу дітей з екстремально малою вагою. У віці 6 років 73 % з них є здоровими або мають мінімальні відхилення у розвитку [10]. У Німеччині проект віддаленого спостереження за глибоко недоношеними дітьми (гестація < 28 тижнів) дозволив прослідкувати частку 81 % дітей, які вижили, до 6 місяців, 74 % — до двох років та 59 % — до 5-річного віку. При порівнянні цих часових інтервалів відмічено зростання як мінімальних, так і грубих порушень здоров’я, що вкотре підтверджує необхідність довготривалого нагляду. У віці 5 років 27 % демонструють нормальний розвиток, 49 % мають мінімальні відхилення та 24 % — грубі порушення [2]. Метааналіз, проведений із залученням 3133 надзвичайно недоношених пацієнтів, показав значний позитивний ефект програм раннього втручання на когнітивний та емоційний розвиток як у малюковому, так і в дошкільному віці з дещо меншим впливом на моторний розвиток [7, 13].
Висновки
Диспансерне спостереження за дітьми, які народилися з масою тіла менше 1000 г та/або терміном гестації до 28 тижнів, повинно здійснюватися в лікувально-профілактичних закладах 3-го рівня (обласна дитяча лікарня) або спеціальних центрах.
Якісна диспансеризація дозволяє своєчасно виявити відхилення в сенсорному, моторному, когнітивному та соціоемоційному розвитку, застосувати методи ранньої реабілітації та знизити рівень інвалідизації надзвичайно недоношених дітей.
Оцінка моторно-когнітивного розвитку за допомогою шкали MSEL (Mullen Scales of Early Learning, 1995) та соціоемоційного розвитку за допомогою модифікованої анкети (M-CHAT-R/F) й опитувальника дитячої поведінки (CBCL 1.5–5) дозволяють своєчасно отримати об’єктивну інформацію щодо особливостей індивідуального розвитку дитини.
Дослідження продемонструвало зниження частоти постнеонатальної смертності вдвічі та частоти розвитку церебрального паралічу в 1,6 раза.
1. Aarnoudse-Moens C.S.H., Weisglas-Kuperus N., van Goudoever J.B. [et al.]. Meta-Analysis of Neurobehavioral Outcomes in Very Preterm and/or Very Low Birth Weight Children // Pediatrics. — 2009. — 124(2). — 717-728.
2. Damm G., Sens B., Harms K. et al. State-wide follow-up of extremely preterm infants: a model of cross-sectoral quality analysis // Z. Evid. Fortbild. Qual. Gesundhwes. — 2011. — 105(8). — 597-605. doi:10.1016/j.zefq.2011.08.002.
3. Delobel-Ayoub M., Arnaud C., White-Koning M. et al. Behavioral Problems and Cognitive Performance at 5 Years of Age After Very Preterm Birth: The EPIPAGE Study // Pediatrics. — 2009. — 123(6). — 1485-1492.
4. Doyle L.W., Anderson P.J. Adult Outcome of Extremely Preterm Infants // Pediatrics. — 2010. — 126. — 342-351.
5. Goldstein R.F., Cotten C.M., Shankaran S. et al. Influence of gestational age on death and neurodevelopmental outcome in premature infants with severe intracranial hemorrhage // J. Perinatol. — 2013. — 33(1). — 25-32.
6. Iwata S., Nakamura T., Hizume E. et al. Qualitative Brain MRI at Term and Cognitive Outcomes at 9 Years After Very Preterm Birth // Pediatrics. — 2012. — 129(5). — 1138-1147.
7. Orton J., Spittle A., Doyle L. et al. Do early intervention programmes improve cognitive and motor outcomes for preterm infants after discharge? A systematic review // Dev. Med. Child. Neurol. — 2009. — 51(11). — 851-859.
8. Reidy N., Morgan A., Thompson D.K. Impaired language abilities and white matter abnormalities in children born very preterm and/or very low birth weight // J. Pediatr. — 2013. — 162(4). — 719-724.
9. Riha O.O. Vidkryti pytannja katamnestyčnoho sposterežennja za novonarodženymy hrup ryzyku. Častyna 1. / O.O. Riha // Neonatolohija, chirurhija ta perynatal’na medycyna. — 2013. — T. III, № 2(8). — S. 118-124.
10. Serenius F., Kеllеn K., Blennow M. et al. Neurodevelopmental outcome in extremely preterm infants at 2.5 years after active perinatal care in Sweden // JAMA. — 2013. — 309(17). — 1810-1820.
11. Spittle A., Orton J., Anderson P. et al. Early developmental intervention programmes post-hospital discharge to prevent motor and cognitive impairments in preterm infants // Cochrane Database Syst. Rev. — 2012.
12. Sutton P.S., Darmstadt G.L. Preterm Birth and Neurodevelopment: A Review of Outcomes and Recommendations for Early Identification and Cost-effective Interventions // J. Trop. Pediatr. — 2013. — 59(4). — 258-265.
13. Woodward L.J., Clark C.A., Pritchard V.E. et al. Neonatal white matter abnormalities predict global executive function impairment in children born very preterm // Dev. Neuropsychol. — 2011. — 36(1). — 22-41.
14. Woodward L.J., Clark C.A.C., Bora S. et al. Neonatal White Matter Abnormalities an Important Predictor of Neurocognitive Outcome for Very Preterm Children // PLoS One. — 2012. — 7(12). — 518-529.

/64/64.jpg)