Журнал «Здоровье ребенка» 2 (53) 2014
Вернуться к номеру
Длительная инсоляция у подростка как триггер дебюта системной красной волчанки. Случай из практики
Авторы: Максимова С.М., Самойленко И.Г. - Донецкий национальный медицинский университет им. М. Горького; Бухтияров Э.В. - ЦГКБ № 3, г. Донецк; Лепихов П.А., Турпакова Г.Н. - ОДКБ, г. Донецк
Рубрики: Семейная медицина/Терапия, Ревматология, Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
В статье описан случай клинического наблюдения за пациенткой с системной красной волчанкой, поступившей с ошибочным диагнозом «фотодерматит, внебольничная пневмония». Благодаря полиорганности поражений и клинико-анамнестическим данным удалось верифицировать диагноз в короткие сроки и направить ребенка в специализированную клинику.
У статті описано випадок клінічного спостереження за пацієнткою з системним червоним вовчаком, яка надійшла з помилковим діагнозом «фотодерматит, позалікарняна пневмонія». Завдяки поліорганності уражень і клініко-анамнестичним даним вдалося верифікувати діагноз у короткий термін і направити дитину в спеціалізовану клініку.
The article describes the case of the clinical observation of the patient with systemic lupus erythematosus, admitted to a hospital with misdiagnosis «photocontact dermatitis, community-acquired pneumonia». Due to multiple organ lesioans and clinical and medical history data we could certain the diagnosis in short terms, and to refer the child to a specialized clinic.
дети, инсоляция, системная красная волчанка.
діти, інсоляція, системний червоний вовчак.
children, exposure to sun, systemic lupus erythematosus.
Статья опубликована на с. 127-130
Проблема ранней диагностики системной красной волчанки (СКВ) у детей остается актуальной до настоящего времени, поскольку, несмотря на достигнутые успехи в лечении, существуют определенные трудности распознавания заболевания. В том числе возможны ошибки в диагностике СКВ, особенно на ранних этапах развития болезни, когда отсутствуют полиорганные поражения и дебют СКВ протекает нередко в виде различных клинических масок. Именно на этом этапе дети поступают в соматические или инфекционные отделения с разными предполагаемыми диагнозами геморрагического васкулита, острого гломерулонефрита, фотодерматита и др. От своевременного распознавания СКВ под масками других заболеваний зависят успех дальнейшего лечения и прогноз заболевания [1].
СКВ является наиболее тяжелой из группы системных аутоиммунных болезней соединительной ткани, в основе которой лежит генетически обусловленное нарушение иммунной регуляции и образование аутоантител к компонентам собственных клеток. В результате развивается прогрессирующая дезорганизация соединительной ткани с признаками иммунного воспаления в тканях многих органов и систем, в том числе возникают некротические и дистрофические изменения в них с исходом в атрофические и склеротические процессы [2].
На самом деле СКВ является инвалидизирующим заболеванием с поражением многих органов и систем (почек, сердца, нервной системы, легких, суставов), приводящим к стойким функциональным и органическим нарушениям, в первую очередь к развитию сердечной недостаточности и хронической почечной недостаточности, и требующим постоянной базисной иммуносупрессивной терапии. Без лечения прогноз неблагоприятный. Этиология СКВ остается неясной, отсюда вытекают трудности диагностики лечения. Известна генетическая предрасположенность к развитию СКВ. Генетические исследования выявили множество (до 50) генов, ассоциированных с развитием болезни и вызывающих различные нарушения иммунного ответа. У некоторых больных СКВ выявляют наследственный дефицит факторов комплемента С1q, С2 или С4, что приводит к нарушению клиренса иммунных комплексов [2, 3]. Предполагают роль гормональных факторов (половых гормонов), некоторых вирусных и бактериальных инфекций, и поэтому болезнь развивается у часто болеющих детей [4].
Среди факторов внешней среды, влияющих на развитие СКВ, первостепенное значение имеет избыточная инсоляция, которая может провоцировать начало и последующие обострения СКВ. Ультрафиолетовое облучение (УФО) приводит к деградации ДНК в клетках кожи, стимулирует апоптоз кератиноцитов, нарушает метаболизм фосфолипидов клеточной мембраны, стимулирует В-клетки и вызывает аутоиммунные реакции у предрасположенных к фотосенсибилизации детей. Кроме того, УФО усиливает высвобождение интерлейкинов (ИЛ)-1, ИЛ-3, ИЛ-6, что способствует развитию местного воспаления, а также повышает общий уровень иммунного ответа [3, 4].
Клиника СКВ у детей характеризуется более острым началом и течением болезни, ранней и бурной генерализацией, а также менее благоприятным исходом, чем у взрослых. Клинические проявления СКВ у детей разнообразны и характеризуются полиорганной симптоматикой, но почти у 20 % детей наблюдается моносиндромный дебют болезни [5]. Первые общие симптомы наиболее часто проявляются в виде интермиттирующей лихорадки, нарастающей слабости, снижения аппетита, потери веса, гнездного или тотального выпадения волос [5, 6]. У каждого шестого ребенка на протяжении начального периода СКВ, иногда длительно, в течение нескольких месяцев, в клинической картине могут преобладать признаки одного синдрома — кожного, суставного, почечного, тромбоцитопенической пурпуры, гемолитической анемии, тромбоза и др., что затрудняет раннюю диагностику и приводит к позднему установлению диагноза [6]. Но у большинства детей (более 80 %) уже в течение нескольких недель (реже — месяцев) с момента появления первых симптомов формируется полисиндромная картина с признаками поражения различных органов и систем [4–6].
Для установления диагноза СКВ в настоящее время используют классификационные критерии Американской ревматологической ассоциации (1997 г.). Поражение кожи наблюдается у 97 % детей и отличается большим разнообразием: от эритематозных высыпаний на лице в области скуловых дуг и переносицы (волчаночная «бабочка», дискоидные высыпания) до эритематозных высыпаний на открытых участках кожи верхней трети груди (область декольте) и спины, над локтевыми и коленными суставами [3–5, 7].
Сосудистые изменения в виде капиллярита ладоней и подошв, сетчатое ливедо, подногтевые кровоизлияния, синдром Рейно, геморрагические высыпания в виде петехий или пурпуры на коже дистальных отделов, чаще нижних конечностей, наблюдаются нередко у детей в остром периоде СКВ. В активном периоде болезни очень характерны истончение и повышенное выпадение волос — алопеция очаговая или диффузная [8–10]. Более чем у 30 % детей, больных СКВ, в активном периоде наблюдается поражение слизистых оболочек полости рта в виде хейлита, энантемы в области твердого неба, афтозного стоматита [9, 10].
Суставной синдром в виде артралгий и острого артрита наблюдается практически у всех больных, и у большинства из них (до 80 %) он проявляется одним из первых, имеет мигрирующий характер и редко приводит к формированию стойких деформаций. Поражение мышц у детей с СКВ проявляется миалгиями или полимиозитом, реже — слабостью в проксимальных симметричных мышцах конечностей и наблюдается более чем у половины больных, что заставляет их обратиться к врачу [8–10].
Поражение серозных оболочек (полисерозит) проявляется плевритом, перикардитом и перитонитом у 30–50 % больных. Миокардит наблюдается реже (10 %), имеет скудную клинику и обнаруживается только при комплексном инструментальном исследовании. Специфичным для СКВ является атипичный бородавчатый эндокардит Либмана — Сакса с образованием бородавчатых наложений, с мелкими перфорациями створок клапанов и разрывом хорд. В то же время формирование пороков сердца для СКВ не характерно [9, 10]. Поражение коронарных артерий у детей чаще протекает асимптомно, в единичных случаях возможно развитие инфаркта миокарда и формирование аневризм [10].
Изменения в легких и плевре наблюдаются у 30–50 % детей с СКВ. Могут отмечаться боль в грудной клетке, кашель. Признаки плеврита (чаще сухого) выявляются при Ro-графии или КТ органов грудной клетки. Пневмония при высокой степени активности заболевания клинически может проявляться одышкой, ослаблением дыхания, сухими и влажными хрипами. На Ro-грамме видны инфильтративные тени в легких, дисковидные ателектазы [7, 9, 10].
Поражение почек у детей при СКВ наблюдается у 70–75 % пациентов. В то же время у одной трети больных клинические симптомы выражены уже в дебюте болезни, а у большинства они развиваются в течение первых двух лет от момента начала заболевания. Морфологические изменения в почках представлены признаками иммунокомплексного гломерулонефрита различного типа. Выделяют нефрит выраженной формы с нефротическим синдромом (НС), нефрит выраженной формы без НС и нефрит латентной формы с умеренно выраженным мочевым синдромом. Возможен и наиболее неблагоприятный вариант поражения почек в виде быстропрогрессирующего волчаночного нефрита со злокачественным течением и быстрым развитием почечной недостаточности, приводящей к неблагоприятному исходу [4, 6, 9].
Нередко отмечают гепато– и спленомегалию, генерализованную лимфаденопатию. Поражение нервной системы проявляется невропатиями, изменениями личности (эмоциональная лабильность, раздражительность, апатия, депрессия), головными болями, судорожным синдромом, транзиторными нарушениями мозгового кровообращения, психозами [4, 5, 9, 10].
Антифосфолипидный синдром при СКВ, как вторичный симптомокомплекс, обусловлен тромбозами сосудов различной локализации и проявляется в виде ладонной и подошвенной эритемы, поверхностных кожных некрозов, пурпурой, инфарктами почек, легких, миокарда [8].
Гематологические нарушения у детей с СКВ в активном периоде болезни проявляются в виде лейкопении, обычно в сочетании с лимфопенией. Реже наблюдается аутоиммунная гемолитическая анемия с положительной реакцией Кумбса. Тромбоцитопения (чаще умеренная) развивается у 15–26 % больных и клинически проявляется в виде петехий, экхимозов, кровотечений из десен, носовых и маточных — у девочек. Увеличение СОЭ характерно для всех больных в активном периоде. Иммунные нарушения при СКВ: антитела (АТ) к нативной ДНК в повышенных титрах; наличие АТ к Sm–антигену; наличие антител к фосфолипидам: повышенный титр антител к кардиолипину (IgМ или IgG); выявление волчаночного антикоагулянта стандартным методом; ложноположительная реакция Вассермана в течение не менее 6 месяцев [2, 9, 10].
В качестве примера приводим случай из нашей практики, когда в генезе полисиндромного дебюта СКВ у девочки-подростка провоцирующую роль сыграла длительная и избыточная инсоляция. Девочка И., 15 лет, заболела остро в конце июня 2013 года, когда после отдыха на море появилась сыпь на коже лица и шеи. Состояние было расценено как фотодерматит. После симптоматического лечения состояние кожи улучшилось, поэтому начиная с середины июля (в течение месяца) девочка вновь находилась на море, сыпь усиливалась. С начала августа присоединились боли в мышцах, преимущественно в нижних конечностях, артралгии в коленных суставах. Спустя 2 недели появилась фебрильная лихорадка и кашель, что было расценено как острый трахеобронхит. Сыпь на коже усилилась. Осмотрена дерматологом, получала лечение амбулаторно, однако состояние не улучшилось: в течение двух недель сохранялась фебрильная температура, резистентная к терапии жаропонижающими средствами и антибиотиками.
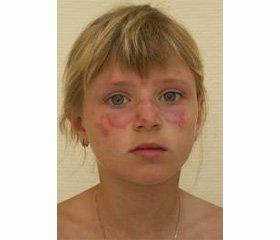
Направлена в местный стационар, где при обследовании выявлена лейкопения до 2,4 Г/л, анемия до 106 г/л, повышение СОЭ до 45 мм/ч. Предположено системное заболевание соединительной ткани. По настоянию родителей была выписана для обследования и лечения в России. При поступлении 03.09.2013 в отделение клинической иммунологии РДКБ состояние девочки расценено как среднетяжелое. Жалобы на повышенную утомляемость, слабость, сыпь на коже лица, туловища, повышение температуры тела до фебрильных цифр. Самочувствие неудовлетворительное за счет астении, интоксикации и фебрильной лихорадки. Кожные покровы, видимые слизистые бледно-розовые, на коже лица выраженный васкулит, на щеках, спинке носа — по типу «бабочки», пятнисто-папулезная сыпь вокруг локтевых суставов, на спине, плечах. Периферических отеков нет. Видимые слизистые чистые, розовые. Кашель сухой. Дыхание в легких жесткое, хрипов нет. Границы сердца не смещены, тоны сердца ясные, ритмичные. Живот мягкий, безболезненный, доступен глубокой пальпации. Печень, селезенка не пальпируются. Мочеиспускание в норме.
Обследована в отделении клинической иммунологии. В общем анализе крови: анемия легкой степени (Нb — 102 г/л, эр. — 3,7 Т/л), лейкопения (лейк. — 1,42 Г/л), тромбоцитопения (тромб. — 160 Г/л), миелоциты — 1 %, метамиелоциты — 1 %, п/я — 23 %, с/я — 42 %, э. — 2 %, л. — 23 %, м. — 8 %, СОЭ – 45 мм/ч. В биохимическом анализе крови: общий белок, мочевина, общий холестерин и билирубин, АлАТ, глюкоза, калий, натрий в пределах нормы. Отмечено умеренное повышение АсАТ до 69 МЕ/л (при норме 10–42). Иммунологические показатели: резко снижено содержание С3 — до 56,7 мг/дл (при норме 79–152), С4 — до 4,83 мг/дл (при норме 16–38), резко повышено содержание АТ к ДНК — более 200 ед/мл (при норме 0–25), IgG — 2060 мг/дл (при норме 45–240), IgА — 303 мг/дл (при норме 81–232). В коагулограмме — без отклонений. Прямая проба Кумбса положительная. В анализе мочи — без патологических изменений. На ЭКГ изменения процессов реполяризации в миокарде. При осмотре окулиста виявлена ангиопатия сетчатки.
При УЗИ органов брюшной полости и почек: печень, поджелудочная железа, желчный пузырь в норме. Уплотнены стенки сосудов селезенки, эхогенность неоднородная за счет единичных гипоэхогенных включений до 3 мм. Слева под кожей в проекции 7-го ребра лимфоузел размером 11 х 4 мм. Почки не увеличены, эхогенность не изменена. На ЭхоКГ: крупные сосуды, перегородки не изменены. Сократимость миокарда в норме. Пролапс АВ-клапанов с регургитацией +1, регургитация на ЛА +1. Дополнительные хорды в левом желудочке. Выпот в полости перикарда у верхушки до 7 мл. Злокачественный онкогематологический процесс исключен.
По совокупности клинико-анамнестических данных результатов обследования подтверждена системная красная волчанка, острый период, высокая степень активности, активность II–III ст., НФО — 1 ст. Кожный васкулит. Миоперикардит. Астеноневротический синдром.
Проведена пульс-терапия солумедролом с дальнейшим переходом на прием преднизолона по 0,5 мг/кг в сутки, и в качестве базовой осуществлялась пульс-терапия циклофосфаном в дозе 1000 мг в/в капельно один раз в 28–30 дней. Также проводилась антибактериальная (сульперазоном 1,5 г два раза в день в/в капельно) и сопроводительная терапия (панангин, кальций-Д3 никомед, нексиум, верошпирон, неотон, месна, лазикс, китрил). На фоне проводимого лечения состояние ребенка с положительной динамикой: температура тела нормализовалась, побледнела сыпь на лице, восстановились до нормы показатели лейкоцитов и тромбоцитов. В стабильном состоянии с улучшением выписана для продолжения терапии по месту жительства с рекомендациями: продолжить прием преднизолона 25 мг/сутки постоянно, продолжить высокодозовую терапию циклофосфаном в дозе 1000 мг один раз в месяц. Медицинский отвод от профилактических прививок сроком на 1 год показан данной больной. Противопоказаны интенсивные физические нагрузки. Показано обучение на дому и оформление инвалидности.
Девочка повторно госпитализирована в отделение клинической иммунологии, где продолжена базисная терапия циклофосфаном в дозе 1000 мг в/в капельно (повторное введение). Рекомендовано продолжить прием преднизолона в дозе 25 мг в сутки, а также высокодозовую терапию циклофосфаном в дозе 1000 мг в месяц (суммарно 6000 мг/курс).
По жизненным показаниям девочка нуждается в проведении регулярной иммуносупрессивной терапии циклофосфаном, т.к. отказ от терапии смертельно опасен. Показан прием верошпирона 50 мг в 19:00 до следующей госпитализации, а также кальций-Д3 никомед 1000 мг/сутки на все время приема преднизолона, предуктал — 1 табл. один раз в день, курантил — 50 мг два раза в день, аспирин кардио — 25 мг на ночь, нексиум — 20 мг на ночь — 2 месяца. Контроль общего анализа крови 1 раз в 14 дней и биохимических и иммунологических показателей, антинуклеарного фактора, АТ к ДНК, АТ к кардиолипину, С3-, С4-компонента комплемента один раз в месяц.
Таким образом, длительная инсоляция спровоцировала у девочки развитие СКВ, сначала под маской фотодерматита, а при повторной инсоляции явилась триггерным фактором и привела к полисиндромному дебюту болезни. Для предотвращения обострения заболевания в данном случае даны рекомендации избегать инсоляции и применения УФО как возможного триггера СКВ.
1. Щербакова М.Ю., Гуревич О.В., Ярошевская О.И. и др. Проблема ранней диагностики системной красной волчанки у детей в условиях многопрофильной клинической больницы // Педиатрия. — 2009. — Т. 88, № 5. — С. 28–32.
2. Рациональная фармакотерапия детских заболеваний: Руководство для практикующих врачей. Системная красная волчанка / Под ред. А.А. Баранова и соавт. — М.: ГЭОТАР-медиа, 2009. — С. 878–901.
3. Прохоров Е.В., Борисова Т.П. Особенности современного течения и терапии системной красной волчанки у детей и подростков // Здоровье ребенка. — 2007. — № 2(5). — С. 60–66.
4. Клиническая ревматология: Руководство для врачей / Под ред. Насоновой В.А., Астапенко М.Г. — М.: Медицина, 1989. — 583 с.
5. Ревматология детского возраста / Под ред. Е.В. Прохорова, А.П. Волосовца. — Донецк, 2006. — С. 50–68.
6. Педиатрия: клинические рекомендации. Системная красная волчанка / Под ред. А.А. Баранова. — Москва: ГЭОТАР-медиа, 2009. — С. 320–345.
7. Детская ревматология: Руководство для врачей / Под ред. А.А. Баранова, Л.К. Баженовой. — М.: Медицина, 2002. — 336 с.
8. Запруднов А.М., Григорьев К.И., Харитонова Л.А. Детские болезни: Учебник для вузов. — М.: ГЭОТАР-медиа, 2004. — С. 383–388.
9. Дранник Г.Н. Клиническая иммунология и аллергология: Пособие для студентов, врачей-интернов, иммунологов, аллергологов. Системная красная волчанка. — Киев, 2010. — С. 246–253.
10. Иванова М.М. Системная красная волчанка // Диффузные болезни соединительной ткани (системные ревматические заболевания): Руководство для врачей. — М.: Медицина, 2004. — 307 с.