Журнал «Актуальная инфектология» 1 (1) 2013
Вернуться к номеру
Лечение и диагностика лямблиоза в современных условиях
Авторы: Мочалова А.А., Ершова И.Б., Карпенко И.Н., Черкасоа С.Н. - Луганский государственный медицинский университет; Луганская областная детская инфекционная больница; Луганская 3-я детская многопрофильная больница
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
Лямблиоз — это широко распространенное заболевание, и оно выявляется во всех странах мира. По данным Всемирной организации здравоохранения (ВОЗ), 10–20 % населения земного шара инвазировано лямблиями [8]. Однако анализ эпидемиологических обзоров свидетельствует, что показатели распространенности лямблиоза зависят не только от страны, но и от города, возрастной группы, времени года, качества питьевой воды, уровня коммунального благоустройства местности, принадлежности к группам риска, иммунного статуса обследованных, от применяемых диагностических методов и т.д. Согласно статистическим отчетам, инвазированность в США составляет 7,4 %, в Норвегии — 3,3 %, но наиболее высокие показатели регистрируются в странах Африки, Азии и Южной Америки — до 35 % [5, 7]. В Украине, к сожалению, распространенность лямблиоза находится на уровне развивающихся стран.
Впервые лямблии были обнаружены в 1681 г. изобретателем микроскопа Антони ван Левенгуком у больного с жидким стулом. И только в 1859 г. были детально изучены и описаны профессором Харьковского университета Д.Ф. Лямблем. Его имя и дало название этим простейшим. Второе название — жиардиаз — они получили благодаря французскому ученому Альфреду Жиарду, описавшему вид протозойной инфекции Giardia, к которому принадлежат лямблии. Во всем мире сохраняется два названия этого заболевания: лямблиоз и жиардиаз.
В настоящее время на основе морфологических исследований среди представителей рода Giardia trophozoites выделяют три вида лямблий: G.lamblia или intestinalis (имеет до 10 подтипов), G.muris и G.agilis. Патогенной для человека и млекопитающих является только G.lamblia [12].
Источником заражения является человек или млекопитающие. Различают три основных пути передачи лямблиоза: водный, контактно–бытовой и пищевой. В детских учреждениях чаще всего основным фактором передачи лямблиоза являются грязные руки детей и, возможно, персонала, объекты и предметы бытовой обстановки, контаминированные цистами паразита (дверные ручки, горшки, игрушки и др.) [9]. Механическим переносчиком цист лямблий могут быть мухи. При загрязнении водопроводной воды цисты сохраняются до 3 мес. Используемые для очистки воды обычные концентрации хлора не оказывают губительного воздействия на цисты лямблий.
От больного в сутки с каловыми массами выделяется до 900 млн цист лямблий, в то время как инфективная доза для человека составляет всего 10–25 цист.
Вегетативная форма неустойчива во внешней среде и погибает через 5–10 минут. Она предназначена для существования в организме человека. Цисты более устойчивы. На предметах при комнатной температуре они сохраняются до 2 недель, а в воде — до 80 суток. Губительны для цист высушивание и высокие температуры. При высыхании они гибнут в течение 1–2 мин, при 70 °С — в течение 30–40 с, при кипячении — мгновенно.
Жизненный цикл лямблий включает две морфологические формы — вегетативную (трофозоиты) и цистированную (цисты).
Вегетативные формы паразитируют в верхнем отделе тонкого кишечника. В процессе своей жизнедеятельности они постепенно спускаются в дистальные отделы тонкой и поперечноободочной кишки, где образуют цисты, и в таком виде выводятся из организма. Процесс образования цист занимает около 10–12 часов [16]. Циста является не только формой защиты лямблии от неблагоприятных факторов внешней среды — это и форма подготовки к делению, так как при повторном попадании в организм человека из цисты уже в течение 10–15 минут образуется сразу два трофозоита (вегетативные формы лямблий), которые в дальнейшем способны к самостоятельному размножению. Причем с такой интенсивностью, что на 1 см2 слизистой оболочки кишки может находиться до 1 млн лямблий и более [12].
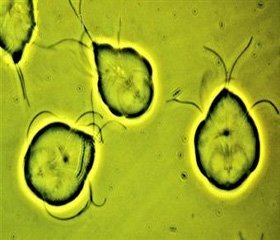
Вегетативные формы поглощают питательные вещества и ферменты осмотическим путем через оболочки из щеточной каймы тонкой кишки, тем самым вмешиваясь в процесс мембранного пищеварения и нарушая его. Они имеют 2 ядра, которые в сочетании с парабазальным телом придают паразиту при микроскопии вид «лица с гримасничающим ртом». Движение вокруг оси тела, которое обеспечивают 4 пары жгутиков, напоминает полет падающего листа. С помощью присасывательного диска лямблии прикрепляются к эпителию кишечных ворсинок.
Отсутствие патогномоничных клинических симптомов заболевания, а также широкое распространение паразитов привело к тому, что длительное время они считались непатогенными. Однако впоследствии клиническое наблюдение позволило прийти к выводу, что лямблии не являются безвредными, заражение ими приводит к развитию болезни, которую необходимо вовремя диагностировать и лечить [1].
Дабы закончить дебаты среди ученых всего мира, ВОЗ в 1988 году опубликовала определение термина «лямблиоз», под которым подразумевается любой случай инвазии лямблиями, как клинически явный, так и бессимптомный.
Касаясь повреждающего действия лямблий на стенку кишечника, необходимо отметить, что паразит, в течение своей индивидуальной жизни многократно прикрепляясь и открепляясь, вызывает не только механическое раздражение, но и, воздействуя также на нервные окончания, может привести к патологическим рефлекторным реакциям со стороны органов пищеварения. Подтверждением вышеописанного является проведенное Е.А. Корниенко с соавт. (2009) эндоскопическое и морфологическое обследование 124 детей с лямблиозом в возрасте от 3 до 17 лет, которое показало, что структурные изменения слизистой оболочки тонкой кишки развиваются в 100 % случаев. Эндоскопически слизистая оболочка желудка и луковицы двенадцатиперстной кишки у большинства больных не имела никаких патологических изменений, в ряде случаев отмечалась лишь незначительная гиперемия. В то же время в постбульбарном отделе двенадцатиперстной кишки во всех случаях наблюдались явления дуоденита (гиперемия, отек, сглаженность складок), в 55 % случаев дуоденит сопровождался лимфостазом (белесый налет на поверхности слизистой оболочки тонкой кишки, симптом «манной крупы»). Лимфостаз в постбульбарном отделе двенадцатиперстной кишки оказался признаком, свойственным лямблиозу (специфичность — 96 %), поэтому наличие этого эндоскопического симптома у ребенка должно вызывать у врача подозрение на лямблиоз и побуждать к дальнейшему поиску паразита.
Наиболее отчетливо изменяется двигательная функция кишечника: появляется склонность к непрерывным сокращениям, спазмам, повышению тонуса кишки, нарушается секреторная функция. Кроме того, нарушение процессов всасывания происходит также вследствие прямого токсического действия лямблий. Угнетение синтеза некоторых ферментов способствует нарушению гидролиза углеводов до моносахаров. В связи с этим развивающаяся диарея имеет, скорее всего, осмотический характер. Снижается абсорбция витамина B12, нарушается С–витаминный обмен. Это указывает, что вещества, продуцируемые лямблиями, прямо или косвенно повреждают структуру микроворсинок тонкой кишки [3].
Лямблии не могут существовать в желчевыводящих путях (желчь убивает их). В связи с этим они не могут быть причиной тяжелых нарушений печени, холецистохолангитов (обусловленная ими рефлекторная дискинезия желчевыводящих путей способствует лишь наслоению вторичной бактериальной инфекции), поражений нервной системы, но создают благоприятный фон для размножения бактерий и дрожжевых клеток.
Клинические проявления лямблиоза крайне многообразны и неспецифичны, в связи с чем многократно пересматривались и переоценивались различные классификации этого заболевания.
Выраженность клинических проявлений зависит как от массивности инвазии, так и от состояния организма [17].
Клинические признаки манифестного лямблиоза можно объединить в несколько групп. В первую очередь для заболевания характерны симптомы со стороны желудочно–кишечного тракта: неустойчивость стула, метеоризм, боли в животе (у детей старшего возраста — часто сильные, принимающие язвенноподобный характер), подташнивание, иногда рвота, снижение аппетита [6]. При обследовании у детей чаще всего выявляется:
— стойкая обложенность языка;
— метеоризм и урчание в кишечнике (вздутый живот);
— «шум плеска» при исследовании толстой кишки (синдром Образцова);
— болезненность в пилородуоденальной зоне, мезо–гипогастрии.
Следующая группа симптомов обусловлена синдромом интоксикации, особой чертой которого является угнетенное, депрессивное состояние пациента. Не случайно Д.Ф. Лямбль называл открытый им микроорганизм «паразитом тоски и печали». Возможны также раздражительность, плаксивость, головные боли, головокружение, нарушение сна, субфебрилитет. У некоторых больных функциональные изменения со стороны нервной системы являются единственными клиническими проявлениями заболевания, в связи с чем у больных с неврозами, этиология которых неясна, целесо–образно наряду с другими исследованиями исключить возможность лямблиоза.
Таких симптомов интоксикации, как лихорадка, –ознобы, рвота, не наблюдается. До сих пор тонкие механизмы угнетающего действия паразита на центральную нервную систему остаются неизученными.
Лямблиозная инвазия может быть причиной аллергических проявлений. По данным некоторых авторов, у 69 % больных с аллергодерматозом обнаруживаются лямблии, у 16 % — энтеробиоз, а у 3 % — аскаридоз [4]. Об аллергодерматозах на почве лямблиоза можно думать тогда, когда десенсибилизирующая терапия не дает эффекта.
При длительном процессе у детей может выявляться полисимптоматика поражения кожи. Бледность кожных покровов, особенно кожи лица, отмечается у всех больных (что иногда считается парадоксальным при высоких показателях гемоглобина), что, вероятнее, обусловлено спазмом сосудов. Иногда встречается неравномерная окраска кожи («разноцветная кожа») и иктеричный ее оттенок. Буро–иктерично–коричневая окраска кожи шеи, боковых поверхностей живота, подмышечных складок отмечается на более поздних этапах хронического течения лямблиоза и обусловлена, вероятно, присоединением глюкокортикоидной недостаточности. Изменение кожи ладоней и подошв — часто регистрируемый в последние годы симптом при лямблиозе. Цвет кожи становится иктерично–розовым, появляется сухость. Довольно частым симптомом при лямблиозе у детей и подростков является поражение красной каймы губ. Степень выраженности бывает различной: от легкого шелушения и сухости, до выраженного хейлита с трещинами, заедами, шелушением пероральной зоны.
И наконец, последним симптомокомплексом является нарушение питания как следствие мальабсорбции.
В целом для клинической картины лямблиоза характерен волнообразный характер с периодами нарастания и стихания гастроэнтерологической симптоматики, хотя нарушения нутритивного статуса, интоксикация и аллергические проявления могут нарастать. В анализах крови часто наблюдается эозинофилия, лимфоцитоз, а по мере прогрессирования заболевания нередко наблюдается гипохромная анемия.
Показаниями к исследованию на лямблиоз являются:
— заболевания пищеварительного тракта с тенденцией к их хроническому течению с частыми, умеренно выраженными обострениями;
— нейроциркуляторная дисфункция, особенно в сочетании с желудочно–кишечными нарушениями;
— стойкая эозинофилия крови;
— аллергические заболевания.
Лабораторная диагностика лямблиоза довольно проблематична. Это связано с тем, что диагноз лямблиоза может быть установлен лишь на основании нахождения цист лямблий в фекалиях при копрологическом исследовании. Однако следует учитывать, что при проведении этого обследования результат зачастую ложноотрицательный.
Анализ неудач в выявлении лямблий при исследовании фекалий позволил систематизировать основные причины неудач, ложноотрицательных результатов [2, 4]. К ним относятся:
1) неправильно собранный материал для исследования (твердые фракции фекалий из нижних отрезков толстой кишки);
2) представление в лабораторию кала на фоне приема медикаментов (антибиотики, антациды, антидиарейные средства, слабительные и т.д.), повреждающих морфологию паразитов;
3) несвоевременная доставка в лабораторию исследуемого материала (кал в теплом виде, дуоденальное содержимое — не позже чем через 10–15 мин после его получения);
4) погрешности лабораторного исследования (не используются все методы подготовки материала, подготовка мазка некачественная, отсутствие настойчивости при осмотре препарата);
5) исследование фекалий в так называемый «немой» период, когда прекращается выделение цист лямблий (поэтому для повышения эффективности диагностики при показаниях необходимо проводить многократные исследования до 6–7 раз с интервалами 1–2 дня).
При устранении данных причин при первом обследовании кала выявление лямблий возможно уже у 76 % больных, после второго исследования вероятность увеличивается до 90 %.
Таким образом, для оптимизации копрологического исследования необходимо:
— 3–4–кратное исследование кала с различными интервалами (7–8 дней);
— исследование по возможности жидких фракций фекалий (порции, прилежащей к тонкой кишке), собранных из 6–7 мест;
— исключение приема медикаментов перед исследованием на 5–7 дней в связи с возможностью повреждения морфологии цист;
— применение консервантов при невозможности доставки материала в лабораторию в течение короткого времени.
Многочисленными исследованиями доказано, что создание неблагоприятных условий для жизнедеятельности паразита способствует образованию и выделению цист. В качестве провокации можно использовать настой кукурузных рыльцев, современные желчегонные препараты. При этом вероятность обнаружения лямблий, по данным разных авторов, повышается до 90 %.
С целью улучшения диагностики используют иммунологические методы исследования (определение специфических антител в крови).
Выявление специфических IgM и IgG к антигенам лямблий методом иммунофлюоресцентного анализа (ИФА) возможно с 12–14–го дня заболевания. После санации IgM быстро исчезают. Их выявление свидетельствует о заболевании лямблиозом. IgG сохраняются до 2 мес. после санации. Однако их определение в крови не является достоверным признаком паразитирования лямблий в настоящий момент, а может свидетельствовать о перенесенной инвазии. Отсутствие специфических иммуноглобулинов у детей с повторным обнаружением цист лямблий является плохим прогностическим признаком и требует от врача применения индивидуальных схем лечения. Достаточно часто антитела к лямблиям не обнаруживаются у пациентов с иммунными дисфункциями.
При обнаружении возбудителя лямблиоза проводят специфическую терапию этого заболевания.
Лечение больного с лямблиозом включает несколько этапов [13]. Перед проведением терапии больному необходимо:
1) тщательное соблюдение личной гигиены;
2) установление диеты и режима питания, направленных на создание условий, ухудшающих размножение лямблий (ограничение углеводов и исключение молочных продуктов); введение продуктов, являющихся нутритивными сорбентами (каши, отруби, печеные яблоки, груши, сухофрукты, растительное масло);
3) очищение билиарной системы, желчного пузыря и кишечника один раз в 6–7 дней: прием натощак 25% раствора сернокислой магнезии (в зависимости от возраста) или 30–50% раствора сорбита или ксилита;
4) назначение спазмолитических препаратов сроком на 1 неделю;
5) устранение дисфункциональных расстройств желудочно–кишечного тракта + антидепрессивный эффект (гастритол — по 20–30 капель 3 р/д, 2 нед.);
6) устранение В–витаминной недостаточности и повышение устойчивости нервной системы (В–витаминные комплексы — 2 нед.);
7) эффективность этиотропной терапии повышается на фоне приема витамина С.
В отношении этиотропной терапии необходимо отметить, что в последнее время все чаще появляются публикации о развитии резистентности лямблий к таким ранее широко применяемым препаратам, как метронидазол и тинидазол [10, 14]. К тому же такие противопоказания при назначении этих препаратов, как беременность, а при назначении тинидазола — еще и болезни крови, расстройства центральной нервной системы, наличие побочных реакций в виде преходящей лейкопении, головокружения, локомоторной атаксии, делают их использование ограниченным.
В связи с этим в настоящее время продолжаются поиск и разработка новых способов лечения данного недуга. Одним из современных средств нового поколения при этиотропном лечении лямблиоза является Макмирор (нифуратель), синтезированный научно–исследовательской лабораторией Polichem, Италия. Нифуратель — производное нитрофурана, отличительной особенностью которого является наличие в химической формуле тиоэфирной группы (SCH3), благодаря которой существенно расширяется спектр противомикробного и противопротозойного действия нифурателя и не вырабатывается устойчивости к препарату.
Спектр антибактериальной активности нифурателя:
— простейшие: Lamblia intestinalis, Trichomonas vaginalis, Entamoeba histolytica;
— патогенные грибы: Candida albicans, Microsporum spp., Trichophyton spp.;
— бактерии:
а) грамотрицательные: E.coli, Shigella spp., Salmonella spp., Proteus spp., Klebsiella spp., Vibrio cholerae;
б) грамположительные: Staphylococcus spp., Streptococcus spp., Helicobacter pylori.
Нифуратель блокирует ряд энзимных цепочек и ингибирует синтез белка в рибосомах на самых ранних этапах трансляции (в отличие от других антибактериальных средств, действующих на белковый синтез). Это препятствует появлению устойчивых штаммов микроорганизмов и развитию перекрестной резистентности (рис. 1).
Важной особенностью препарата Макмирор является то, что он практически полностью элиминируется почками, не затрагивая при этом дезинтоксикационные резервы печени, в то время как метронидазол элиминируется клетками печени [11].
Кроме того, очень важной особенностью является способность нифурателя угнетать рост патогенной флоры (E.сoli с измененной ферментативной активностью, грибы рода Candida) в кишечнике, при этом наблюдается рост бифидо– и лактобактерий (табл. 1).
Макмирор (нифуратель) применяется у детей с 6 лет из расчета 30 мг/кг/сут за 2 приема, а у взрослых — по 2 таблетки после еды 3 раза в день в течение 7 дней.
Побочные эффекты возникают редко, поэтому препарат рекомендован в педиатрической практике.
В связи с изложенным целью нашего исследования стало изучение клинико–лабораторной эффективности препарата Макмирор у больных лямблиозом.
Материалы и методы
Под наблюдением находилось 78 человек. Среди них 46 детей и подростков от 6 до 18 лет, а также 32 пациента в возрасте старше 18 лет. Наблюдение всех больных осуществлялось на базе инфекционных отделений Луганска и Луганской области. Во всех случаях диагноз установлен на основании обнаружения цист лямблий при копрологическом обследовании фекалий. Пациенты были разделены на 2 группы. Больные 1–й группы (n = 34) получали в качестве противопаразитарного лечения метронидазол: пациенты младше 8 лет — по 375 мг в сутки, старше 8 лет — по 500 мг в сутки (в 2 приема). Больные 2–й группы (n = 44) получали Макмирор (нифуратель), который назначался детям по 15 мг/кг 2 раза в день, взрослым — по 400 мг (2 таблетки) 3 раза в день после еды. Курс терапии составил 10 дней.
Клиническая картина обследуемых больных в двух группах до лечения была сходной и характеризовалась диареей, болями в животе, метеоризмом, слабостью, тошнотой, аллергодерматозами, повышенной утомляемостью, без достоверных отличий между группами.
Результаты и их обсуждение
После проведенного курса терапии при контрольном обследовании пациентов было установлено, что такие симптомы, как слабость, снижение аппетита, различного характера боли в животе, периодические головные боли, исчезали в среднем на 2–3 дня раньше при лечении, включающем в качестве этиотропного препарата Макмирор (табл. 2, рис. 2).
Метеоризм, повышенное урчание в кишечнике при пальпации были на 4,1 дня продолжительнее при терапии, в комплексе которой использовался метронидазол. Высыпания различного характера, напоминающие аллергодерматозы, сохранялись более продолжительно, чем при терапии с применением препарата Макмирор.
К концу терапии у больных, получавших Макмирор, полностью исчезала эозинофилия. В гемограмме пациентов, принимавших метронидазол, только у 67,6 % отмечалась нормализация относительного содержания эозинофилов, а у 32,4 % наблюдалось лишь снижение эозинофилии, что свидетельствует о неполной санации патологического процесса.
Дискинезия желчевыводящих путей после проведенной терапии наблюдалась во 2–й группе в 1,5 раза реже.
Повторное обнаружение лямблий при лечении препаратом Макмирор зарегистрировано у 6,8 % обследуемых, в то время как при терапии метронидазолом — у 20,6 %.
Полученные результаты позволяют сделать вывод о высокой клинико–лабораторной эффективности препарата Макмирор при лечении лямблиоза. Кроме того, широкий спектр противомикробного и противопротозойного действия нифурателя является очень важным свойством препарата, так как лямблиоз довольно часто протекает на фоне других кишечных заболеваний.
Макмирор хорошо переносился всеми пациентами. Ни один больной не указывал на побочные эффекты или непереносимость препарата. Поэтому не потребовалось досрочной отмены данного лекарственного средства или дополнительного назначения других лекарств.
Профилактика лямблиоза проводится в комплексе мероприятий против кишечных инфекций и гельминтозов [15]. Очень важно строгое соблюдение санитарно–гигиенических правил в быту и в детских учреждениях. Цисты выделяются во внешнюю среду носителями в огромных количествах, поэтому для профилактики лямблиоза необходимо строгое соблюдение мер по предотвращению фекального загрязнения окружающей обстановки, пищевых продуктов и воды, строгое соблюдение правил личной гигиены. Вместе с тем необходимы меры по обезвреживанию источника возбудителя.
1. Авдюхина Т.И., Константинова Т.Н., Кучеря Т.В., Горбунова Ю.П. Лямблиоз. — М., 2003. — 32 с.
2. Агафонова Е.В., Долбин Д.А., Куликов С.Н. и др. Со–временные аспекты диагностики лямблиоза у человека // Рус. мед. журн. — 2008. — Т. 16, № 17. — С. 146–149.
3. Бельмер С.В. Лямблиоз у детей // Рус. мед. журн. — 2004. — Т. 12, № 3. — С. 141–144.
4. Бодня Е.И., Повгородняя О.И. Лямблиоз: проблемы и перспективы диагностики // Мистецтво лікування. — 2013. — № 8. — С. 14–16.
5. Клиническая паразитология. — Женева: ВОЗ, 2012. — С. 231–240.
6. Корниенко Е.А., Дроздова С.Н., Калинина Н.М. и др. Современное течение лямблиоза // Вопросы детской диетологии. — 2008. — Т. 8, № 2. — С. 6–11.
7. Корниенко Е.А., Минина С.Н., Фaдинa С.A., Лo6oдa T.Б. Клиника, диагностика и лечение лямблиоза у детей // Педиатрическая фармакология. — 2009. — Т. 6, № 4. — С. 2–7.
8. Крамарев С., Григорович Ю. Роль лямблій в патології органів травлення у дітей // Medicus Amicus. — 2005. — № 4.
9. Лямблиоз у детей: Метод. реком. / Н.И. Зрячкин, Ю.С. Цека, Т.Ю. Гроздова и др. — Саратов, 2012. — 24 с.
10. Падейская Е.Н. 5–нитроимидазолы — антимикробные препараты для лечения бактериальных и протозойных инфекций // Consilium medicum. — 2004. — Т. 6, № 1.
11. Cedillo–Rivera R., Munoz O. In–vitro susceptibility of Giardia lamblia to albendazole, mebendazole and other chemotherapeutic agents // J. Med. Microbiol. — 2004. — Vol. 37. — P. 221–224.
12. Escobedo A.A., Nunez F.A., Moreira I. Comparison of chloroquine, albendazole and tinidazole in the treatment of children with giardiasis // Annals of Tropical Medicine & Parasitology. — 2003. — Vol. 97, № 4. — P. 367–371.
13. Michael J.G. Farthing treatment options for the eradication of intestinal protozoa // Nature Clinical Practice Gastroenterology & Hepatology. — 2006. — № 3. — P. 436–445.
14. Oguz К., Аli Т., Huseyin G. et al. Albendazole versus metronidazole treatment of adult giardiasis: An open randomized clinical study // World J. Gastroenterol. — 2004. — 10 (8). — P. 1215–1217.
15. Pennardt M., Cox F.E. Human parasitology. Giardiasis // Clin. Microbiol. Rev. — 2006. — Vol. 15, № 4. — P. 595–612.
16. Sesirbellioglu S.A., Ulcay A., Can M., Erdern M. et al. Saccharomyces boulardiiand infection due to Giardia lamblia // Scand. J. Infect. Dis. — 2006. — Vol. 38, № 6–7. — P. 479–481.
17. Syed А., Аli Т., David R. Hill Giardia intestinalis // Curr. Opin. Infect. Dis. — 2003. — 16 (5). — P. 453–460.

/98/98.jpg)
/98/98_2.jpg)
/99/99.jpg)
/100/100.jpg)