Журнал «» 4(18) 2011
Вернуться к номеру
Ефективність застосування фіксованої комбінації аторвастатину з езетимібом (Статезі) в корекції дисліпідемії в пацієнтів із цукровим діабетом 2-го типу
Авторы: Чернишов В.А., Інститут терапії ім. Л.Т. Малої АМН України, м. Харків
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
У статті подані результати 8-тижневого застосування фіксованої комбінації аторвастатину 10 мг та езетимібу 10 мг (препарат Статезі) у корекції дисліпідемії (ДЛП) ІІа, ІІb типів і при їх поєднанні з гіпоальфахолестеринемією (ГАХС) у 34 хворих віком від 39 до 53 років із гіпертонічною хворобою і цукровим діабетом 2-го типу, які не досягли цільових рівнів холестерину (ХС) ліпопротеїдів низької щільності (ЛПНЩ) на попередній 4-тижневій терапії аторвастатином 10 мг/добу. Установлено, що незалежно від фенотипу ДЛП препарат знижує рівень загального ХС на 34,5 % (р < 0,01), ХС ЛПНЩ — на 49,2 % (р < 0,001), що дозволяє досягти цільового рівня ХС ЛПНЩ у 91,2 % хворих. Гіпотригліцеридемічний ефект проявляється зниженням рівня тригліцеридів у середньому на 21,2 % (p < 0,05). Спостерігається тенденція до підвищення концентрації ХС у ліпопротеїдах високої щільності (ЛПВЩ) на 9,2 % (p > 0,05). При ІІа типі ДЛП Статезі справляє переважно гіпохолестеринемічний ефект, при ІІb типі проявляє гіпохолестеринемічний і гіпотригліцеридемічний ефекти, а при поєднанні ІІа й ІІb типів ДЛП із ГАХС реалізуються всі три ефекти препарату: гіпохолестеринемічний, гіпотригліцеридемічний і здатність підвищувати вміст ХС у ЛПВЩ.
Виявлені корисні для хворих на ЦД 2-го типа плейотропні ефекти Статезі: зниження концентрації СРБ у крові на 31,3 % (p < 0,05), тенденція до зниження інсулінемії і глікемії натще відповідно на 9,9 и 12,4 % (p > 0,05), індексу НОМА — на 20,7 % (p > 0,05).
Цукровий діабет, дисліпідемія, аторвастатин, езетиміб.
Сьогодні для корекції порушень ліпідного обміну найбільш ефективними препаратами вважають інгібітори 3-гідрокси-3-метилглутарил-коензим А-редуктази — статини, що не тільки знижують рівні загального холестерину (ЗХС) і холестерину (ХС) ліпопротеїдів низької щільності (ЛПНЩ), але й підвищують ХС ліпопротеїдів високої щільності (ЛПВЩ) та справляють виражений антисклеротичний ефект [25]. Цукровий діабет (ЦД) розглядається як один із вагомих самостійних показань до постійного приймання статинів [29].
Одним із найбільш активних представників класу статинів є аторвастатин — синтетичний статин, ефективність і безпечність якого вивчені в численних контрольованих клінічних дослідженнях (MIRACL, PROVE-IT, TIMI-22, CARDS, ASCOT-LLA, TNT, IDEAL, REVERSAL). Серед статинів аторвастатин є єдиним препаратом, що продемонстрував високу ефективність у досить широкому діапазоні добових доз — від 10 до 80 мг [9].
Середні терапевтичні дози статинів недостатньо знижують уміст ХС у складі ЛПНЩ, а використання максимальних добових доз не у всіх хворих призводить до досягнення цільового рівня показника. Навіть кожне подвоєння дози статину, починаючи з 20 мг/добу, дозволяє додатково знизити рівень ХС ЛПНЩ лише на 6–7 % [5]. Один із механізмів такого незначного підвищення ефективності статинів при подвоєнні добової дози може бути пов’язаний із посиленням абсорбції ХС із кишечника. Тому використання комбінації статину з речовинами, що блокують абсорбцію ХС у кишечнику, є дуже перспективним [10]. Серед таких речовин найбільш вивченим і таким, що добре зарекомендував себе на світовому фармацевтичному ринку, є препарат езетиміб [17].
Компанією Mili Healthcare Ltd. (Великобританія) на фармацевтичний ринок України виведено препарат Статезі, до складу якого входять аторвастатин (у дозі 10 мг) і езетиміб (у дозі 10 мг) [11].
Отже, метою роботи була оцінка ефективності застосування фіксованої комбінації аторвастатину з езетимібом (Статезі) в корекції різних фенотипів дисліпідемії (ДЛП) у пацієнтів із ЦД 2-го типу, які не досягли цільового рівня ХС ЛПНЩ при застосуванні монотерапії аторвастатином 10 мг/добу.
Матеріал і методи
У дослідження шляхом спеціального відбору залучені 34 пацієнти (19 чоловіків і 15 жінок) віком від 39 до 53 років (середній вік — 45,7 ± 2,3 року) з гіпертонічною хворобою (ГХ) ІІ стадії і ЦД 2-го типу в стадії компенсації або субкомпенсації вуглеводного обміну, що супроводжувався вторинною ДЛП ІІа і ІІb типів, незважаючи на приймання аторвастатину 10 мг/добу упродовж 4 останніх тижнів. Усі запрошені особи дали добровільну згоду на участь у дослідженні й знаходилися під динамічним амбулаторним спостереженням у відділі популяційних досліджень ДУ «Інститут терапії ім. Л.Т. Малої АМН України». Усі пацієнти під час спостереження дотримувалися гіполіпідемічної дієти, уникали споживання алкогольних напоїв і продовжували приймати індивідуально підібрану гіпоглікемічну терапію, що не змінювалася протягом усього терміну дослідження.
За даними анамнезу, тривалість ГХ становила від 4 до 14 років (у середньому — 9,6 ± 1,9 року), тривалість ЦД 2-го типу — від 1 до 11 років (у середньому — 6,3 ± 1,4 року). Стадію ГХ та ступінь підвищення артеріального тиску (АТ) установлювали за рекомендаціями Української асоціації кардіологів із профілактики та лікування артеріальної гіпертензії [6]. У всіх запрошених у дослідження осіб мали місце ГХ ІІ стадії, підвищення АТ, що відповідало 1-му ступеню, спостерігалося в 14 (41,2 %) осіб, 2-му ступеню — у 20 (58,8 %) хворих. Усі залучені в дослідження особи хворіли на ЦД 2-го типу, серед них у 22 (64,7 %) обстежених виявлено стан компенсації вуглеводного обміну й у 12 (35,3 %) — стан субкомпенсації за відомими діагностичними критеріями ВООЗ [35].
Тип ДЛП встановлювався за класифікацією D.S. Fredrickson із сучасними доповненнями [4]. ДЛП ІІа і ІІb типів виявлено відповідно в 16 (47,1 %) і 18 (52,9 %) хворих. Поєднання ІІа та ІІb типів ДЛП зі зниженим умістом ХС у складі ЛПВП — гіпоальфахолестеринемією (ГАХС) спостерігалося відповідно у 6 (17,6 %) і 8 (23,5 %) випадках.
У дослідження не включали хворих зі стенокардією напруження, тяжкою артеріальною гіпертензією, застійною серцевою недостатністю, тяжкими порушеннями серцевого ритму і проведення імпульсу, клінічно вагомими порушеннями функції печінки й нирок, ЦД 1-го типу, захворюваннями м’язів, патологією щитоподібної залози, наявністю в анамнезі інфаркту міокарда або мозкового інсульту терміном до 6 міс. перед залученням у дослідження.
Із приводу ГХ хворим призначено комбіновану антигіпертензивну терапію, що включала у 18 (52,9 %) випадках кардіоселективні b-адреноблокатори, у 23 (67,6 %) — інгібітори ангіотензинперетворюючого ферменту, в 11 (32,2 %) — блокатори рецепторів ангіотензину ІІ, у 16 (47,0 %) — антагоністи кальцію і в 34 (100 %) — ацетилсаліцилову кислоту. Індивідуально підібрана гіпоглікемічна терапія включала в 14 (41,2 %) випадках метформін, у 8 (23,5 %) — гліклазид і в 12 (35,3 %) — глімепірид.
Ураховуючи недосягнення цільових рівнів ХС ЛПНЩ упродовж попередніх 4 тиж. приймання аторвастатину 10 мг/добу, із метою корекції ДЛП усім пацієнтам призначено Статезі (фіксовану комбінацію аторвастатину 10 мг та езетимібу 10 мг) через 30 хв після вечері упродовж 8 тиж.
Усім залученим у дослідження хворим визначали вміст ЗХС, тригліцеридів (ТГ), ХС ЛПВЩ ферментативним методом на автоаналізаторі Humareader (Німеччина) з використанням наборів реагентів фірми Human (Німеччина). Уміст ХС ЛПНЩ обчислювали за формулою W.T. Friedewalt [8]:
ХС ЛПНЩ = ЗХС — (ХС ЛПВЩ + ТГ/2,22),
де ТГ/2,22 — уміст ХС у складі ліпопротеїдів дуже низької цільності (ЛПДНЩ).
Для поглибленої характеристики гіполіпідемічних ефектів Статезі додатково розраховували концентрацію ХС у складі не-ЛПВЩ (ЛПДНЩ + ЛПНЩ) за різницею ЗХС і ХС ЛПВЩ. Оскільки відмінною рисою ДЛП, що асоціюється з ЦД 2-го типу, є одночасне порушення метаболізму ЛПВЩ і ТГ, обчислювали також співвідношення ТГ/ХС ЛПВЩ, що характеризує внесок ліпопротеїдліполізу ТГ-умісних ЛПДНЩ в утворення ЛПВЩ [1]. Для оцінки впливу Статезі на систему зворотного транспорту ХС використовували співвідношення ЗХС/ХС ЛПВЩ [3].
Зазначені показники ліпідного обміну визначали відповідно у вихідному стані пацієнтів до призначення Статезі й через 8 тиж. від початку приймання препарату.
Досягнення цільових рівнів ліпідів у хворих контролювали за рекомендаціями Європейського товариства кардіологів (ESC, 2007) [19] та Менеджменту з лікування дисліпідемій ADA і АСС (2008) для пацієнтів високого кардіометаболічного ризику [16].
Плейотропні ефекти Статезі, зокрема вплив на системне запалення та інсулінорезистентність (ІР), досліджували за допомогою визначення рівня С-реактивного білка (СРБ) імуноферментним методом із використанням діагностичного набору фірми Diagnоstic Automation Inc. (США) та рівня імунореактивного інсуліну натще методом ELISA-твердофазного імуноферментного аналізу з антитілами проти молекули людського інсуліну з використанням реактивів фірми DRG Instruments GmbH (Німеччина). Індекс HOMA (Homeostatic Model Assessment), що характеризує ІР, вираховували за відомою формулою: рівень інсуліну натще (мкОд/мл) х глюкоза крові натще (ммоль/л)/22,5.
Рівень глюкози в сироватці крові натще визначали глюкозооксидазним методом. ІР в обстежених хворих діагностували при індексі НОМА вищому за 3 ум.од.
Для оцінки безпечності застосування фіксованої комбінації аторвастатину з езетимібом (Статезі) в динаміці спостереження за хворими проводили біохімічні дослідження крові з визначенням умісту сечовини, креатиніну, глюкози, сечової кислоти, активності печінкових трансаміназ (аспартат- і аланінамінотрансферази (АсАТ, АлАТ)), креатинфосфокінази (КФК) стандартними загальновідомими методами [2].
Статистичну обробку отриманих даних виконано на персональному комп’ютері за допомогою прикладної програми Stаtistica. Результати наведено у вигляді середніх арифметичних значень і помилки середньої величини М ± m. Вірогідність відмінностей показників оцінювали за t-критерієм Стьюдента.
Результати та обговорення
Відомо, що аторвастатин є найчастіше призначуваним та ефективним статином щодо зниження ХС ЛПНЩ. Він спричиняє виражене і стійке підвищення активності ЛПНЩ-рецепторів, а також сприятливо впливає на якість циркулюючих у кровотоці часток ЛПНЩ. У добовій дозі 10–80 мг він знижує рівень ЗХС на 3–46 %, ХС ЛПНЩ — на 41–61 %, ТГ — на 14–33 % і підвищує вміст ХС у складі ЛПВЩ на 5,1–8,7 % у пацієнтів із різними типами ДЛП [24].
У пацієнтів із гіперхолестеринемією (ГХС) монотерапія езетимібом сприяє зменшенню концентрації ХС ЛПНЩ на 20 %, ТГ — на 8 % і підвищенню рівня ХС ЛПВЩ на 5 % [30].
У клінічних дослідженнях доведено, що езетиміб і статини справляють взаємопотенціюючу дію і при їх одночасному застосуванні гіполіпідемічний ефект суттєво зростає порівняно з монотерапією статинами [11]. Сьогодні з’явилася можливість застосування фіксованої комбінації аторвастатину 10 мг з езетимібом 10 мг у вигляді препарату Статезі. Привабливим є те, що для цієї фіксованої комбінації характерне не просте фармакологічне поєднання двох препаратів, а взаємне потенціювання їх ефектів, про що свідчить той факт, що поєднання 10 мг аторвастатину й 10 мг езетимібу еквівалентне за гіполіпідемічним ефектом 80 мг (!) статину (максимальній добовій дозі) [15].
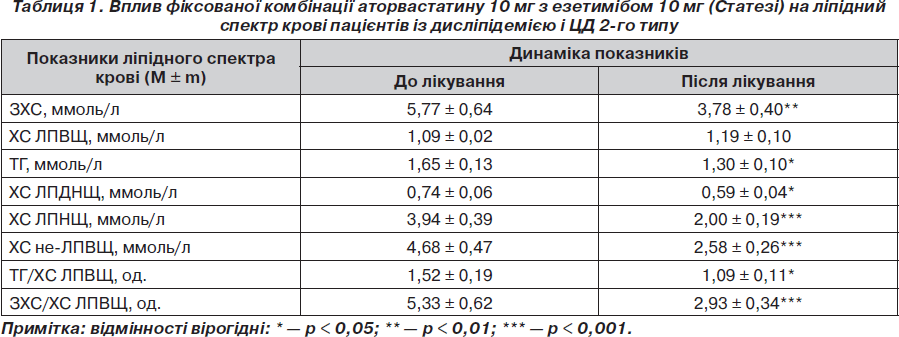
У нашому дослідженні у цілому по групі хворих на ГХ і ЦД 2-го типу з ДЛП, які не досягли цільового рівня ХС ЛПНЩ на 4-тижневій монотерапії аторвастатином 10 мг/добу, застосування препарату Статезі (табл. 1) упродовж 8 тиж. супроводжувалося вірогідним зниженням умісту в сироватці крові ЗХС на 34,5 % (p < 0,01) переважно за рахунок зменшення концентрації ХС у складі ЛПНЩ на 49,2 % (p < 0,001). Слід відзначити, що певний внесок у загальний гіпохолестеринемічний ефект препарату робила гіпотригліцеридемічна дія Статезі. Так, завдяки вірогідному зниженню ТГ на 21,2 % (p < 0,05) досягнуто зменшення вмісту ХС у складі ЛПДНЩ у середньому на 20,3 % (p < 0,05). Підвищення концентрації ХС ЛПВЩ на 9,2 % було невірогідним, що свідчить про необхідність більш тривалого застосування препарату для досягнення вірогідних змін цього показника. Але все ж таки така суттєва тенденція до підвищення рівня ХС ЛПВЩ свідчить про покращення стану двох систем — ліпопротеїдліполізу ТГ-умісних ЛПДНЩ та зворотного транспорту ХС при застосуванні препарату Статезі у хворих на ЦД 2-го типу. Підтвердженням цього було зниження відповідних ліпідних співвідношень ТГ/ХС ЛПВЩ (на 28,3 %; p < 0,05) та ЗХС/ХС ЛПВЩ (на 45,03 %; p < 0,001), а також концентрації ХС не-ЛПВЩ на 44,9 % (p < 0,001) на тлі гіпотригліцеридемічного і гіпохолестеринемічного ефектів.
Із всіх пацієнтів (n = 34), які не досягли цільового рівня ХС ЛПНЩ < 2,5 ммоль/л на попередній 4-тижневій терапії аторвастатином 10 мг/добу, при застосуванні Статезі це вдалося зробити у 31 (91,2 %) хворого.
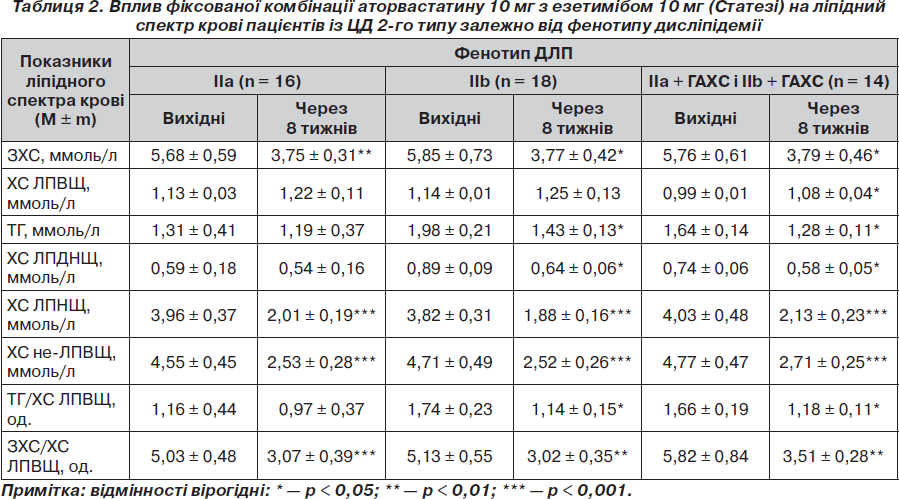
Більш поглиблений аналіз впливу фіксованої комбінації аторвастатину з езетимібом (Статезі) на ліпідний спектр крові пацієнтів із ЦД 2-го типу залежно від фенотипу ДЛП (табл. 2) дозволив установити такі особливості гіполіпідемічної дії препарату.
При ізольованій ГХС (ІІа тип ДЛП) переважним був виражений гіпохолестеринемічний ефект. Спостерігалося зниження вмісту в сироватці крові ХС ЛПНЩ на 49,4 % (р < 0,001), що погоджується з результатами інших дослідників, які застосовували комбіновану терапію в режимі езетиміб + аторвастатин у дозі 10 мг/добу упродовж більш тривалого терміну (12 тижнів) і отримали зниження аналогічного показника на 50 % [15]. У нашому дослідженні зниження рівня ХС ЛПНЩ на 49,4 % сприяло зменшенню концентрації ЗХС у крові на 33,9 % (р < 0,01). Гіпотригліцеридемічний ефект Статезі проявився лише тенденцією до зниження сироваткового вмісту ТГ і ХС ЛПДНЩ на 9,2 і 8,5 % (р > 0,05) відповідно. Схожий результат (зниження рівня ТГ лише на 7 %) отримали інші дослідники [22] при додаванні до статинотерапії езетимібу 10 мг/добу хворим на ЦД 2-го типу з вихідним умістом ТГ у крові ≤ 1,5 ммоль/л, які не досягли цільового рівня ХС ЛПНЩ при застосуванні монотерапії статином. Відзначено також тенденцію до підвищення рівня ХС ЛПВЩ на 7,9 % (p > 0,05). Обговорюючи отримані дані, слід вказати, що в раніше надрукованих роботах із вивчення статинів відсоток зниження рівня ТГ і підвищення рівня ХС ЛПВЩ залежав від вихідного значення цих показників [7, 32]: чим вищим був вихідний рівень ТГ, тим більший відсоток його зниження на тлі монотерапії статином, навпаки, чим нижче вихідне значення ХС ЛПВЩ, тим більший відсоток його підвищення. Зазначені зміни вмісту в сироватці крові ТГ і ХС ЛПВЩ у хворих на ЦД 2-го типу з ІІа типом ДЛП під впливом Статезі супроводжувалися тенденцією до зниження величини співвідношення ТГ/ХС ЛПВЩ у середньому на 16,4 % (p > 0,05).
Виражена гіпохолестеринемічна дія застосованої в дослідженні фіксованої комбінації аторвастатину з езетимібом (Статезі) поряд із тенденцією до покращення зворотного транспорту ХС під впливом такої гіполіпідемічної терапії сприяли вірогідному зниженню концентрації ХС не-ЛПВЩ на 44,4 % (p < 0,001) та величини співвідношення ЗХС/ХС ЛПВЩ на 38,9 % (р = 0,001).
У групі хворих на ГХ і ЦД 2-го типу з ІІа типом ДЛП цільового рівня ХС ЛПНЩ за 8 тижнів лікування досягли 14 (87,5 %) із 16 осіб.
У пацієнтів зі змішаним варіантом ДЛП ІІb типу, при якому ГХС поєднується з гіпертригліцеридемією (ГТГ) (n = 18) (табл. 2), гіпохолестеринемічний ефект Статезі був схожим на такий при ІІа типі ДЛП. Спостерігалося зниження концентрації ЗХС на 35,5 % (p < 0,05) переважно за рахунок зменшення вмісту ХС у складі ЛПНЩ на 50,8 % (p < 0,001). Відмічено також значно виражений порівняно з ІІа типом ДЛП гіпотригліцеридемічний ефект препарату. Вірогідне зниження сироваткового рівня ТГ у хворих на ЦД 2-го типу з ІІb типом ДЛП у середньому на 27,8 % (p < 0,05) супроводжувалося зменшенням умісту ХС у складі ЛПДНЩ на 27,7 % (p < 0,05). Імовірно, це пов’язано з вихідною ГТГ (рівень ТГ до призначення Статезі в пацієнтів із ІІb типом ДЛП на 51,1 % перебільшував аналогічний показник у хворих з ІІа типом ДЛП). Інші дослідники [20, 33] також спостерігали зниження рівня ТГ понад 20 % при вихідній ГТГ > 1,7 ммоль/л у разі додавання до статинотерапії езетимібу 10 мг/добу хворим на ЦД 2-го типу, які не досягли цільового рівня ХС ЛПНЩ на монотерапії статином.
Тенденція до підвищення ХС ЛПВЩ під впливом Статезі при ІІb типі ДЛП була більш помітною, ніж при ІІа типі (9,6 проти 7,9 %; p > 0,05), що пояснюється додатковим внеском ліпопротеїдліполізу ТГ-умісних ЛПДНЩ в утворення ЛПВЩ на тлі гіпотригліцеридемічної дії препарату. Саме за рахунок останньої спостерігалося вірогідне зниження величини співвідношення ТГ/ХС ЛПВЩ у середньому на 34,5 % (p < 0,05). Однак варто відмітити, що при ЦД 2-го типу вірогідному підвищенню ХС ЛПВЩ під впливом гіполіпідемічних втручань можуть перешкоджати якісні зміни частинок ЛПВЩ у вигляді глікозування апобілків, перекисного окислення, збільшення вмісту в них ТГ та кількості малих щільних частинок ЛПВЩ [12].
Завдяки гіпохолестеринемічній та гіпотригліцеридемічній дії Статезі у хворих на ЦД 2-го типу з ІІb типом ДЛП спостерігалося ефективне зниження концентрації ХС не-ЛПВЩ на 46,7 % (p < 0,001). Цей ефект був схожим із аналогічним при ІІа типі ДЛП (ХС не-ЛПВЩ знизився на 44,4 % (р < 0,001)). Усе це дає підставу припустити, що в обох випадках зниження вмісту ХС у складі не-ЛПВЩ переважно відбувається за рахунок впливу препарату на рівень ХС ЛПНЩ. У контексті обговорення отриманих даних підкреслимо, що ефективне зниження ХС не-ЛПВЩ має суттєве клінічне значення для хворих, оскільки існують докази того, що рівень ХС не-ЛПВЩ може розглядатися як більш сильний предиктор серцево-судинних захворювань, ніж рівень ХС ЛПНЩ, особливо в пацієнтів, які приймають статини [16, 18].
На тлі вираженої гіпохолестеринемічної дії Статезі та тенденції до підвищення вмісту ХС у складі ЛПВЩ під впливом препарату у хворих на ЦД 2-го типу з ІІb типом ДЛП спостерігалося ефективне зниження величини співвідношення ЗХС/ХС ЛПВЩ у середньому на 41,1 % (p < 0,01), що не набагато відрізнялося від аналогічного при ІІа типі ДЛП (38,9 %; р = 0,001).
17 (94,4 %) із 18 хворих з ІІb типом ДЛП досягли цільового рівня ХС ЛПНЩ при застосуванні препарату Статезі упродовж 8 тижнів.
У нашому дослідженні проаналізовано гіполіпідемічні ефекти фіксованої комбінації аторвастатину з езетимібом (Статезі) у 6 і 8 пацієнтів відповідно з ІІа та ІІb типами ДЛП, у яких виявлено ГАХС. У цій підгрупі із 14 осіб було 9 чоловіків і 5 жінок. Критерієм ГАХС для чоловіків вважали рівень ХС ЛПВЩ < 1,0 ммоль/л, для жінок — нижче 1,2 ммоль/л [19]. Середній вихідний рівень ХС ЛПВЩ у зазначеній підгрупі хворих становив 0,99 ± 0,01 ммоль/л (табл. 2).
Як свідчать дані табл. 2, у пацієнтів із ЦД 2-го типу та комбінованою ДЛП, складовою якої є ГАХС, препарат Статезі продемонстрував гіпохолестеринемічний, гіпотригліцеридемічний ефекти та спроможність вірогідно підвищувати вміст ХС у складі ЛПВЩ. Гіпохолестеринемічний ефект препарату проявився у зниженні рівня ЗХС на 34,2 % (p < 0,05) та ХС ЛПНЩ на 47,1 % (p < 0,001), гіпотригліцеридемічний — у зниженні сироваткової концентрації ТГ на 21,9 % (p < 0,05) та вмісту ХС у складі ЛПДНЩ на 21,6 % (p < 0,05). Підвищення рівня ХС ЛПВЩ за 8 тижнів лікування становило 9,1 % (p < 0,05). Інші дослідники [15] навіть при більш тривалому терміні застосування комбінованої терапії «аторвастатин + езетиміб» у режимі 10 мг/добу (12 тижнів) у хворих без ЦД 2-го типу спостерігали аналогічний ефект: рівень ХС ЛПВЩ вірогідно підвищився в середньому на 9 % порівняно з 3 % при застосуванні монотерапії аторвастатином. Обговорюючи отримані дані, слід зазначити, що окремі дослідники [26] повідомили навіть про зниження рівня ХС ЛПВЩ у хворих на ЦД 2-го типу після додавання езетимібу до симвастатину. Однак аналіз результатів більшого дослідження, що включало 786 осіб, із яких у групі пацієнтів із ЦД 2-го типу 191 хворий [31] не підтвердив суттєвого зниження рівня ХС ЛПВЩ при додаванні до статинотерапії езетимібу 10 мг/добу. При цьому слід відзначити, що вихідний уміст ХС ЛПВЩ у крові в пацієнтів із цих двох досліджень не відповідав критеріям ГАХС і становив відповідно 48 ± 11 мг/дл і 49 ± 11 мг/дл або приблизно 1,24 і 1,27 ммоль/л. Усе це свідчить про залежність підвищення рівня ХС ЛПВЩ при застосування статинів від вихідного значення показника [7].
У нашому дослідженні підвищення вмісту ХС у складі ЛПВЩ на 9,1 % (p < 0,05) у пацієнтів із ГАХС супроводжувалося вірогідним зниженням концентрації ХС не-ЛПВЩ на 43,2 % (p < 0,001) на тлі гіпохолестеринемічного і гіпотригліцеридемічного ефектів Статезі. Покращення зворотного транспорту ХС під впливом препарату позитивно відбивалося на динаміці величини співвідношення ЗХС/ХС ЛПВЩ (показник знизився на 39,7 % (р = 0,01)).
Гіполіпідемічна терапія, що спрямована на корекцію співвідношення ТГ/ХС ЛПВЩ, уважається сьогодні доречним підходом до лікування пацієнтів із метаболічним синдромом або ЦД 2-го типу з категорії високого кардіоваскулярного ризику, у яких частіше за все спостерігається одночасне порушення метаболізму ЛПВЩ і ТГ [34]. У нашому дослідженні у хворих на ЦД 2-го типу з ГАХС під впливом лікування препаратом Статезі спостерігалося вірогідне зниження величини співвідношення ТГ/ХС ЛПВЩ на 28,9 % (p < 0,05), що свідчить про доцільність застосування фіксованої комбінації аторвастатину 10 мг та езетимібу 10 мг у корекції діабетичної ДЛП або ДЛП при синдромі ІР, що супроводжується ГТГ і ГАХС за умов недосягнення хворими цільового рівня ХС ЛПНЩ на попередній статинотерапії.
Серед 14 хворих із комбінованою ДЛП, складовою якої є ГАХС, досягнення цільового рівня ХС ЛПНЩ на тлі гіполіпідемічної терапії препаратом Статезі спостерігалося в 11 (78,6 %) осіб. Серед 3 пацієнтів, які не досягли цільового значення показника, у 2 хворих ІІа тип ДЛП поєднувався з ГАХС, в 1 пацієнта мало місце поєднання ІІb типу ДЛП із ГАХС. Імовірно, цим особам для корекції порушень ліпідного обміну й досягнення цільового рівня ХС ЛПНЩ потрібна більш тривала гіполіпідемічна терапія фіксованою комбінацією аторвастатину з езетимібом.
В останні роки отримано переконливі дані про те, що маркери запалення можуть бути передвісниками тяжкості перебігу атеросклерозу, а езетиміб знижує їх рівні в крові [13, 27]. Установлено, що більш суттєве зниження такого маркера запалення, як СРБ, відбувається при поєднаному застосуванні езетимібу зі статином. Так, комбінована гіполіпідемічна терапія комбінацією «езетиміб + аторвастатин» сприяла більш вираженому зниженню рівня СРБ порівняно з монотерапією аторвастатином (на 41 і 31 % відповідно; p < 0,01), що вказує на більш виражений протизапальний ефект комбінованого лікування (аналогічне зниження рівня СРБ спостерігалося при додаванні езетимібу до інших статинів [21]). Стосовно хворих із метаболічними розладами, зокрема з порушеннями толерантності до глюкози, монотерапія езетимібом 10 мг/добу або симвастатином 20 мг/добу через 12 тижнів лікування призводила до зниження рівня СРБ, що було більш вираженим при комбінованому застосуванні препаратів (35 проти 25 %; p< 0,001) [23]. У нашому дослідженні, як свідчать дані табл. 3, застосування фіксованої комбінації аторвастатину з езетимібом (Статезі) навіть при більш короткому терміні лікування (8 тижнів) супроводжувалося вірогідним зниженням рівня СРБ на 31,3 % (p < 0,05), що можна розглядати як важливий для хворих на ЦД 2-го типу плейотропний (протизапальний) ефект препарату.
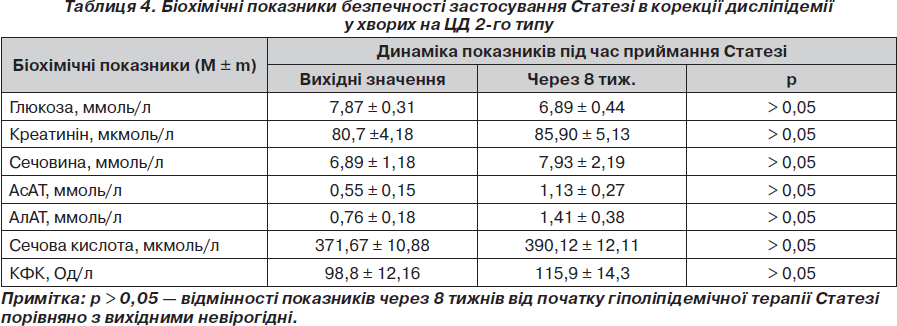
Серед інших плейотропних ефектів езетимібу у хворих на ЦД 2-го типу, відомих за останні роки, слід відзначити спроможність зменшувати ІР [27]. Так, повідомляється про позитивну динаміку індексу НОМА (індексу ІР) після призначення езетимібу 10 мг/добу хворим із ГХС, 30 % із яких мали ЦД 2-го типу або порушення толерантності до глюкози. Ці дані становлять особливий інтерес у контексті нещодавніх доказів асоціації статинотерапії з невеликим збільшенням ризику нових випадків ЦД 2-го типу [14, 28]. У цьому разі додавання езетимібу до статину було б найбільш доцільним для нейтралізації діабетичного ефекту й покращення чутливості тканин до інсуліну. У нашому дослідженні гіполіпідемічна терапія препаратом Статезі у хворих на ЦД 2-го типу супроводжувалася тенденцією до зниження рівня інсуліну натще на 9,9 % (p > 0,05), індексу ІР (індексу НОМА) — на 20,7 % (p > 0,05) (табл. 3) та глікемії натще на 12,4 % (p > 0,05) (табл. 4). Ураховуючи, що індивідуально підібрана гіпоглікемічна терапія до призначення Статезі не змінювалася упродовж 8-тижневого терміну приймання препарату, можна припустити самостійний позитивний вплив фіксованої комбінації аторвастатину з езетимібом на чутливість тканин до інсуліну завдяки зменшенню ІР.
У нашому дослідженні препарат Статезі мав задовільний профіль толерантності у хворих на ЦД 2-го типу. Побічні явища зареєстровано у 8 із 34 пацієнтів. У 2 випадках спостерігались диспептичні розлади у вигляді печії, в 1 — дискомфорт у животі, у 3 випадках — явища метеоризму, у 2 — зниження апетиту. Причому в 4 із 8 випадків не виявлено чіткого взаємозв’язку зареєстрованих явищ із прийманням препарату. В усіх 8 випадках описані зміни в самопочутті хворих мали тимчасовий характер і не потребували відміни Статезі.
У процесі дослідження не відзначено негативних змін лабораторних показників, у тому числі активності печінкових трансаміназ (АсАТ, АлАТ), КФК, рівнів креатиніну, сечової кислоти (табл. 4). Препарат справляв позитивний вплив на вуглеводний обмін, про що свідчила тенденція до зниження глікемії натще на тлі відсутності корекції добових доз гіпоглікемічних засобів.
Висновки
1. 8-тижневе застосування фіксованої комбінації аторвастатину 10 мг з езетимібом 10 мг (препарату Статезі) з метою корекції ДЛП у хворих на ГХ і ЦД 2-го типу, які не досягли цільових значень ХС ЛПНЩ при попередньому застосуванні 4-тижневої терапії аторвастатином 10 мг/добу, дозволяє знизити рівень ЗХС крові на 34,5 % (p < 0,01), уміст ХС ЛПНЩ — на 49,2 % (p < 0,001), досягти цільового рівня останнього у 91,2 % хворих. Поряд із гіпохолестеринемічною дією препарат знижує концентрацію ТГ у сироватці крові на 21,2 % (p < 0,05), сприяє тенденції до підвищення вмісту ХС у складі ЛПВЩ у середньому на 9,2 % (p > 0,05).
2. При ІІа типі ДЛП у хворих на ЦД 2-го типу спостерігається переважно гіпохолестеринемічний ефект Статезі, що проявляється вірогідним зниженням рівнів ЗХС і ХС ЛПНЩ відповідно на 33,9 % (p < 0,01) і 49,4 % (p < 0,001), зменшенням сироваткової концентрації ХС не-ЛПВЩ у середньому на 44,4 % (p < 0,001) та зниженням величини співвідношення ЗХС/ХС ЛПВЩ на 38,9 % (р = 0,001). Зниження сироваткового вмісту ТГ, підвищення рівня ХС ЛПВЩ, зменшення величини співвідношення ТГ/ХС ЛПВЩ у цьому разі має характер тенденції.
3. При змішаній ДЛП (тип ІІb) у хворих на ЦД 2-го типу окрім гіпохолестеринемічного (зниження рівнів ЗХС на 35,5 % (p < 0,05), ХС ЛПНЩ — на 50,8 % (p < 0,001)) спостерігається гіпотригліцеридемічний ефект Статезі, що проявляється зниженням сироваткового вмісту ТГ у середньому на 27,8 % (p < 0,05). Підвищення концентрації ХС ЛПВЩ на 9,6 % (p > 0,05) має характер тенденції. Зазначені гіполіпідемічні ефекти препарату при ІІb типі ДЛП сприяють зниженню рівня ХС не-ЛПВЩ на 46,5 % (p < 0,001) та величин співвідношень ТГ/ХС ЛПВЩ і ЗХС/ХС ЛПВЩ відповідно на 34,5 % (p < 0,05) і 41,1 % (p < 0,01).
4. При комбінованій ДЛП (поєднанні ІІа і ІІb типів із ГАХС) у хворих на ЦД 2-го типу 8-тижневе застосування Статезі призводить до зниження рівнів ЗХС на 34,2 % (p < 0,05), ХС ЛПНЩ — на 47,1 % (p < 0,001)), ТГ — на 21,9 % (p < 0,05) та вірогідного підвищення рівня ХС ЛПВЩ на 9,1 % (p < 0,05). Відповідно до цих змін відбувається зменшення вмісту в сироватці крові ХС не-ЛПВЩ у середньому на 43,2 % (p < 0,001) та зниження величин співвідношень ТГ/ХС ЛПВЩ і ЗХС/ХС ЛПВЩ відповідно на 28,9 % (p < 0,05) і 39,7 % (р = 0,01), що свідчить про покращення стану системи зворотного транспорту ХС та системи ліпопротеїдліполізу.
5. Препарат Статезі справляє у хворих на ЦД 2-го типу з ДЛП корисні плейотропні ефекти, що проявляються у вірогідному зниженні концентрації СРБ у крові на 31,3 % (p < 0,05), тенденції до зменшення інсулінемії та глікемії натще відповідно на 9,9 і 12,4 % (p > 0,05), індексу НОМА — на 20,7 % (p > 0,05).
6. Гіполіпідемічний препарат Статезі є безпечним у застосуванні у хворих на ЦД 2-го типу з ДЛП і має задовільний профіль толерантності. Він не спричиняє суттєвих побічних ефектів, що потребують змін добової дози або припинення лікування. Статезі можна безпечно й успішно застосовувати в корекції ІІа, ІІb типів ДЛП та при їх поєднанні з ГАХС.
1. Бубнова М.Г., Аронов Д.М., Перова Н.В. и др. Правастатин в коррекции атерогенной экзогенно-индуцированной постпрандиальной гиперлипидемии // Кардиология. — 2002. — № 1. — С. 27-32.
2. Комаров Ф.И., Коровкин Б.Ф., Меньшиков В.В. Биохимические исследования в клинике. — Элиста: Джангар, 1999. — 250 с.
3. Липовецкий Б.М. Клиническая липидология. — Санкт-Петербург: Наука, 2000. — 119 с.
4. Лутай М.І. Дисліпідемії: клінічне значення та класифікації // Нова медицина. — 2003. — № 4(9). — С. 16-21.
5. Лутай М.И., Лысенко А.Ф., Пономарева Г.В. Клинический опыт применения препарата Вабадин (Симвастатин) для коррекции дислипидемии в условиях клинической практики // Артериальная гипертензия. — 2009. — № 6(8). — С. 10-14.
6. Рекомендації Української Асоціації кардіологів з профілактики та лікування артеріальної гіпертензії. Посібник до Національної програми профілактики і лікування артеріальної гіпертензії. — К.: ПП ВМВ, 2008. — 80 c.
7. Рожкова Т.А., Сусеков А.В., Соловьева Е.Ю. и др. Эффективность и переносимость статинов у больных с первичными гиперлипидемиями в амбулаторной клинической практике // Кардиология. — 2005. — № 9. — С. 32-34.
8. Смирнова І.П. Дисліпопротеїдемії: методи діагностики та епідеміологія // Нова медицина. — 2003. — № 4(9). — С. 22-25.
9. Сусеков А.В. Аторвастатин: от контролируемых исследований до повседневной практики // Здоров’я України. — 2009. — Тематичний номер. Червень. — С. 16-17.
10. Чернишов В.А. Подвійне блокування абсорбції та синтезу холестерину в корекції дисліпідемій // Укр. терапевт. журн. — 2011. — № 1. — C. 97-102.
11. Шатило В.Б., Ищук В.А. Применение Статези — современный подход к снижению липопротеинов низкой плотности в лечении кардиоваскулярной патологии // Медицина неотложных состояний. — 2010. — №3(28). — С. 130-135.
12. Яфасов К.М., Дублянская Н.В. Дислипидемия при сахарном диабете II типа: патогенез и лечение // Кардиология. — 2001. — № 9. — С. 74-77.
13. Athyros V.G., Kakafika A.I., Karagiannis A. et al. Do we need to consider inflammatory markers when we treat atherosclerotic disease? // Atherosclerosis. — 2008. — Vol. 200. — P. 1-12.
14. Athyros V.G., Tziomalos K., Karagiannis A. et al. Lipid-lowering agents and new onset diabetes mellitus // Expert Opin. Pharmacother. — 2010. — Vol. 11. — P. 1965-1970.
15. Ballantyne C., Houri J., Notarbartolo A. et al. Effect of ezetimibe coadministered with atorvastatin in 628 patients with primary hypercholesterolemia. A prospective, randomized, double-blind trial // Circulation. — 2003. — Vol. 107. — P. 2409-2415.
16. Brunzell J.D., Davidson V., Furberg C.D. et al. Consensus Conference Report. Lipoprotein management in patients with cardiometabolic risk // J. Am. Coll. Cardiol. — 2008. — Vol. 51. — P. 1512-1524.
17. Cheng A.Y., Leiter L.A. Clinical use of ezetimibe // Can. J. Clin. Pharmacol. — 2003. — Vol. 10 (Suppl. A). — P. 21A-25A.
18. Denke M.A. Weighing in before the fight: low-density lipoprotein cholesterol and non-high-density lipoprotein cholesterol versus apolipoprotein В as a best predictor for coronary heart disease and the best measure of therapy // Circulation. — 2005. — Vol. 112. — P. 3868-3870.
19. Fourth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular disease prevention in clinical practice: executive summary // Eur. Heart J. — 2007. — Vol. 28. — P. 2375-2414.
20. Fras Z., Mikhailidis D.P. Statin plus ezetimibe treatment in clinical practice: The SL-SPECT (Slovenia (SL) Statin Plus Ezetimibe in Cholesterol Treatment) monitoring of clinical practice // Curr. Med. Res. Opin. — 2008. — Vol. 24. — P. 2467-2476.
21. Gagne C., Bays H., Weiss S. et al. Efficacy and safety of ezetimibe added to ongoing statin therapy for treatment of patients with primary hypercholesterolemia // Am. J. Cardiol. — 2002. — Vol. 90, № 10. — P. 1084-1091.
22. Gazi I.F., Daskalopoulou S.S., Nair D.R. et al. Effect of ezetimibe in patients who cannot tolerate statins or cannot get to the low-density lipoprotein cholesterol target despite taking a statin // Curr. Med. Res. Opin. — 2007. — Vol. 23. — P. 2183-2192.
23. Kater A.L., Batista M.C., Ferrera S.R. Synergistic effect of simvastatin and ezetimibe on lipid and proinflammatory profiles in pre-diabetic subjects // Diabetol. Metab. Syndr. — 2010. — Vol. 2. — P. 34.
24. Lamon-Fava S., Diffenderfer M.R., Barrett P.H. et al. Effects of different doses atorvastatin on human apolipoprotein B-100, B-48, and A-I metabolism // J. Lipid Res. — 2007. — Vol. 48, № 8. — P. 1746-1753.
25. Ludman A., Venugopal V., Yellon D.M., Hausenloy D.J. Statins and cardioprotection — More than just lipid lowering? // Pharmacol. and Therapeut. — 2009. — Vol. 122. — P. 30-43.
26. Ruggenenti P., Cattaneo D., Rota S. et al. Effects of combined ezetimibe and simvastatin therapy as compared to simvastatin alone in patients with type 2 diabetes: a prospective, randomized, double blind, clinical trial // Diabetes Care. — 2010. — Vol. 133. — P. 1954-1956.
27. Sarigianni M., Katsiki N., Mikhailidis D.P. Ezetimibe in diabetes: more than cholesterol lowering // Curr. Med. Res. Opin. — 2010. — Vol. 26, № 10. — P. 2517-2520.
28. Sattar N., Preiss D., Murray H.M. et al. Statins and risk of incident diabetes: a collaborative meta-analysis of randomized statin trials // Lancet. — 2010. — Vol. 375. — P. 735-742.
29. Schwartz G.G., Olsson L.G., Szarek M., Sasiela W.J. Relation of Characteristics of Metabolic Syndrome to Short-Term Prognosis and Effects of Intensive Statin Therapy After Acute Coronary Syndrome // Diabetes Care. — 2005. — Vol. 28. — P. 2508-2513.
30. Shinichiro M., Keijiro S. Ezetimibe, a selective inhibitor of the transport of cholesterol // Inter. Med. — 2008. — Vol. 47. — P. 1165-1170.
31. Simons L., Tonkon M., Masana L. et al. Effects of ezetimibe added to on-going statin therapy on the lipid profile of hypercholesterolemic patients with diabetes mellitus or metabolic syndrome // Curr. Med. Res. Opin. — 2004. — Vol. 20. — P. 1437-1445.
32. Stein E., Lane M., Laskarzewski P. et al. Comparison of Statins in Hypertriglyceridaemia // Am. J. Cardiol. — 1998. — Vol. 81(Suppl. 4A). — P. 66B-69B.
33. Tomassini J.E., Mazzone T., Goldberg R.B. et al. Effect of ezetimibe/simvastatin compared with atorvastatin on lipoprotein subclasses in patients with type 2 diabetes and hypercholesterolaemia // Diabetes Obes. Metab. — 2009. — Vol. 11. — P. 855-864.
34. Wild S.H., Byrne C.D. Коррекция липидного профиля в снижении кардиоваскулярного риска у пациентов с метаболическим синдромом или сахарным диабетом 2 типа // Практична ангіологія. — 2006. — № 2(03). — С. 57-60.
35. World Health Organization. Definition, diagnosis and classification of diabetes mellitus and its complications. Report of WHO consultation: Part 1. Diagnosis and classification of diabetes mellitus. — Geneva, 1999. — P. 1-59.