Международный неврологический журнал 3 (41) 2011
Вернуться к номеру
Эпимил в лечении эпилепсии у женщин молодого возраста
Авторы: Литовченко Т.А., Харьковская медицинская академия последипломного образования
Рубрики: Неврология
Версия для печати
Эпилепсия у женщин молодого возраста сопровождается патологией репродуктивной сферы гораздо чаще, чем в популяции. Патогенез патологии репродуктивной системы, по-видимому, мультифакторный, зависящий как от течения эпилепсии, так и от применяемых АЭП. Эпимил (ламотриджин) является препаратом выбора для лечения эпилепсии у женщин репродуктивного возраста, так как по эффективности не отличается от наиболее распространенных АЭП и при этом обладает минимальными побочными действиями на женский организм.
Эпилепсия у женщин, антиэпилептическая терапия, патология репродуктивной сферы.
Лечение эпилепсии у женщин является сложной проблемой. Не случайно в последние 10–20 лет гендерному аспекту терапии эпилепсии уделяется повышенное внимание [7, 9]. Это обусловлено, с одной стороны, рядом физиологических особенностей женского организма, психологическими и социальными особенностями, а с другой — значительными побочными влияниями антиэпилептической терапии на женский организм. Особенную сложность представляет собой лечение эпилепсии у женщин в периоды физиологических гормональных изменений: пубертатный период, беременность, роды и лактация, климакс. Кроме того, женскому организму присуща месячная цикличность изменения гормонального фона. С этими гормональными изменениями связан ряд специфических форм эпилепсии и эпилептических синдромов: полозависимые синдромы Айкарди и Ретта, катамениальная эпилепсия, фотосенситивная эпилепсия [2, 8].
Эпилептические припадки, в свою очередь, оказывают неблагоприятное воздействие на гормональный статус, нарушают процессы полового созревания, показатели фертильности, обладают значимым тератогенным действием. Женщины с эпилепсией имеют более низкие коэффициенты рождаемости, частые ановуляторные менструальные циклы. Менструальные нарушения (аменорея, менометроррагия, олигоменорея) наблюдаются у 1/3 женщин с эпилепсией по сравнению с 12–14 % случаев в популяции; ановуляторный цикл — у 1/3 по сравнению с 8–10 %; синдром поликистозных яичников (СПКЯ — овуляторная дисфункция, гиперандрогенизм, гиперандрогенемия, поликистоз яичников) — у 10–20 % женщин с эпилепсией при 4–10 (20) % в популяции [2, 8]. На 2009 г. до 3,8 % материнской смертности составляет смертность женщин с эпилепсией, при том что распространенность эпилепсии среди беременных — 0,3–0,4 % случаев [2, 7].
Снижение фертильности у женщин, страдающих эпилепсией, объясняется несколькими причинами. В первую очередь это структурно-функциональные особенности гипоталамо-гипофизарно-гонадной системы и взаимосвязь с лимбической системой. Персистирование эпилептической активности приводит к дисфункции этих структур и изменению гормонального статуса, снижению уровня эстрогенов. Эпилептические припадки вызывают повышение уровня пролактина, который подавляет овуляцию, влияя на гипоталамо-гипофизарно-надпочечниковую систему. Прием многих базовых антиэпилептических препаратов (АЭП) — фенитоина, карбамазепина, фенобарбитала, примидона, тиагабина — усиливает синтез гормонсвязывающих белков и индуцирует повышение активности печеночных ферментов [4, 7]. Это приводит к снижению концентрации эндогенных свободных половых гормонов в плазме крови.
Несмотря на незначительное превалирование в популяции больных эпилепсией мужского пола, в пубертатном периоде (манифестация в 10–14 лет существенно преобладает у девочек, на этот возраст приходится второй пик заболеваемости после раннего детского возраста) и до 30 лет, а также после 70 лет значимо преобладает распространенность эпилепсии у женщин [2].
Пубертатный период характеризуется началом циклического функционирования гипоталамо-гипофизарно-гонадной системы с альтернативным влиянием стероидных (эстрадиол и прогестерон) половых гормонов на эпилептическую активность и значительным повышением обменных процессов. В пубертатном периоде дебютирует и так называемая катамениальная (менструальная) эпилепсия, при которой эпилептические приступы тесно связаны с определенной фазой менструального цикла. Отмечается значительное преобладание генерализованных судорожных эпиприпадков в структуре катамениальной эпилепсии. Еще Гиппократ указывал, что задержка mensis может способствовать развитию припадков [2, 9].
Обычно эпилептические приступы учащаются в перименструальный период, но возникают и в другое время и гораздо реже (около 12 %) связаны только с определенной фазой цикла. Наибольшая частота приступов отмечается при нарастании уровня эстрадиола и снижении прогестерона в крови (лютеиновая фаза и первые дни менструации). Нейроэндокринные расстройства выявляются у 58 % пациенток с катамениальной эпилепсией (гиперпролактинемический синдром, поликистоз яичников, гипотиреоз) [4].
Одним из приоритетных направлений при эпилепсии у женщин по праву является лекарственная терапия, однако учет только соответствия назначаемого препарата форме эпилепсии и типу эпилептических припадков недостаточен. Лекарственный аспект предполагает учет взаимодействия АЭП (или нескольких совместно назначаемых противоэпилептических препаратов) между собой, с гормональными контрацептивами, влияние препаратов на менструальный цикл, показатели фертильности.
При назначении медикаментозного лечения эпилепсии у женщин необходимо учитывать возможность взаимодействия АЭП не только с гормональными контрацептивами, но и с гормональными препаратами, которые нередко назначаются женщинам в качестве заместительной терапии во время менопаузы или при лечении заболеваний половой сферы.
К сожалению, назначение таких эффективных и наиболее широко применяемых антиэпилептических препаратов, как вальпроаты, фенитоин, карбамазепины может быть нежелательно в пубертатном периоде и у молодых женщин: вальпроаты в период полового созревания вызывают поликистоз яичников, нарушения менструального цикла, мастопатию, прибавку веса; длительное применение фенитоина приводит к ряду косметических дефектов, карбамазепины, индуцируя ферментативную систему, снижают эффективность гормональных контрацептивов и заместительной гормональной терапии. Кроме того, прием энзиминдуцирующих АЭП приводит к нарушению минерального обмена костной ткани и, как следствие, к развитию остеопороза.
Лечение эпилепсии у женщин требует учета особенностей функционирования эндокринной системы в различные периоды. Наиболее адекватным представляется выбор эффективного препарата, оказывающего наименьшее количество негативных эффектов на функцию гипоталамо-гипофизарно-эндокринной системы, особенно у женщин детородного возраста. При высокой эффективности ламотриджин лишен ряда неблагоприятных влияний на женский организм. Применение ламотриджина в периоды изменения веса пациенток (интенсивный рост, беременность) обычно не требует частой коррекции дозы, что благоприятно сказывается на эффективности лечения. По данным International Lamotrigine Pregnancy Registry, риск «больших» дефектов плода при использовании ламотриджина в монотерапии не превышает 2,9 % [3, 5, 6], что практически не превышает аналогичный показатель в популяции (2,3 %), хотя некоторые авторы говорят о дозозависимом (свыше 200 мг/сут) повышении риска развития мальформаций. Ламотриджин не вызывает прибавки веса и косметических дефектов, изменения метаболизма эндогенных и экзогенных половых гормонов, остеопороза, не влияет на печеночные ферменты. Препарат эффективен при ряде гормонально-зависимых эпилептических синдромов у женщин.
Целью настоящего исследования является уточнение клинической эффективности и безопасности применения ламотриджина (Эпимил) для лечения парциальной эпилепсии у женщин.
Материалы и методы исследования
Обследовано 70 больных эпилепсией (1-я группа) в возрасте от 16 до 35 лет (средний возраст 23,2 ± 5,2 года) с длительностью заболевания не менее 2 лет (в среднем 6,8 ± 2,1 года), которые принимали ламотриджин (Эпимил) на протяжении не менее 1 года в качестве монотерапии (в среднем 4,5 ± 1,3 года) в дозировке от 150 до 250 мг/сут. Выбор препарата обусловлен его минимальным влиянием на гормональный фон, отсутствием взаимодействия с гормональными контрацептивами, отсутствием изменений веса, косметических дефектов, минимальной тератогенностью. Выбор торговой формы ламотриджина — Эпимила (производитель Teva) был обусловлен оптимальным сочетанием цена/качество и соответствием препарата международным требованиям GMP (подтвержденным плазмоконцентрацией).
Группу сравнения составили 56 женщин, больных эпилепсией (2-я группа), с длительностью заболевания не менее 2 лет (7,1 ± 3,4 года), принимавших карбамазепин или препараты вальпроевой кислоты в виде моно- или дуотерапии на протяжении не менее 1 года (4,9 ± 1,6 года) в средних терапевтических дозировках.
Оценка обследованных больных проводилась на основании клинических данных, жалоб больных, данных нейрофизиологического и нейровизуализационного исследований [1, 2, 9]. Всем больным проводилось гинекологическое консультирование и ультразвуковое исследование матки и яичников. Катамнез прослежен на протяжении 3,0 ± 0,4 года.
Результаты исследования и обсуждение
Всем пациенткам было проведено полное клиническое исследование, электроэнцефалографическое исследование в динамике с диагностической целью и для подтверждения эффективности лечения, нейровизуализационное исследование (магнитно-резонансная томография) для исключения прогрессирующих заболеваний, неопластических процессов и выявления возможной этиологии заболевания.
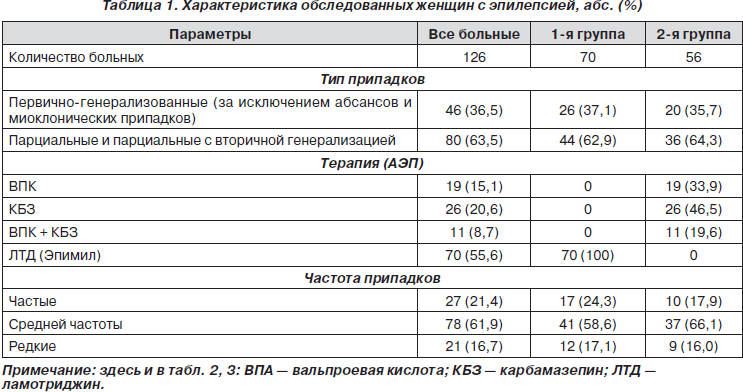
У женщин группы исследования и группы сравнения в 36,5 % случаев были первично-генерализованные припадки, в 63,5 % — парциальные припадки и парциальные припадки с вторичной генерализацией. Из них с частыми эпилептическими припадками было 21,4 %, с припадками средней частоты — 61,9 % и с редкими приступами — 16,7 % больных. Основное количество пациенток было на монотерапии, только 9 человек (8,7 %) получали дуотерапию комбинацией вальпроатов и карбамазепина, из них 6 больных были с частыми припадками (табл. 1).
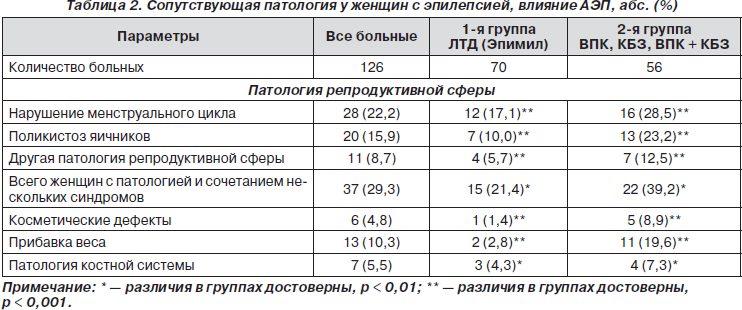
Патология репродуктивной сферы оценивалась по данным анамнеза (нарушение сроков полового созревания, нарушения менструального цикла, невынашивание беременности и патология беременности, бесплодие) и по данным гинекологического осмотра и ультразвукового исследования (нарушение развития внутренних половых органов, поликистоз яичников, мастопатия). Также оценивали наличие косметических дефектов (гирсутизм, алопеция, кожные проявления), изменения массы тела (прибавка веса), жалобы со стороны костной системы (боли в костях, повреждение/выпадение зубов, общая слабость) (табл. 2).
Анализ данных табл. 2 наглядно показывает, что в обеих группах обследованных больных выявлялась патология репродуктивной сферы и нарушения обмена, приводящие к прибавке веса, патологии костной системы и косметическим дефектам. Однако пациентки, длительно принимающие Эпимил в средних терапевтических дозировках, имели такую сопутствующую патологию достоверно реже.
Обращает на себя внимание то, что прибавка веса и поликистоз встречались значительно чаще у больных, принимавших препараты вальпроевой кислоты в виде монотерапии или в сочетании с карбамазепином, однако небольшое количество больных не позволяет сделать статистически обоснованный вывод.
При анализе анамнестических данных нами установлено, что на развитие патологии репродуктивной сферы решающее влияние оказывает возраст дебюта заболевания и возраст начала терапии АЭП. При анализе анамнестических данных и сравнении женщин с дебютом заболевания и началом терапии АЭП в возрасте до 26 лет определено, что дисфункция репродуктивной сферы различной степени выраженности развилась у 46,6 % (14 чел.) пациенток, получавших вальпроевую кислоту в виде моно- или дуотерапии, у 26,9 % (7 чел.), получавших карбамазепин, и только у 21,4 % (15 чел.) женщин, получавших Эпимил. При начале заболевания и лечения после 26 лет нарушения репродуктивной сферы развиваются значительно реже в обеих группах (21,4 % в первой группе и 25 % — во второй группе больных). Причем существует четкая тенденция превалирования таких нарушений у пациенток с началом лечения в пубертатном периоде.
Можно отметить, что при отмене лечения АЭП или замене препарата при наблюдении в течение 2–3 лет у женщин отмечается тенденция к нормализации нарушений репродуктивной сферы (нормализация менструального цикла, восстановление овуляторных циклов), однако незначительное количество наблюдений (9 женщин) не позволяет сделать обоснованный вывод об обратимости эндокринной дисфункции у женщин.
Кроме того, применение Эпимила редко приводит к изменению веса, косметическим дефектам или нарушению минерального обмена (патологии костной системы — остеопорозу), что объясняется отсутствием влияния препарата на ферменты печени и особенностями его метаболизма (табл. 2).
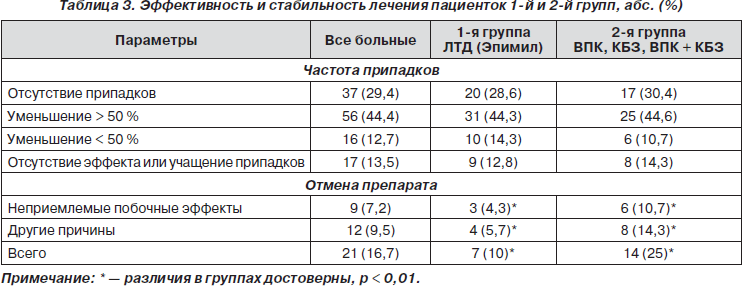
Для оценки эффективности проводимой антиэпилептической терапии мы использовали стандартные показатели: полный контроль припадков, уменьшение частоты припадков > 50 %, уменьшение частоты < 50 %, отсутствие эффекта или учащение припадков. Также мы учитывали стабильность лечения пациенток в двух группах (отмена препарата из-за побочных эффектов, планирования беременности или по другим причинам — экономические, неэффективность, неудобство приема, необходимость частого контроля или изменения дозы и др.) (табл. 3).
Эффективность лечения в обеих группах была одинаковой, выявленные незначительные различия недостоверны. Однако при анализе стабильности лечения (приверженности пациенток к терапии) группы достоверно отличаются (табл. 3). Больные, принимавшие Эпимил, отказывались от лечения вследствие неприемлемых побочных явлений только в 3 случаях (4,3 %). Причем только в одном из них отмена препарата была произведена по медицинским показаниям (у одной пациентки была кожная реакция из-за быстрой титрации дозы), а в двух других пациентки настояли на изменении терапии (сонливость, слабость, тошнота).
При приеме карбамазепина и вальпроата неприемлемые побочные эффекты терапии наблюдались значительно чаще (10,7 %): нарушения менструального цикла, поликистоз яичников, нарушения костной системы, выраженная прибавка веса. Среди других причин отмены препарата в 1-й группе больных (5,7 %) пациентки чаще всего называли недостаточную эффективность терапии. Во 2-й группе: недостаточная эффективность терапии, желание планировать беременность и опасение тератогенного действия АЭП, необходимость частого контроля и изменения дозировки и др. (14,3 %). Различия по этому показателю также статистически достоверны.
Таким образом, у женщин молодого возраста, больных эпилепсией, патология репродуктивной сферы определяется значительно чаще, чем в популяции. Вероятно, это является следствием как самого заболевания, так и приема АЭП. Эпилептическая активность вызывает дисфункцию нейрорегуляторных систем, кроме того, нейромедиаторные изменения приводят к нарушению секреции регуляторных гормонов. С другой стороны, антиэпилептические препараты зачастую являются причиной изменения секреции половых стероидов и других метаболических нарушений. Патогенез патологии репродуктивной системы, по-видимому, мультифакторный, зависящий как от течения заболевания, так и от применяемых АЭП.
Эпимил (ламотриджин) может быть препаратом выбора для первой монотерапии у женщин фертильного возраста. Препарат так же эффективен [5, 6], как и вальпроаты и карбамазепин при лечении парциальных, вторично-генерализованных и первично-генерализованных припадков (за исключением абсансов и миоклонических припадков), при этом обладает минимумом побочных эффектов на женскую половую сферу и метаболизм.
Выводы
— Эпилепсия и антиэпилептические препараты приводят к репродуктивным нарушениям у женщин молодого возраста.
— Развитие патологии репродуктивной системы зависит от возраста дебюта эпилепсии, начала противоэпилептического лечения и применяемых АЭП.
— Эпимил (ламотриджин) является препаратом выбора для лечения эпилепсии у женщин репродуктивного возраста, так как по эффективности не отличается от наиболее распространенных АЭП (карбамазепин и вальпроат) и при этом обладает минимальными побочными действиями на женский организм.
1. Евтушенко С.К., Омельяненко А.А. Клиническая электроэнцефалография у детей. — Донецк: Донеччина, 2005. — 860 с.
2. Карлов В.А. Эпилепсия у детей и взрослых, женщин и мужчин. — М.: Медицина, 2010. — 718 с.
3. Cunnington M., Tennis P. Lamotrigine and the risk of malformations in pregnancy // Neurology. — 2005. — V. 64. — P. 955-960.
4. Luef G., Rauchenzauner M. Epilepsy and hormones: A critical review. — Epilepsy &Behavior, 2009. — doi:10.1016/j.yebeh.2009.02.022
5. Marson A.G., Al-Kharisi A.M., Alwaidh M., Appleton R. et al. The SANAD study of effectiveness of valproate, lamotrigine, or topiramate for generalized and unclassifiable epilepsy: an unblended randomized controlled trial // Lancet. — 2007. — Vol. 369. — P. 1000-1015.
6. Morrow J. The XX factor: Treating women with antiepileptic drugs. — UK, National Services for Health Improvement, 2009. — 80 p.
7. Panayiotopoulos C.P. Therapy in the epilepsies. — USA, Springer, 2010. — 235 p.
8. Shorvon S., Perucca E., Endgel J. The treatment of Epilepsy (third edition). — Wieley-Blackwell, 2009. — 1060 p.